Предлагаем ДДГ водоотливной насос, насос десульфурации ДДГ, передачи, мощности ДДГ завод водоотливной насос, циркуляционный насос десульфурации ДДГ из Китая Пзготовителей
КАТЕГОРИИ ТОВАРОВ
Центробежный шламовый насос
Гравий земснаряда насос
Десульфация ДДГ насос
Пенный шламовый насос
Насос нефтехимических процессов
Насос сточных вод канализации
Центробежный насос
Части шламового насоса
OEM и сопутствующих товаров
Шламовый насос
- Горизонтальные шламовые насосы
Самовсасывающий насос
Магнитный насос
Диафрагменный насос
Винтовой насос
Химический насос
Многоступенчатый насос
Трубопроводный насос
Вакуумный насос
Погружные насосы
Просмотр в виде :
Свяжитесь сейчас
Насос для сероочистки серии DT
Свяжитесь сейчас
Насос для сероочистки серии BHR (P) BLR и SP (R)
Свяжитесь сейчас
Шламовый насос FGD для обессеривания TL (R)
Свяжитесь сейчас
Насос десульфурации высокого качества
-
Свяжитесь сейчас
ДДГ насос Десульфурации дымовых газов
Свяжитесь сейчас
ДДГ силовой установки вертикального насоса
Свяжитесь сейчас
Высокая производительность ДДГ промышленный насос
Свяжитесь сейчас
Циркуляционный насос десульфурации ДДГ
Насос для сероочистки серии DT
марка: БОДА
Подробности Упаковки: Деревянная коробка
Способность поставки: 500
Количество минимального заказа: 1 Set/Sets
Сертификаты : ISO
Описание товара Технические характеристики сероочистного насоса серии DT A.
 OEM добро пожаловать б. высокоэффективный c. экономия энергии г. ISO9001, CE Насос сероочистки серии DT 1, Обзор производства: В ограничительных деталях насоса используется передовая технология моделирования потока, чтобы гарантировать…
OEM добро пожаловать б. высокоэффективный c. экономия энергии г. ISO9001, CE Насос сероочистки серии DT 1, Обзор производства: В ограничительных деталях насоса используется передовая технология моделирования потока, чтобы гарантировать…Свяжитесь сейчас
Насос для сероочистки серии BHR (P) BLR и SP (R)
марка: НАСОС БОДА
Подробности Упаковки: Деревянная коробка
Способность поставки: 500
Количество минимального заказа: 1 Piece/Pieces
Модель: BODA-002
В соответствии с особыми требованиями международных отраслевых стандартов и регулирующими SO2, эксплуатация системы FGD на всех угольных электростанциях в мире доказала, что формованная резиновая футеровка в сочетании с насосом обессеривания является наиболее разумной.
 ниже, чем с металлической футеровкой, а срок ее…
ниже, чем с металлической футеровкой, а срок ее…Свяжитесь сейчас
Шламовый насос FGD для обессеривания TL (R)
марка: НАСОС БОДА
Подробности Упаковки: Деревянная коробка
Способность поставки: 500
Количество минимального заказа: 1 Piece/Pieces
Модель: BD-001
Насос для сероочистки серии TL (R) Серия насосов для сероочистки TL (R) D: 350-1000 мм Q: 1500-14000 м3 / ч Высота: 12-32 м Описание товара: 1 ) Ограничительные части насоса используют передовую технологию моделирования потока, чтобы гарантировать надежность конструкция насоса и высокий КПД. 2 ) Антикоррозия &…
Свяжитесь сейчас
марка: BODA
Подробности Упаковки: Деревянная коробка
Способность поставки: 500
Количество минимального заказа: 1 Set/Sets
Сертификаты : ISO9901
Насос сероочистки Наша компания может обрабатывать импортные и отечественные насосы десульфурации, и мы можем обработать детали насоса десульфурации, если вы предоставите чертежи.
 Наша компания может обрабатывать импортные и отечественные насосы десульфурации, и мы можем обработать детали насоса десульфурации, если вы…
Наша компания может обрабатывать импортные и отечественные насосы десульфурации, и мы можем обработать детали насоса десульфурации, если вы…Свяжитесь сейчас
ДТ серии Сероочистке насос 1,Обзор Продукции: Насос ограничивающие части принимают передовую технологию имитации подачи для того чтобы гарантировать надежную конструкцию насоса и высокую эффективность Operating. Анти-коррозии и анти-износа металла и резиновых материалов, которые специально разработаны для насосов ДДГ…
Свяжитесь сейчас
ДДГ силовой установки вертикального насоса
ДДГ Мощность отстойник завода насос Описание: Насосы БВ вертикальные, центробежные насосы slurry погруженные в воду в грязевике для работы.
 Они конструированы для поставлять истирательную, большую частицу и суспензий высокой плотности. Эти насосы нет необходимости любой воды уплотнения и запечатывания вала. Они также…
Они конструированы для поставлять истирательную, большую частицу и суспензий высокой плотности. Эти насосы нет необходимости любой воды уплотнения и запечатывания вала. Они также…Свяжитесь сейчас
Высокая производительность ДДГ промышленный насос
Описание производства ОбзорНасос десульфурации TL DT широко используются для передачи известняка и известковая штукатурка с содержанием ионов хлора Макс. 60000, PH значение 2,5-13. системы ДДГ. ОсобенностиВысокой эффективностью, износ и коррозионная стойкость, низкий уровень вибрации и шума, работает стабильно,…
Свяжитесь сейчас
Циркуляционный насос десульфурации ДДГ
Описание продукта:1) ограничение частей насоса принять расширенный потока технологии моделирования гарантировать надежный насос дизайн и высокая эффективность.
 2) антикоррозионная и противоизносных металла и резины материалы, которые специально разработаны для насосов ДДГ оказались на практике, что они могут обеспечить…
2) антикоррозионная и противоизносных металла и резины материалы, которые специально разработаны для насосов ДДГ оказались на практике, что они могут обеспечить…Свяжитесь сейчас
Китай Десульфация ДДГ насос Поставщики
1) ДДГ насос ограничение частей принять расширенный потока технологии моделирования гарантировать надежный насос дизайн и высокая эффективность.
2) антикоррозионная и противоизносных металла и резины материалы, которые специально разработаны для насосов ДДГ оказались на практике, что они могут обеспечить долгую жизнь работы насоса.
3) это легко для поддержания и ремонта, и это на необходимости демонтажа входе и выходе воды трубы.

Принят контейнерных механическое уплотнение, специально используется для процесса установки по десульфуризации и его эксплуатации является надежным.
Мы разработали новый вид специализированный материал, который обладает дуплекс нержавеющая сталь антикоррозионные свойства и высокий белый хром железа анти абразивный ДДГ процесса.
В резиновый корпус насоса, рабочее колесо, всасывающая крышка/крышка изготовлены из специализированных противоизносные и антикоррозионных материалов: Материал передней лайнера, обратно лайнера и вставить обратно лайнера, натуральный каучук, имеющие отличные антикоррозионные свойства.
ДДГ мощность завода водоотливной насос и циркуляционный насос десульфурации ДДГ главным образом используются для обработки шлама с дымом в поглощение башня, электрическая мощность станции
Это тепловой электростанции проекта ДДГ (сероочистки дымовых газов).
Горячие продукты
10-дюймовый центробежный горизонтальный шламовый насос
Вертикальный Водоотливной Насос Slurry
Высокая хром сплава погружной шламовый насос
Бак Для Пенообразователя Пена Шламовый Насос
Песочный насос для дноуглубительных машин
Речной Песок Всасывания Земснаряда Насос
Насос для подкачки труб
Взаимозаменяемые глянцевое хромовое сплава шламовый насос частей
Прайс-лист центробежного насоса для добычи угля
Шламовый насос пу крыльчатка частей
Циркуляционный насос десульфурации ДДГ
Шламовый насос Резиновые вкладыши Насос для сточных вод
Горизонтальная многошаговая центробежная водяная помпа
API610 Химический насос нефтехимических процессов
Фабрика оптом электродвигатель водяной насос
Самодельный десульфатор схема
Главное, в своих экспериментах обязательно ставьте на клеммы реле неполярный конденсатор, дабы не засорять радиэфир помехами от дребезга контактов. Работает на самом деле отлично! Только у меня вопрос такой : 2 Ампера ток заряда от ибп, параллельно к акуму подключена 3х ваттная лампочка, следоватьльно идет заряд- разряд, что и есть самое эффективное? Уважаемый изобрегатель!
Работает на самом деле отлично! Только у меня вопрос такой : 2 Ампера ток заряда от ибп, параллельно к акуму подключена 3х ваттная лампочка, следоватьльно идет заряд- разряд, что и есть самое эффективное? Уважаемый изобрегатель!
Поиск данных по Вашему запросу:
Схемы, справочники, даташиты:
Прайс-листы, цены:
Обсуждения, статьи, мануалы:
Дождитесь окончания поиска во всех базах.
По завершению появится ссылка для доступа к найденным материалам.
Содержание:
- Самое простое, но самое правильное зарядное устройство
- Восстановление кислотных аккумуляторов
- Зарядка аккумулятора асимметричным током
- ДЕСУЛЬФАЦИЯ АВТОМОБИЛЬНЫХ АККУМУЛЯТОРОВ
- Способы десульфатации кислотного автомобильного аккумулятора
- Форум РадиоКот • Просмотр темы — Десульфатор и зарядка
ПОСМОТРИТЕ ВИДЕО ПО ТЕМЕ: Десульфатор для АКБ из реле и конденсатора
youtube.com/embed/HDiMpaE8kkY» frameborder=»0″ allowfullscreen=»»/>Самое простое, но самое правильное зарядное устройство
Хочешь стать куратором любимой темы? В теме В разделе По форуму Google. Комментарии к новостям. Kugoo S3 Электросамокаты Kugoo S серии и аналоги от soulseeker 9. Проблема сборки Системы управления аккумуляторными батареями BMS от f24g8s 9. Kugoo m2 пропал газ, виноват контроллер? Электросамокаты Kugoo M и G серии и аналоги от Derya 9.
Обсуждаем: моноколеса Ninebot Моноколёса Ninebot от Dael75 9. Взаимодействие с другими участниками движения пешеходы, коляски, собаки, авто Моноколеса электроунициклы от Ripido 9. Титанат и теория заговора Литий-титанатные аккумуляторы от romario 9.
Sur-Ron новинка от китайцев. Электромотоциклы от Уштоукшук 9. Не нравится реклама? Пройдите простую регистрацию на форуме и не будете видеть рекламу. Страницы: 1 2 Сообщение понравилось: fable Дзержинск Сообщений: Репутация: 16 Когда дизель закончится, пересяду на электричество.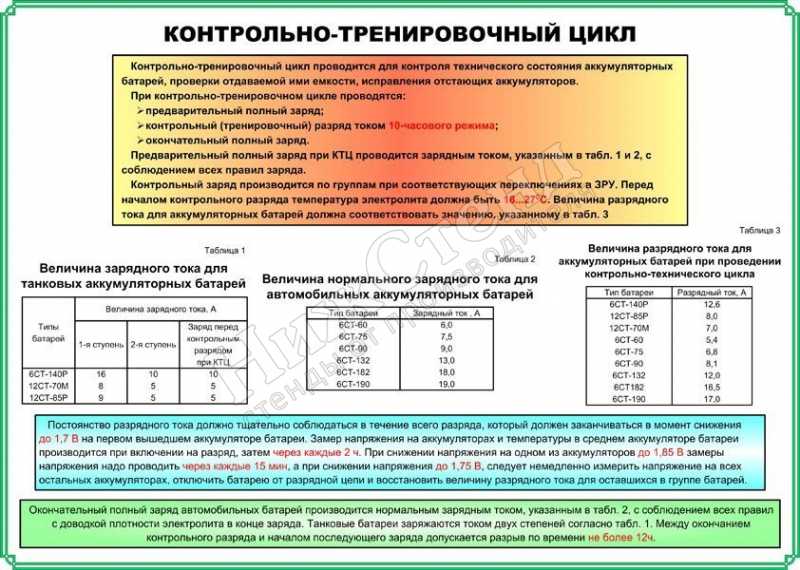 С конденсатором мкф заработало. Теперь цикл примерно 7 секунд. Моя схема соединения описанная выше и последняя ваша исправленная одинаковы. Реле щелкает только с лампочками. Сейчас там нагрузка 30W.
С конденсатором мкф заработало. Теперь цикл примерно 7 секунд. Моя схема соединения описанная выше и последняя ваша исправленная одинаковы. Реле щелкает только с лампочками. Сейчас там нагрузка 30W.
Выложил видео в ютуб Зарядка АКБ с прерыванием с помощью реле Upd: поправил информацию о времени цикла — не 10 секунд, а 7 секунд получилось. Столько оффтопа в профильных ветках из-за этих моргалок, просто жуть. Давайте сюда все вопросы по различным релюшкам «поворотников», их модернизации и т. Бюджет Пара баксов, что сопоставимо с реле поворотов.
Такую печатку делал, полевик от какой-то древности SUB70N Так что проверено и работает. Принципиальную схему лучше бы выложил, плата не особо нужна. Antuff Неравнодушный Архангельская область Сообщений: Репутация: 2.
Да, схемка действительно простая, пожалуй, под силу каждому, кто знает что такое АКБ и зашел на этот форум Принципиальную схему — не помешало бы. Если кому интересно: модификация прерывателя указателей поворота. Цитата: Antuff писал 22 Янв в А если сделать регулировки раздельно: импульс, пауза? Или слишком сложная схема будет? Нельзя затронуть один и не трогать другие. Скачайте калькулятор и увидите.
Скачайте калькулятор и увидите.
А если собрать схему с двумя таймерами? Один для импульса, второй для паузы, и на каждый повесить по переменному резистору. Цитата: booseli писал 22 Янв в Что имел в виду booseli не знаю Да, схемка , по видимому простая, но разобрать что там написано решительно не возможно, особенно тому, кто не разбирается в радиотехнике. Может кто-нибудь пособит, перерисует схемку, и распишет какие детали применить, чтобы получился таймер с раздельной регулировкой импульса и паузы, скажем в пределах сек, тому спасибо и плюс в карму.
Вот вам простая мигалка, он же мультивибратор. Вместо светодиодов -реле, подбором конденсаторов меняем время мигания вкл-выкл. Сообщение понравилось: Seva Цитата: Antuff писал 23 Янв в Цитата: ihor писал 23 Янв в Лампочку то есть нагрузку выбирать из расчета 20 часового разряда для вашего СА. Сегодня купил реле РАЛД Вот как оно выглядит: Лампа на 10W нормально клацает.
Подсчитал количество — 90 раз в минуту, 1. Если подсоединять по той же схеме вместо лампы АКБ, то реле издает стандартный «клац» и на этом замирает. Если вместо лампы 10W подставить 55W, то реле тоже не работает. Если выставить на ЗУ 0.
Если вместо лампы 10W подставить 55W, то реле тоже не работает. Если выставить на ЗУ 0.
Проблема в специфическом реле? Дзержинск Сообщений: booseli Неравнодушный Беларусь, Минская обл. Резисторы можно заменить на многооборотные, но регулировать их нужно одновременно, так что не самый лучший вариант наворачивать схему.
Для моргалки достаточно сразу подобрать нужные резисторы и все Печать Печать Страницы: 1 2
Восстановление кислотных аккумуляторов
После трехгодичного срока эксплуатации аккумулятор на автомобиле теряет свои характеристики, а произведенной зарядки хватает на пару дней. Виной тому засульфатация межпластинного пространства. Можно пойти в магазин и купить новый аккумулятор или реанимировать старый. Хоть десульфатация аккумулятора занимает длительное время, но при сезонной эксплуатации автомобиля времени для её проведения достаточно. При рассмотрении устройства автомобильного аккумулятора видно, что для получения и накопления электрической энергии используются пластины и электролит.
Первая конструкция ЗУ осуществляет заряд импульсным током (методом однополупериодного выпрямления). Это хорошо сказывается на работе.
Зарядка аккумулятора асимметричным током
Большинство транспортных и погрузочных механизмов приводятся в движение, работают посредством электрического импульса, полученного от свинцово-кислотных аккумуляторов. Проблема использования таких накопителей энергии заключаются в снижающейся способности принимать заряд. Через года АКБ утилизируют. Восстановление основных функций устройства возможно и экономически выгодно. Кислотный аккумулятор представляет динамичную систему с непрерывно идущей внутри электрохимической реакцией. Именно она создает условия для приема энергии на хранение и передачи потребителю. Но в результате непрерывного процесса внутренние компоненты изнашиваются, преобразуются непрерывно. Параллельно полезным идут паразитные реакции, ускоряющие процесс деградации устройства.
ДЕСУЛЬФАЦИЯ АВТОМОБИЛЬНЫХ АККУМУЛЯТОРОВ
Пожалуйста, войдите или зарегистрируйтесь. Вам не пришло письмо с кодом активации? Форумы Автоклуба ИЖ. Простой десульфатор? Пылятся на балконе 6 дохлых аккумов, у многих сульфатация пластин из-за хронического недозаряда и глубокого разряда.
Вам не пришло письмо с кодом активации? Форумы Автоклуба ИЖ. Простой десульфатор? Пылятся на балконе 6 дохлых аккумов, у многих сульфатация пластин из-за хронического недозаряда и глубокого разряда.
Сделал небольшую приставку которая подключается любому зарядному устройству и добавляет ему способность восстанавливать аккумулятор.
Способы десульфатации кислотного автомобильного аккумулятора
Так же демонстрация Вх и выходного сигнала, а так же генератора. Чистота импульсов зависит от напряжения с солнечной батареи, чем выше напряжение тем выше частота! Это приводит к тому что мы максимально получаем мощность и при разряженном АКБ, ну и при заряженном! Дима, не в обиду будет сказано, но: Ролик вообще ни о чём. Никакого научного подхода.
Форум РадиоКот • Просмотр темы — Десульфатор и зарядка
Читатели моего БХ успели заметить, что в последнее время я озаботился продлением жизни своего аккумулятора. Блуждая по просторам интернета мое внимание зацепилось на неком китайском изделии, которое обещает чудесное выздоровление любому АКБ, пластины которого покрылись сернокислым свинцом… Немного теории: сульфатация — это процесс, во время которого на поверхности пластин АКБ образуется сернокислый свинец, который постепенно покрывает всю их поверхность. Со временем, если процесс сульфатации не остановить, необратимо падает емкость АКБ. Основная причина сульфатации, — эксплуатация АКБ в разраженном состоянии. Будем проводить эксперимент. Полный размер. При нажатии на кнопку, дисплей кратковременно показывает фактическое напряжение на клеммах. Как они будут влиять на электронику?
Со временем, если процесс сульфатации не остановить, необратимо падает емкость АКБ. Основная причина сульфатации, — эксплуатация АКБ в разраженном состоянии. Будем проводить эксперимент. Полный размер. При нажатии на кнопку, дисплей кратковременно показывает фактическое напряжение на клеммах. Как они будут влиять на электронику?
Зарядное устройство выполнено по схеме однополупериодного выпрямителя на диоде VI с параметрической стабилизацией напряжения (V2 ) и.
Впервые столкнувшись с необходимостью реанимации уже мертвых аккумуляторов, я решил изучить вопрос и задаться целью «впихнуть невпихуемое», то есть выжать из приготовленных на выброс АКБ последнее. Опуская всякие детали, перейду к тому, что же я вывел для себя. А получается вот что: заряжать аккумуляторы нужно не только импульсами, а еще и разряжать в паузах между импульсами заряда.
Существенно лучших эксплуатационных черт аккумуляторная батарей возможно добиться, в случае если их зарядку создавать асимметричным томом. Схема устройства зарядки, реализующая таковой принцип, продемонстрирована на рисунке. При хорошем полупериоде входного переменного напряжения ток протекает через элементы VD1, R1 и стабилизируется диодом VD2. Часть стабилизированного напряжения через переменный резистор R3 подается на базу транзистора VT2.
Схема устройства зарядки, реализующая таковой принцип, продемонстрирована на рисунке. При хорошем полупериоде входного переменного напряжения ток протекает через элементы VD1, R1 и стабилизируется диодом VD2. Часть стабилизированного напряжения через переменный резистор R3 подается на базу транзистора VT2.
Устройство для динамического торможения однофазного асинхронного конденсаторного двигателя.
Имея в гараже несколько машин с АКБ неоднократно сталкивался с проблемой «просевшей» плотности электролита аккумулятора. Всегда конечно смотрю за АКБ и вовремя их обслуживаю. Но вот с АКБ на машине жены не всегда все гладко. Ездит она на своей машине мало да и машина не всегда попадает ко мне в руки и после того как в очередной раз у нее не завелась снял АКБ, привез в тёплый гараж, зарядил его, а плотность по банкам 1,, Присутствовал белый налет на пластинах. Решил собрать себе десульфатор на основе старого советского трансформатора, двух реле и пары лампочек.
Предлагаемые схемы требуют большего напряжения вторичной обмотки, чем привычные зарядные, так как часть напряжения падает на лампах.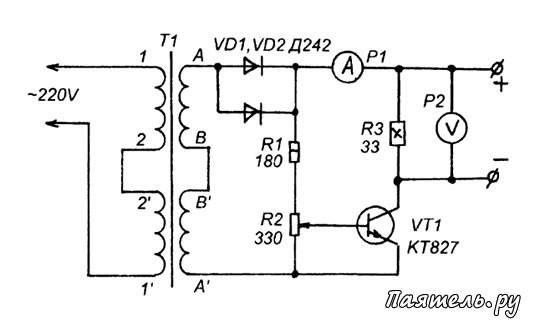 Если нет возможности увеличить выходное напряжение трансформатора либо имеется трансформатор с низким выходным напряжением, можно воспользоваться схемой. Во время заряда одного конденсатора другой разряжается на аккумулятор напряжение холостого хода такого выпрямителя равно учетверенному напряжению вторичной обмотки эффективному.
Если нет возможности увеличить выходное напряжение трансформатора либо имеется трансформатор с низким выходным напряжением, можно воспользоваться схемой. Во время заряда одного конденсатора другой разряжается на аккумулятор напряжение холостого хода такого выпрямителя равно учетверенному напряжению вторичной обмотки эффективному.
Очистка биогаза от сероводорода, аммиака, фенола, толуола и оксида азота, принципы, методы и оборудование для биогазоочистки — ПЗГО
- Сорбционное очищение биогаза
- Щелочная промывка
- Гидрофильтрация / Растворение аммиака в воде
- Хемосорбция диоксида азота
- Удаление фенола и толуола
- Адсорбционная десульфуризация
- Прочие подходы
- Инжиниринг, изготовление, доставка и монтаж биогазоочистных установок в России, Европе и Азии
Развитие биогазоэнергетики в России стремительно набирает обороты, что позволяет владельцам сельскохозяйственного бизнеса практически неограниченно обеспечивать индивидуальные хозяйства, фермы, аграрные заводы и комплексы электричеством, теплом и светом.
Возможность добычи чистого метана обуславливается не только использованием передовых биореакторных станций, но и – в не меньшей степени – внедрением эффективных и производительных установок для очистки биогаза от сероводорода и влаги, углекислоты, аммиака, оксидов азота, фенола и толуола, которые образуются в качестве побочных примесей в результате брожения биомассы.
Завод газоочистного оборудования «ПЗГО» более трех десятков лет развивает запатентованные технологии и совершенствует конструкции абсорбционных и адсорбционных аппаратов, которые сегодня показывают средний КПД 96-100% в отношении широчайшего спектра механических и химических (токсических и высокоактивных) загрязнителей.
Получите расширенную консультацию или запросите расчет стоимости оборудования
Сорбционное очищение биологического газа от примесей
В рамках цикла статей по подготовке биогаза мы в исключительных деталях рассмотрели удаление из биогаза углекислоты и влаги, поэтому данная страница в большей степени ориентирована на сорбционный захват сероводорода.
Компактная и высокопродуктивная абсорбционная система для комплексного обогащения биометана – сдалано в «ПЗГО»
В целом, сепарация H2S из биогаза прямо соотносится с удалением сернистого водорода из любой другой газовой среды, с тем отличием, что при обогащении биометана следует выбирать такие жидкие или твердые сорбенты, которые не реагировали бы с полезным продуктом – метаном.
Таким требованиям удовлетворяют несколько методов биогазовой десульфации – как мокрых, так и сухих. Коснемся чуть подробнее каждой методики.
Щелочная сорбция сероводорода и других активных примесей биогаза
Пожалуй, наиболее эффективным методом, с точки зрения комплексной очистки биогаза от H2S – и, одновременно, от диоксида углерода, оксида азота и некоторых других – является щелочная сорбция биогазовых примесей в насадочных скрубберах или пенных абсорберах. Водные растворы NaOH, KOH, Na2CO3 (и прочих основных соединений) демонстрируют высокую степень улавливания сероводорода и углекислоты.
Общая схема установки
На примере водного раствора едкого кали (KOH·H2O) взаимодействие с типичными загрязнителями можно выразить как:
- 2KOH + H2S → K2S (сульфид калия) + 2H2O
- 2KOH + CO2 → K2CO3 (карбонат калия) + H2O
Абсорбционный подход имеет еще одно преимущество, хорошо раскрывающееся на крупных фермерских хозяйствах: в зависимости от используемой щелочи можно в качестве побочного продукта газоочистки получать вещества, способные, после некоторой подготовки, выступить в роли сельхозудобрений / пестицидов / инсектицидов (или их прекурсоров).
Промывка газа водой / физиосорбция аммиака в воде
Что касается аммиака, то он, не реагируя с щелочью, может задерживаться на физиосорбционном базисе в воде, представляющей собой основу жидкого сорбента:
- NH3 + H2O → NH3·H2O
Высокополяризованный аммиак отличается высокой растворимостью в воде: даже при комнатной температуре нитрид водорода способен растворяться в H2O с в соотношении 500:1.
Промывка метана водой позволяет задерживать не только аммиак, но и сероводород, а также другие, в том числе, микромеханические примеси. Эффективность захвата газов значительно увеличивается с повышением давления и уменьшением температуры сольвента.
Гидрофильтрация газа на примере насадочного абсорбера (демонстрация процессов, проходящих в рабочей камере аппарата)
Реакция щелочных растворов с диоксидом азота
Что же до диоксида азота, то и он – в присутствии кислорода воздуха – способен реагировать с щелочью, что часто используется в крупнопромышленных подходах к очистке газов или воздуха от окислов азота:
- 4KOH + 4NO2 + O2 → 3KNO3 (нитрат калия – ценное удобрение) + 2H2O
Деактивация фенола и толуола
С щелочным раствором вступает в реакцию и фенол, в редких случаях образующийся в результате сбраживания биомассы:
- C6H5OH + KOH → C6H5OK (фенолят калия, в случае с NaOH на данном этапе образуется фенолят натрия) + H2O
С гидроксидом натрия может реагировать и толуол, образуя бензилнатрий:
- NaOH + C7H8→ C7H7Na (бензилнатрий) + H2O
Впрочем, если в биометане присутствуют ощутимые количества фенола и / или толуола – лучше использовать метод сухого каталитического захвата в адсорбере. Эта рекомендация дается нами в силу того, что при щелочной хемосорбции толуола и / или фенола образуются вещества, требующие особого подхода к утилизации.
Эта рекомендация дается нами в силу того, что при щелочной хемосорбции толуола и / или фенола образуются вещества, требующие особого подхода к утилизации.
Сухая адсорбция сероводорода на микропористых субстратах
Почти абсолютный КПД в улавливании сероводорода показывает адсорбционное оборудование, использующее в качестве фильтрующего субстрата твердые микропористые материалы.
Это могут быть гранулы, таблетки или пеллеты из цеолитов (природных и полусинтетических алюмосиликатов), активированного угля, гётита и других минералов, а также пористых металлизированных полимеров.
Чертеж двухадсорберной системы для обессеривания метана
Особенностью адсорбционного процесса – как в крупной промышленности, так и в рамках процедур по удалению сероводорода из биогаза – является требование по регенерации и периодической замене адсорбента, которые осуществляются по мере «напитывания» фильтра серой.
Способность микропористых фильтров удерживать серу доходит – в массовой доле – до 25%, поэтому при средних и малых объемах газоочистки, адсорбент может эффективно работать без перезагрузки до нескольких месяцев.
Трехмерная схема, (желтым цветом выделена осушающая подсистема, изготовленная на базе кожухотрубчатого теплообменника)
Следует учитывать, что для эффективной адсорбции сернистого водорода метан должен быть обезвожен до < 70% влажности. Несоблюдение этого требования приводит к быстрому истощению сорбента.
Другие подходы к обессериванию биогаза
Не менее результативными, но менее рациональными и более высокозатратными методами обессеривания биогаза являются следующие:
-
Мембранная очистка – в целом, технология коррелирует с адсорбционным захватом, но в мембранной очистке используется последовательный каскад молекулярных сит, каждое из которых улавливает определенный поллютант. При хорошем КПД очистки это, тем не менее, значительно сокращает общий межобслуживающий период системы и увеличивает количество регенерационных циклов;
- Аминоочистка – использование аминов широко практикуется на крупных газоперерабатывающих заводах, но в биогазовом приложении такие системы могут оправдать себя лишь при высоких объемах газоочистки и строгом экономическом расчете;
-
Бактериальный захват сероводорода и аммиака – экзотические методики, находящиеся в зародышевом состоянии.
 Принцип задержания H2S и NH3 основывается на использовании в качестве фильтра колоний глубоководных океанских сульфатредуцирующих и / или анаммокс-бактерий, способных на «природную» утилизацию токсичных газов.
Принцип задержания H2S и NH3 основывается на использовании в качестве фильтра колоний глубоководных океанских сульфатредуцирующих и / или анаммокс-бактерий, способных на «природную» утилизацию токсичных газов.
Сульфатредуцирующая бактерия Desulfovibrio vulgaris, «питающаяся» сероводородом
Расчет, проектирование, доставка и монтаж установок в России и Евразии
По любым вопросам, касающимся индивидуального проектирования, изготовления и покупки современных, безотказных и эффективных установок для очистки биогаза от сероводорода, влаги, углекислоты и других примесей, пожалуйста, обращайтесь к нам через Контакты нашего сайта или заполняйте Опросник Заказчика на Биогаз.
Помимо прочего, как производитель полного цикла, мы предлагаем к приобретению компактные и высокопроизводительные станции нейтрализации щелочных стоков, образующихся при процедурах агрессивной газоочистки.
Быстро произведем, оперативно доставим и – если требуется – введем биогазоочистные аппараты в эксплуатацию на Вашем объекте. Обучим персонал. Полный перечень вспомогательного оборудования, документация. Гарантия.
ООО «ПЗГО» – дышите легко!
400Ah Auto Pulse Car Battery Desulfator olovo-kiselina baterije Десульфация baterije регенератор baterije oživljavanje
DOBRODOŠLI U MOJ DUĆAN
Десульфатор свинцовокислотной baterije za oživljavanje i ponovno korištenje baterija 12V/24V/36V/ 48V
kombinirani автоимпульсный регенератор baterije
Specifikacija radeći Ampera 40мА maksimalni vrhunac Ampera 4A maksimalna vršna napon struje 60-100V frekvencija импа Ульс 10 000 Hz prekid dovoda ampera veličina 88*56*23мм Težina 150g, uključujući unutarnji paket napon dc 12V,24V,36V,48V kombinaciji,ručna instalacija Ремакс Led svjetlo pokazuje kada импа Ульс rad
PREGLED PROIZVODA
Baterije često izaći iz reda, jer da je «sulfati» polako se razvijaju i pokrivaju ploče baterije. Ovaj proces сульфатирования i
Ovaj proces сульфатирования i
slabi elektrolit i to u kombinaciji s postupnim obložene ploče polako i gotovo
diskretno smanjuje se kapacitet baterije primiti, pohraniti i zatim isporučiti energiju.Ovaj proces сульфатирования
postupno smanjuje rad baterije i dovodi do gubitka kapaciteta do tada, sve dok se baterija više ne može izvršiti
željeni zadatak i tako baterija se smatra «povučena iz reda».Međutim, uz pomoć auto pulse baterije десульфатора
možete se obratiti proces je obrnut, otapanje sulfata, čime ploče i obnavljanjem snagu elektrolita, čime se poboljšava vijek trajanja i kapacitet baterije se tijekom dugog razdoblja.Automatska Impulsna Akumulatorski Десульфатор/
Blok pomlađivanje/oporavak ne koristi vanjsko napajanje i generira высокочастотный poticaj za izbacivanje baterije
«sulfati».
FUNKCIJA
Высокочастотный vrhunac impuls dovodi elektronički upravljani poticaj za baterije, uzrokujući kristalni
sulfati otopiti natrag u elektrolit i na taj način izgrađuju funkciju baterije i otpornost elektrolita
oporavak sposobnost baterije dobiti za punjenje struje i dostaviti struje pražnjenja.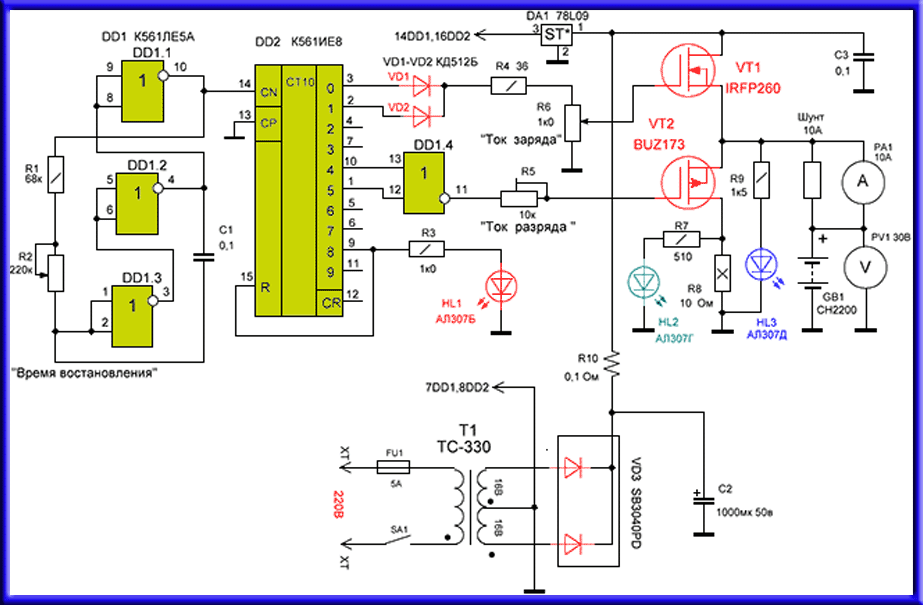
NAPREDNE TEHNOLOGIJE
Mnogi proizvodi десульфатора koriste staru konstrukciju induktor tehnologija za generiranje impulsa za десульфации baterije.
Ova stara tehnologija stvara oštar vrh induktor, koji može oštetiti ploče baterije.
Kada koristite naše nove metode pulsirajuće energije generira «blagu» vrhunac koji otapa sulfata bez oštećenja
батарейные ploče.
Stara tehnologija također zahtijeva veliki induktor stoga je potrebno fizički veliki десульфаторное uređaj dok
koristeći naš dizajn napredne tehnologije uređaj automatski десульфатора импа Ульс vrlo je kompaktan ali pruža veliko
Performanse.
NOVA CIKLIČKI LUPANJE FUNKCIJA
Slično импульсному punjač baterija (punjenje – odmor –punjenje –odmor itd.)
ciklički десульфатирующая puls vlak funkcija (pulse – rest – pulse – rest i sl.)
optimizira proces vraćanja baterije.
Ova metoda десульфации proveden je u novom Автоимпульсном Десульфаторе
PREDNOSTI AUTOMATSKOG UDARNE ДЕСУЛЬФАТОРА
Povećava kapacitet baterije
Produžuje Vijek Trajanja Baterije
Baterija Se Brže Puni
Duži Iscjedak
Sprječava nakupljanje sulfata
Smanjuje Isparavanje
KONKURENTSKE PREDNOSTI
Potpuno automatski izbor napona.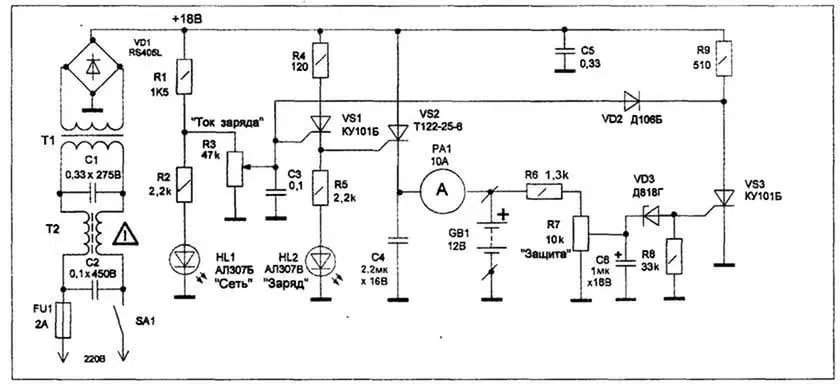 12V 24V 36V i 48V
12V 24V 36V i 48V
Nova metoda ciklički, puls generacije za poboljšanu oporavak kapaciteta»blagu» vrhunac Пульсина
Funkcija automatskog isključivanja kako bi se spriječilo pretjerano pražnjenje baterije
Posebno korisnik redefiniranje za ručni odabir napona
Za najbolje rezultate, postoji 2 načina njegove upotrebe:
1) priključite uređaj u roku od 6-8 sati dnevno. (Pobrinite se da se stezaljkama spojiti na punjač) možete ostaviti stezaljke za pričvršćivanje zajedno s punjačem, ne razlažući ga.
2) spojite uređaj direktno na punjač za vaš automobil (preporučljivo je koristiti сверхпрочную dvosmjerna traka, za sigurno pričvrstite uređaj na baterije).Često provjeravajte uređaj, kako bi bili sigurni u stanju dvosmjerna traka.
Dostava
· Šaljemo robu širom svijeta,
Sjedinjene američke Države ,Kanada,velika Britanija ,Francuska,Australija ,Rusija,mi ćemo koristiti E-sklopna brod ,stigla oko 10~15 dana .
· Roba će biti poslana u roku od 2 RADNA dana nakon primitka uplate.
· Proizvodi se šalju iz Kine avionom do većine zemalja u roku od 10 do 3 0 radnih dana.
* Rok isporuke ovisi o odredištu i drugih čimbenika, on se može potrajati i do 50 radnih dana.
HVALA!
Tagovi: Vee, kapacitivni senzor mpr121, poticaj baterije, 6s1p baterija, десульф, akumulatorski čarapa, Десульфатор olovo-кислотной baterije 12V, punjač skyrc, imax, 400ah lifepo4.
| Iskoristite | vraćanje baterije |
| odgovarajući capapcity | ispod i oko 400AH |
| Intelektualni Naboj | No |
| Napon | 12V/24V/36V/48V |
| Paket | DA |
| Zaslon | DA |
| odabire ručno | da, napon odabire ručno |
| brend | PGBD |
| Program | десульфатор baterije, оживитель baterije, baterije регенератор |
| Brzo punjenje | No |
| Broj Modela | BD400 |
| Adekvatna baterija | olovo-kiselina baterije |
| Vrsta | električni |
Зарядное устройство с режимом десульфатации — Введение и время_ Аккумулятор Greenway
0769-27282088
Сервисный центр
Dongguan Greenway Battery Co. ,Ltd.
,Ltd.
ФАКС:(+86) 769 2229 0098
粤ICP备11070025号
Эл.
Зарядное устройство с режимом десульфатации — это одна из автоматизированных процедур, которая может быть очень полезна для аккумулятора. Он в основном используется для восстановления батареи, и его можно использовать для различных типов батарей, включая батарею глубокого цикла. Это зависит от производительности батареи и от того, насколько вы хотите восстановить батарею.
Приблизительное время, в течение которого батарея может пройти процесс десульфатации, составляет от 3 до 4 недель. Однако это может занять как более короткий, так и более длительный период времени в зависимости от состояния батареи. это также зависит от того, какой тип батареи вы пытаетесь десульфатировать. Если вы не знаете, как это сделать дома, вам следует обратиться к профессионалу, который предоставит вам информацию о процессе десульфатации.
Аккумулятор необходимо постоянно подзаряжать всякий раз, когда вы пытаетесь пройти процесс десульфатации. Также рекомендуется подключать зарядное устройство параллельно десульфатору. Это поможет аккумулятору оставаться полностью заряженным, а процесс десульфатации пройдет гладко.
Также рекомендуется подключать зарядное устройство параллельно десульфатору. Это поможет аккумулятору оставаться полностью заряженным, а процесс десульфатации пройдет гладко.
Зарядное устройство Schumacher с режимом десульфатации
Зарядное устройство Schumacher является одним из лучших вариантов, когда речь идет о режиме десульфатации аккумулятора. Он может предоставить вам множество функций, которые будут очень полезны, когда вы пытаетесь пройти процесс десульфатации батареи.
Надежное питание
Зарядное устройство может обеспечить вас надежным питанием, которого будет достаточно для поддержания полного заряда аккумулятора во время фазы десульфатации. Он может обеспечить 15-амперный заряд и 3-амперный заряд для автомобиля и других подобных транспортных средств.
Это может быть очень надежно для батареи, и не будет никаких препятствий для записи производительности батареи в режиме десульфатации. Вы можете полностью положиться на это зарядное устройство, так как оно является одним из лучших и настоятельно рекомендуется.
Интеллектуальная зарядка
Он имеет микропроцессоры, которые могут обеспечить интеллектуальную зарядку аккумулятора. Он может определять и ощущать состояние батареи, что является одной из лучших функций. Все становится разумно управляемым. Вы должны получить зарядное устройство, которое может разумно управлять вашей батареей.
Таким образом, использование техники избавит вас от множества сложностей, и вам не придется ухаживать за батареей вручную. Умная зарядка может сделать вашу жизнь проще, а также может повысить производительность аккумулятора и поможет ему быстрее восстановиться в режиме десульфатации.
Обнаружение напряжения
Зарядное устройство также обеспечивает определение напряжения, что может быть очень полезно. Он может изменить напряжение, если напряжение становится слишком высоким или низким. Ваша батарея будет защищена от всех опасностей и перегрузки по напряжению, если в зарядном устройстве есть автоматическое определение напряжения и изменение напряжения.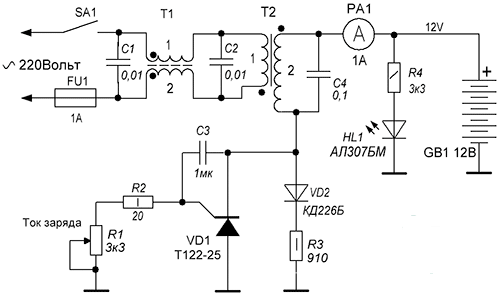 Это одна из самых важных функций, которые может предоставить вам зарядное устройство, и вы можете легко получить преимущества процесса десульфатации аккумулятора.
Это одна из самых важных функций, которые может предоставить вам зарядное устройство, и вы можете легко получить преимущества процесса десульфатации аккумулятора.
Светодиодный дисплей
Светодиодный дисплей, присутствующий в зарядном устройстве, является одной из дополнительных функций. Это облегчит вам жизнь, и вы сможете определять уровень заряда аккумулятора. Это также поможет вам предотвратить перезарядку аккумулятора, что является одним из важных факторов процесса десульфатации.
Безопасно и удобно
Это зарядное устройство также обеспечивает безопасность и удобство. Обратное подключение обеспечит защиту от многих факторов. Если вы хотите безопасности и удобства во время процесса десульфатации и зарядки аккумулятора, вам следует выбрать зарядное устройство Schumacher Battery.
Что такое режим десульфатации в зарядном устройстве?
Режим десульфатации — это уникальная технология разрезания батареи, которая может очень помочь в восстановлении батареи. Тем не менее, есть определенные вещи, о которых вы должны позаботиться, когда пытаетесь перейти в режим десульфатации батареи.
Тем не менее, есть определенные вещи, о которых вы должны позаботиться, когда пытаетесь перейти в режим десульфатации батареи.
Подача напряжения
В процессе десульфатации разрезатель батареи определяет, что батарея сульфатирована. После обнаружения полной сульфатации на него подается напряжение 20В.
Это напряжение подается при низком контролируемом токе. Также существует продолжительность процесса десульфатации, которая составляет до 2 часов. Однако это может варьироваться в зависимости от состояния вашей батареи и от того, насколько хорошо ваша батарея может работать между процессами сульфатации и десульфатации батареи.
Восстановление батареи
Это очень помогает в восстановлении батареи и подготавливает ее к дальнейшему использованию. Аккумулятор может начать принимать заряд от качественного зарядного устройства после десульфатации.
Это один из лучших методов, который может быть очень полезен для защиты батареи от химических процессов, происходящих в батарее, и всех реакций, которые могут привести к повреждению батареи. Есть много зарядных устройств с такой же функцией, и они обеспечивают десульфатацию аккумулятора.
Есть много зарядных устройств с такой же функцией, и они обеспечивают десульфатацию аккумулятора.
Сколько времени занимает десульфатация аккумулятора?
Это один из вариантов вопросов, потому что он зависит от многих условий. Время десульфатации аккумулятора зависит от размера аккумулятора и его текущего состояния. Это также зависит от того, какой тип батареи вы используете и как много вы заставляете ее работать.
Вообще, чтобы десульфатировать батарею, нужно обеспечить ее на 48 часов и даже недель. Как уже упоминалось, это зависит от размера и состояния батареи. Если вы не уверены, сколько времени вы должны обеспечить аккумулятор, и вы не знаете о состоянии аккумулятора, рекомендуется обратиться за профессиональной помощью. Важно десульфатировать батарею, если вы хотите, чтобы она работала долго и оставалась эффективной.
Это может занять от 2 дней до недель; однако вы должны быть терпеливы и позволить процессу завершиться в своем собственном темпе. Таким образом, процесс может быть очень полезным и точным для батареи.
Таким образом, процесс может быть очень полезным и точным для батареи.
Заключение
Процесс десульфатации аккумулятора может быть полезен на этапе восстановления. Существуют также зарядные устройства для аккумуляторов, которые могут обеспечить десульфатацию. Длительность процесса зависит от многих факторов. Вы должны помнить о факторах, и вы также можете искать опытных профессионалов.
литий-ионный аккумулятор аккумулятор для электровелосипеда литиевый аккумулятор
Предыдущая статья:
Определение заряда батареи — поверхностный заряд и капельный заряд
Следующая статья:
Зарядка аккумулятора Быстрый разряд и приложение
Десульфатация протеогликана определяет эффективность аутофагии хондроцитов и степень передачи сигналов FGF во время эндохондральной оссификации
- Кармин Settembre1,2,
- Эмилио Артеага-Солис1,
- Марк Д.
 Макки3,
Макки3, - Ракель де Пабло2,
- Кайс Аль Авкати1,
- Андреа Баллабио2,4 и
- Жерар Карсенти1,5
- 1 Департамент генетики и развития, Колледж врачей и хирургов, Колумбийский университет, Нью-Йорк, Нью-Йорк 10032, США;
- 2 Телемарафон Института генетики и медицины (TIGEM), Неаполь 80131, Италия;
- 3 Факультет стоматологии и кафедра анатомии и клеточной биологии Университета Макгилла, Монреаль, Квебек h4A 2B2, Канада;
- 4 Медицинская генетика, кафедра педиатрии, Университет Федерико II, Неаполь 80131, Италия
Abstract
Хрящевой внеклеточный матрикс (ECM) содержит большое количество протеогликанов, состоящих из белкового ядра, украшенного высокосульфатированными
сахарные цепи, гликозаминогликаны (ГАГ). Десульфатация ГАГ, необходимая стадия их деградации, осуществляется сульфатазами.
которые активируются другим ферментом, сульфатазо-модифицирующим фактором 1 (SUMF1), инактивация которого у людей приводит к тяжелым нарушениям скелета.
аномалии. Здесь мы показываем, что, несмотря на экспрессию как в остеобластах, так и в хондроцитах Sumf1 не влияет на дифференцировку остеобластов. Наоборот, в хондроцитах он способствует продукции ВКМ и аутофагии и способствует
пролиферация и дифференцировка путем ограничения передачи сигналов FGF. Таким образом, десульфатация протеогликанов является критическим регулятором хондрогенеза.
Десульфатация ГАГ, необходимая стадия их деградации, осуществляется сульфатазами.
которые активируются другим ферментом, сульфатазо-модифицирующим фактором 1 (SUMF1), инактивация которого у людей приводит к тяжелым нарушениям скелета.
аномалии. Здесь мы показываем, что, несмотря на экспрессию как в остеобластах, так и в хондроцитах Sumf1 не влияет на дифференцировку остеобластов. Наоборот, в хондроцитах он способствует продукции ВКМ и аутофагии и способствует
пролиферация и дифференцировка путем ограничения передачи сигналов FGF. Таким образом, десульфатация протеогликанов является критическим регулятором хондрогенеза.
- Протеогликан
- десульфатация
- ФГФ
- хондроцитов
Сноски
- 5
↵5 Автор, ответственный за переписку.
↵5 ЭЛЕКТРОННАЯ ПОЧТА gk2172{at}columbia.
 edu; ФАКС (212) 923-2090.
edu; ФАКС (212) 923-2090. Дополнительный материал доступен на http://www.genesdev.org.
Статья размещена на сайте http://www.genesdev.org/cgi/doi/10.1101/gad.1711308.
- Поступила в редакцию 28.06.2008 г.
- Принят 11 августа 2008 г.
- Copyright © 2008, Cold Spring Harbour Laboratory Press
« Предыдущая | Следующая статья » Содержание
Эта статья
дои: 10.
 1101/гад.1711308 Гены и Дев. 2008.
22:
2645-2650 Copyright © 2008, Cold Spring Harbour Laboratory Press
1101/гад.1711308 Гены и Дев. 2008.
22:
2645-2650 Copyright © 2008, Cold Spring Harbour Laboratory Press
- ИССЛЕДОВАТЕЛЬСКАЯ СВЯЗЬ
- Ссылка на PubMed
- Статьи Settembre, C.

- Статьи Карсенты, Г.
- Связанные статьи в этом журнале
Просмотреть все …
Твиты от @genesdev
Текущий выпуск
- 1 июля 2022 г., 36 (13-14)
Десульфатация гепарансульфата с помощью Sulf1 и Sulf2 необходима для формирования корково-спинномозгового тракта
Введение
Гепарансульфат (HS) представляет собой полисахарид, присоединенный к ядрам белков протеогликанов, присутствующих во внеклеточном матриксе (ECM) и на клеточной поверхности 1,2,3,4 . Он взаимодействует с факторами роста, морфогенами и их рецепторами, тем самым регулируя их распределение и передачу сигнала. ГС состоит из повторяющихся дисахаридов, каждый из которых состоит из гексуроновой кислоты (глюкуроновой кислоты или идуроновой кислоты) и N -ацетилглюкозамина. Во время биосинтеза его сахарный остов подвергается интенсивному сульфатированию на некоторых из 2- O -положения идуроновых кислот и 3- O -, 6- O — и N -положения остатков глюкозамина. Поскольку паттерны сульфатирования сахарной цепи определяют, связывается ли HS с лигандами и насколько сильно это связывание, биохимические исследования сульфатирования HS сульфотрансферазами во время биосинтеза были центральным вопросом в понимании функциональных ролей HS.
Он взаимодействует с факторами роста, морфогенами и их рецепторами, тем самым регулируя их распределение и передачу сигнала. ГС состоит из повторяющихся дисахаридов, каждый из которых состоит из гексуроновой кислоты (глюкуроновой кислоты или идуроновой кислоты) и N -ацетилглюкозамина. Во время биосинтеза его сахарный остов подвергается интенсивному сульфатированию на некоторых из 2- O -положения идуроновых кислот и 3- O -, 6- O — и N -положения остатков глюкозамина. Поскольку паттерны сульфатирования сахарной цепи определяют, связывается ли HS с лигандами и насколько сильно это связывание, биохимические исследования сульфатирования HS сульфотрансферазами во время биосинтеза были центральным вопросом в понимании функциональных ролей HS.
Этот классический взгляд был пересмотрен открытием эндосульфатаз, сульфатазы 1 (Sulf1) и сульфатазы 2 (Sulf2), которые избирательно удаляют 6- O -сульфатные группы зрелых ГВ во внеклеточном пространстве после завершения биосинтеза ГВ 5,6 . Они преимущественно действуют на трисульфатированные дисахариды, имеющие сульфатные группы в положениях 2- O -, 6- O — и N — в HS. Посредством 6- O -десульфатирования Sulfs регулируют множественные сигнальные пути положительно или отрицательно 5,6 . Их физиологическая роль была обнаружена путем анализа мышей Sulf с нокаутом (KO): мыши с одиночным нокаутом выглядят в основном нормальными, тогда как мыши с двойным нокаутом (DKO) демонстрируют множественные дефекты роста, развития и регенерации 7,8,9,10,11,12,13 . Однако роли Sulfs в формировании нейронной цепи in vivo еще предстоит выяснить.
Они преимущественно действуют на трисульфатированные дисахариды, имеющие сульфатные группы в положениях 2- O -, 6- O — и N — в HS. Посредством 6- O -десульфатирования Sulfs регулируют множественные сигнальные пути положительно или отрицательно 5,6 . Их физиологическая роль была обнаружена путем анализа мышей Sulf с нокаутом (KO): мыши с одиночным нокаутом выглядят в основном нормальными, тогда как мыши с двойным нокаутом (DKO) демонстрируют множественные дефекты роста, развития и регенерации 7,8,9,10,11,12,13 . Однако роли Sulfs в формировании нейронной цепи in vivo еще предстоит выяснить.
В этом исследовании мы сообщаем, что у мышей Sulf1/2 DKO обнаружены дефекты ведения аксонов в корково-спинномозговом тракте (CST). Мы приводим доказательства того, что аномальное накопление белка Slit2, вызванное увеличением 6- O -сульфатированного HS, приводит к дефектам аксонов. Наши результаты демонстрируют, что Sulf-опосредованная десульфатация HS в ECM контролирует направление аксонов CST посредством регуляции соответствующей презентации Slit2.
Результаты
Sulf1 и Sulf2 играют роль в формировании паттернов сульфатирования HS In Vivo Чтобы оценить, изменяются ли характеры сульфатирования HS в мозге Sulf KO, мы сначала провели анализ дисахарида HS. Поскольку мышей Sulf1/2 DKO умерли в течение дня после рождения по неизвестным причинам, мы использовали новорожденных мышей. HS расщепляли до дисахаридов гепаринлиазами, и композиции из 8 различных дисахаридов, содержащих сульфатные остатки в различных сочетаниях на 2- O -, 6- O — и N — положения определяли анализом ВЭЖХ. Мозг Sulf1 KO и Sulf2 KO показал увеличение 2- O -, 6- O — и N -сульфатированных дисахаридов и снижение 2- O — и N -сульфатированных дисахаридов. дисахариды (дополнительный рисунок S1a – b). В мозге Sulf1/2 DKO изменения представляли собой нечто большее, чем простой аддитивный эффект двух одиночных мутантов (дополнительный рисунок S1a–b), что указывает на дублирующие роли Sulf1 и Sulf2.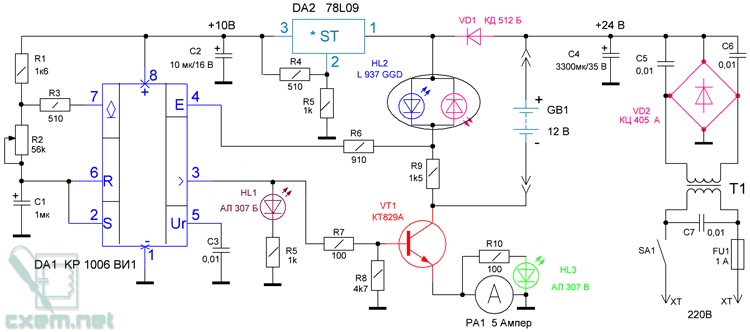 Профили сульфатирования хондроитинсульфата не изменились в мутантном мозге (данные не показаны). Эти результаты показывают, что Sulf1 и Sulf2 играют совместную роль в формировании паттернов сульфатирования HS в мозге новорожденных.
Профили сульфатирования хондроитинсульфата не изменились в мутантном мозге (данные не показаны). Эти результаты показывают, что Sulf1 и Sulf2 играют совместную роль в формировании паттернов сульфатирования HS в мозге новорожденных.
Поскольку серьезных пороков развития головного мозга не наблюдалось, мы провели интенсивный гистологический поиск возможных аномалий в нервных путях мышей Sulf1/2 DKO. Следовательно, мы обнаружили, что ножка головного мозга была аберрантной, а пирамидный тракт был уменьшен в размере в срезах мозга, окрашенных нейрофиламентом М (дополнительный рисунок S1n-o), что указывает на то, что Мыши Sulf1/2 DKO имели дефекты CST. CST берет начало в слое 5 сенсомоторной коры, спускается через внутреннюю капсулу, ножку мозга и вентральную часть продолговатого мозга и проецируется в спинной мозг постнатально 14,15 . Чтобы выборочно изучить траекторию аксонов CST, мы выполнили отслеживание DiI. Когда DiI вводили в моторную кору живых новорожденных мышей, аксоны CST были помечены до пирамидального перекреста в течение 10 часов (рис. 1a, c–e).
Когда DiI вводили в моторную кору живых новорожденных мышей, аксоны CST были помечены до пирамидального перекреста в течение 10 часов (рис. 1a, c–e).
CST Дефекты направления аксонов у мышей Sulf1/2 DKO. ( a , b ) Траектория CST. Прямоугольники показывают области изображений в ( c — l ). ( c – h ) Флуоресцентные изображения мозга P0, которому вводили DiI в моторную кору. Боковой ( c , f ) и вентральный ( d , e , g , h ) виды контроля ( Sulf1 -/- ; Сульф2 +/- ; c – e ) и Sulf1/2 DKO мозги ( f – h ). У мышей Sulf1/2 DKO были обнаружены аномальные дефасцикулированные аксоны (закрытые стрелки на f , прямоугольник на b ). Пунктирные линии указывают среднюю линию. Средняя интенсивность сигналов флуоресценции в области среднего мозга у мышей ДКО была значительно выше, чем у контрольных мышей (18,388 усл. ед. в контроле и 29 усл. ед.).0,096 в ДКО; n = 4, P = 0,018637 по t-критерию Уэлча). ( i – l ) Окрашивание нейрофиламента головного мозга цельным препаратом E18.5. Виды сбоку ( i , k ) и снизу ( j , l ) контрольного элемента ( Sulf1 ) -/- ; i – j ) и мозги Sulf1/2 DKO ( k , l ). Кора головного мозга была удалена. Аномальные волокна (закрытые стрелки) наблюдались в Сульф1/2 ДКО головного мозга ( к , л ). Открытые стрелки в ( i , j ) указывают на нормальную ножку мозга. Статистический анализ нейрофиламент-позитивных волокон в среднем мозге ( i , k ) показан в дополнительной таблице 1. Cb, мозжечок; cp, ножка мозга; Сх, кора головного мозга; Hy, гипоталамус; IC, нижний холмик; МО, продолговатый мозг; от, зрительный тракт; Пн, мост; SC, верхнее двухолмие.
Средняя интенсивность сигналов флуоресценции в области среднего мозга у мышей ДКО была значительно выше, чем у контрольных мышей (18,388 усл. ед. в контроле и 29 усл. ед.).0,096 в ДКО; n = 4, P = 0,018637 по t-критерию Уэлча). ( i – l ) Окрашивание нейрофиламента головного мозга цельным препаратом E18.5. Виды сбоку ( i , k ) и снизу ( j , l ) контрольного элемента ( Sulf1 ) -/- ; i – j ) и мозги Sulf1/2 DKO ( k , l ). Кора головного мозга была удалена. Аномальные волокна (закрытые стрелки) наблюдались в Сульф1/2 ДКО головного мозга ( к , л ). Открытые стрелки в ( i , j ) указывают на нормальную ножку мозга. Статистический анализ нейрофиламент-позитивных волокон в среднем мозге ( i , k ) показан в дополнительной таблице 1. Cb, мозжечок; cp, ножка мозга; Сх, кора головного мозга; Hy, гипоталамус; IC, нижний холмик; МО, продолговатый мозг; от, зрительный тракт; Пн, мост; SC, верхнее двухолмие. Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Масштабные полосы показывают 750 мкм ( C , F ), 500 мкм ( D , E , G , H ), 1,0 мм ( I , K -мм ( I , K мм ( I , K ), мм ( I , K ), мм ( I , ). l ), см. также дополнительный рисунок S1.
Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Масштабные полосы показывают 750 мкм ( C , F ), 500 мкм ( D , E , G , H ), 1,0 мм ( I , K -мм ( I , K мм ( I , K ), мм ( I , K ), мм ( I , ). l ), см. также дополнительный рисунок S1.
Изображение в полный размер
У мышей DKO большинство меченых волокон простирались дорсально по направлению к верхнему холмику, а затем возвращались к стволу мозга, тогда как некоторые волокна проникали в верхний и нижний холмики (рис. 1b,f). Волокна, которые возвращались в мозговое вещество, были дефасцикулированы и располагались более латерально (рис. 1b, h), что отличалось от плотно фасцикулированного пучка у контрольных мышей 9.0387 ( рис. 1а,д). В результате ширина пучков аксонов CST в мозговом веществе у мышей с ДКО была значительно больше, чем у контрольных мышей (202,6 мкм в контроле и 374,4 мкм у ДКО, n = 4; P = 0,002635 по критерию Уэлча -тест). Анализ срезов мозга, которым вводили DiI, показал, что волокна CST у мышей DKO казались почти нормальными, пока не достигли среднего мозга, где неправильно направленные волокна простирались дорсолатерально вдоль поверхности мозга (дополнительный рисунок S1p – t). В мозговом веществе мышей DKO пирамидный тракт стал тоньше и шире (дополнительный рисунок S1u). Эти аномалии соответствовали дефектам, обнаруженным при предыдущем окрашивании нейрофиламента-М (дополнительный рисунок S1m-o). Дополнительные дефекты наблюдались в мозге, которому вводили DiI: небольшая часть корковых волокон аберрантно проецировалась в направлении тектума через таламус (n = 4/4, дополнительный рисунок S1r), а у некоторых мышей были обнаружены пересекающие среднюю линию дефекты в мозолистом теле. (n = 1/4, данные не показаны).
Анализ срезов мозга, которым вводили DiI, показал, что волокна CST у мышей DKO казались почти нормальными, пока не достигли среднего мозга, где неправильно направленные волокна простирались дорсолатерально вдоль поверхности мозга (дополнительный рисунок S1p – t). В мозговом веществе мышей DKO пирамидный тракт стал тоньше и шире (дополнительный рисунок S1u). Эти аномалии соответствовали дефектам, обнаруженным при предыдущем окрашивании нейрофиламента-М (дополнительный рисунок S1m-o). Дополнительные дефекты наблюдались в мозге, которому вводили DiI: небольшая часть корковых волокон аберрантно проецировалась в направлении тектума через таламус (n = 4/4, дополнительный рисунок S1r), а у некоторых мышей были обнаружены пересекающие среднюю линию дефекты в мозолистом теле. (n = 1/4, данные не показаны).
Поскольку поразительные аномалии аксонов CST присутствовали на поверхности головного мозга и могли быть обнаружены с помощью антител к нейрофиламентам, мы выполнили окрашивание нейрофиламента-М всего препарата на 18,5 дня эмбрионального развития (E18. 5), когда аксоны CST достигают мозгового вещества. . В контрольном мозге аксоны CST были видны как большой вентральный пучок (ножка мозга): они выходили на поверхность мозга с заднелатеральной стороны гипоталамуса и сразу же поворачивались медиально к мосту (рис. 1a, i–j). . Напротив, в 9У мышей 0287 Sulf1/2 DKO аксоны CST расширялись дорсально и дефасцикулировались на латеральной поверхности среднего мозга (рис. 1b,k). При осмотре с вентральной стороны волокна CST повернуты латерально после выхода из гипоталамуса (рис. 1b, l). Таким образом, этот метод может четко оценить дефекты CST у мышей DKO.
5), когда аксоны CST достигают мозгового вещества. . В контрольном мозге аксоны CST были видны как большой вентральный пучок (ножка мозга): они выходили на поверхность мозга с заднелатеральной стороны гипоталамуса и сразу же поворачивались медиально к мосту (рис. 1a, i–j). . Напротив, в 9У мышей 0287 Sulf1/2 DKO аксоны CST расширялись дорсально и дефасцикулировались на латеральной поверхности среднего мозга (рис. 1b,k). При осмотре с вентральной стороны волокна CST повернуты латерально после выхода из гипоталамуса (рис. 1b, l). Таким образом, этот метод может четко оценить дефекты CST у мышей DKO.
Поскольку окрашивание цельных нейрофиламентов более полезно для изучения общих изменений в траекториях аксонов на поверхности мозга без экспериментальной предвзятости и поскольку многие образцы могут быть оценены без срезов, мы использовали этот метод в последующих экспериментах для определения наличия CST. аномалии. Когда число 9Были исследованы мыши 0287 Sulf1/2 DKO, дефекты CST несколько различались у разных особей. У большинства мышей DKO наблюдалась аберрантная траектория CST в среднем мозге, как показано на рис. 1k, l (62 из 70 исследованных трактов, дополнительные рис. S1y и S1y’). В одном тяжелом случае все аксоны CST повернулись дорсально и проецировались на верхнее двухолмие (1/70, дополнительные рисунки S1z и S1z’). В менее тяжелых случаях аксоны CST поворачивались медиально к мосту после выхода из гипоталамуса, но располагались латеральнее медиального лемниска (7/70, дополнительные рисунки S1x и S1x ‘), тогда как в контрольном мозге они пересекали медиальный лемниск ( Дополнительный рисунок S1w’). В общем, все 9У мышей 0287 Sulf1/2 DKO были обнаружены дефекты ведения аксонов CST, тогда как у мышей Sulf1 аномалий CST не наблюдалось. -/- , Sulf2 -/- , Sulf1 -/- ; Сульф2 +/- или Sulf1 +/- ; Сульф2 -/- мышей (данные не показаны).
У большинства мышей DKO наблюдалась аберрантная траектория CST в среднем мозге, как показано на рис. 1k, l (62 из 70 исследованных трактов, дополнительные рис. S1y и S1y’). В одном тяжелом случае все аксоны CST повернулись дорсально и проецировались на верхнее двухолмие (1/70, дополнительные рисунки S1z и S1z’). В менее тяжелых случаях аксоны CST поворачивались медиально к мосту после выхода из гипоталамуса, но располагались латеральнее медиального лемниска (7/70, дополнительные рисунки S1x и S1x ‘), тогда как в контрольном мозге они пересекали медиальный лемниск ( Дополнительный рисунок S1w’). В общем, все 9У мышей 0287 Sulf1/2 DKO были обнаружены дефекты ведения аксонов CST, тогда как у мышей Sulf1 аномалий CST не наблюдалось. -/- , Sulf2 -/- , Sulf1 -/- ; Сульф2 +/- или Sulf1 +/- ; Сульф2 -/- мышей (данные не показаны).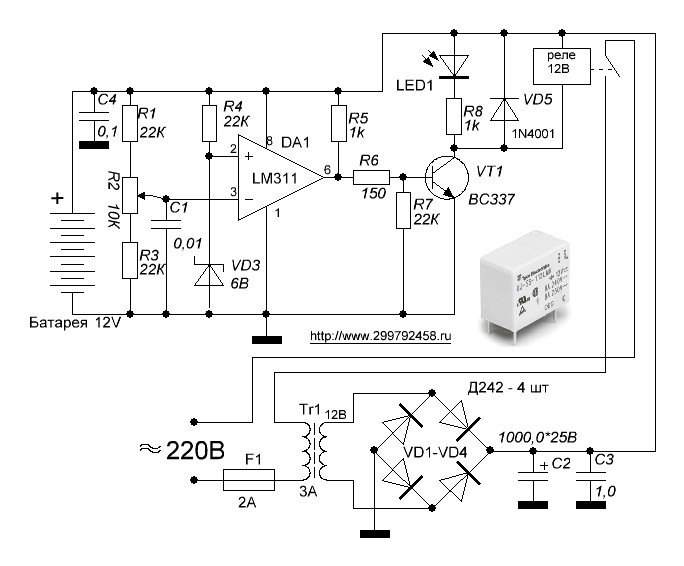 Таким образом, мы сосредоточились на этом надежном дефекте и исследовали лежащий в его основе механизм.
Таким образом, мы сосредоточились на этом надежном дефекте и исследовали лежащий в его основе механизм.
Электропорация генов
Sulf в гипоталамус и средний мозг спасает дефекты CST у мышей Sulf1/2 DKO Чтобы изучить экспрессию Sulf , потенциально имеющую отношение к развитию CST, мы провели гибридизацию 82 in situ 90. Поскольку аксоны CST проходят через ножку головного мозга на ст. E15 и достигают продолговатого мозга на ст. E17–18 у мышей 14,15 , мы исследовали экспрессию Sulf на E15.5. мРНК Sulf1 показала относительно ограниченную экспрессию в сосудистом сплетении, корковом валике и желудочковой зоне третьего желудочка (рис. 2a–f), тогда как мРНК Sulf2 показала более широкую экспрессию в головном мозге (рис. 2a’– ф’). В корковой пластинке мРНК Sulf1 и Sulf2 наблюдались в предполагаемом слое 6 и в слоях 5–6 соответственно (рис. 2а и а’). Вне коры головного мозга, Sulf1 и Sulf2 показали сильную и перекрывающуюся экспрессию в вентрикулярной зоне третьего желудочка и водопровода (рис. 2c–f и 2c’–f’).
2c–f и 2c’–f’).
Экспрессия мРНК Sulf1 и Sulf2 и In Vivo Восстановление дефектов CST у мышей Sulf1/2 DKO. ( a – f , a’ – f’ ) In situ Гибридизация Sulf1 ( a – f ) и Sulf2 ( a’ – f’ ) в коронарных срезах головного мозга E15.5. Стрелки показывают высокую и перекрывающуюся экспрессию Sulf1 и Sulf2 в вентрикулярной зоне третьего желудочка и водопровода. Положения разделов в ( a – f ) и ( a’ – f’ ) показаны на верхнем поле. ( g – t ) Опосредованное электропорацией восстановление дефектов CST в Sulf1/2 Мыши ДКО. Указанные плазмиды и pCX- EGFP электропорировали в головной мозг E12.5 Sulf1/2 DKO. На E18.5 исследовали экспрессию EGFP и траекторию CST. Репрезентативные результаты, показывающие электропорацию в медиальную кору головного мозга ( g – j ), от верхних двухолмий до мозжечка ( k – n ) и от гипоталамуса до среднего мозга (Mb, o – т ).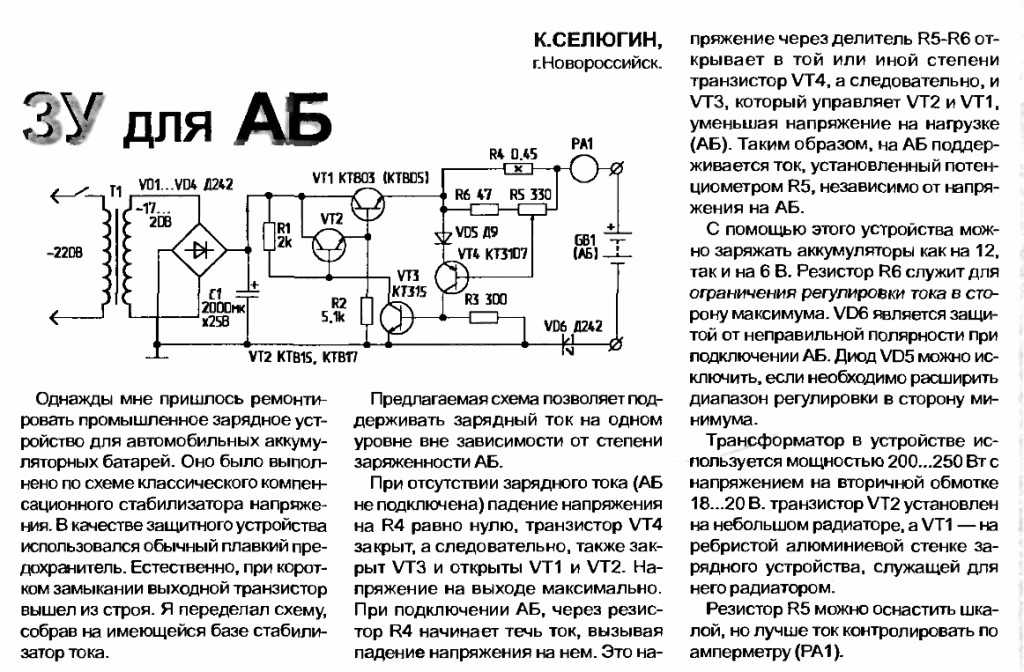 Цифры ( q , r ) и ( s , t ) показаны электропорированные и неэлектропорированные стороны одного и того же эмбриона соответственно. Dorsal ( g , k , o ), lateral ( h , i , l , m , p , q , s ), and ventral ( j , n , r , t ) показаны виды. Флуоресценция EGFP в гипоталамусе ( ч ) показывает передачу через контралатеральную сторону. Стрелки указывают места электропорации. Закрытые наконечники стрел ( I , J , M , N , S , T ) указывают на аномальные волокна CST в SULF1/2 DKO Brain Opene HOMAR HOMAE HOMAE HOMERW HOMEROW HOMEROW HOMEROW HOMEROW HOMEROW HOMERW HOMEROW HOMAE HOMERW HOMERW HOMERW HOMERW HOMERW HOMERW HOMERW HOMERW HOMEROW HOMEROW HOMEROW HOMEROW HOMEROW HOMEN. указывают CST, восстановленный электропорацией. Статистический анализ нейрофиламент-позитивных волокон в среднем мозге ( q , s ) показан в дополнительной таблице 1.
Цифры ( q , r ) и ( s , t ) показаны электропорированные и неэлектропорированные стороны одного и того же эмбриона соответственно. Dorsal ( g , k , o ), lateral ( h , i , l , m , p , q , s ), and ventral ( j , n , r , t ) показаны виды. Флуоресценция EGFP в гипоталамусе ( ч ) показывает передачу через контралатеральную сторону. Стрелки указывают места электропорации. Закрытые наконечники стрел ( I , J , M , N , S , T ) указывают на аномальные волокна CST в SULF1/2 DKO Brain Opene HOMAR HOMAE HOMAE HOMERW HOMEROW HOMEROW HOMEROW HOMEROW HOMEROW HOMERW HOMEROW HOMAE HOMERW HOMERW HOMERW HOMERW HOMERW HOMERW HOMERW HOMERW HOMEROW HOMEROW HOMEROW HOMEROW HOMEROW HOMEN. указывают CST, восстановленный электропорацией. Статистический анализ нейрофиламент-позитивных волокон в среднем мозге ( q , s ) показан в дополнительной таблице 1.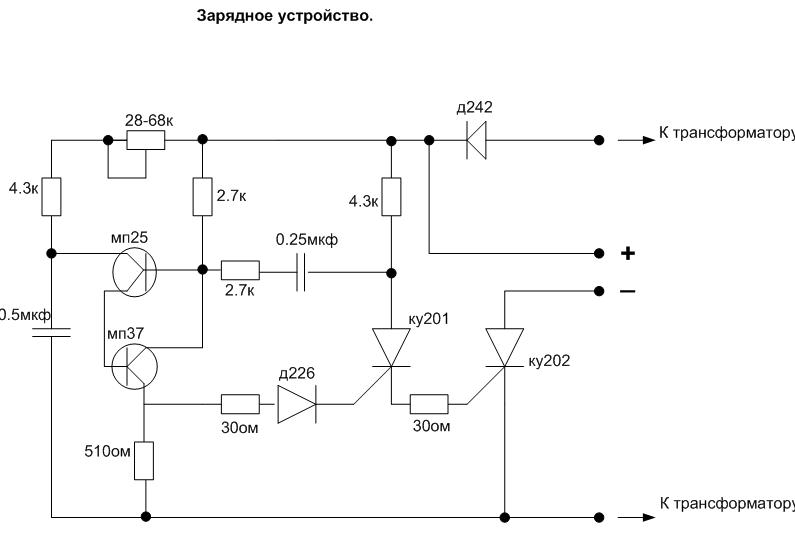 ( u – w ) Колокализация коэлектропорированных генов. Когда EGFP и DsRed2 электропорировали вместе, они экспрессировались в одних и тех же областях мозга. Ак, акведук; ЧП, сосудистое сплетение; CP, кортикальная пластинка; cst, корково-спинномозговой тракт; FM, отверстие Монро; ml, медиальная петля; ОВ — обонятельная луковица; PoA, преоптическая область; preTc, претектум; Sp, перегородка; Т; таламус; V3, третий желудочек. Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Масштабные линейки указывают 300 мкм ( a , a’ ), 750 мкм ( b – f , b’ – f’ ), 3.1 mm ( g , h , k , l , o , p ), 550 μm ( i , j , n , r , t ), 1.0 mm ( m , q , s ), and 2.1 mm ( u – w ). См. также дополнительный рисунок S2.
( u – w ) Колокализация коэлектропорированных генов. Когда EGFP и DsRed2 электропорировали вместе, они экспрессировались в одних и тех же областях мозга. Ак, акведук; ЧП, сосудистое сплетение; CP, кортикальная пластинка; cst, корково-спинномозговой тракт; FM, отверстие Монро; ml, медиальная петля; ОВ — обонятельная луковица; PoA, преоптическая область; preTc, претектум; Sp, перегородка; Т; таламус; V3, третий желудочек. Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Масштабные линейки указывают 300 мкм ( a , a’ ), 750 мкм ( b – f , b’ – f’ ), 3.1 mm ( g , h , k , l , o , p ), 550 μm ( i , j , n , r , t ), 1.0 mm ( m , q , s ), and 2.1 mm ( u – w ). См. также дополнительный рисунок S2.
Изображение в полный размер
Чтобы определить, какие области мозга с экспрессией Sulf необходимы для образования CST, мы выполнили in vivo спасение фенотипа Sulf1/2 DKO путем локального введения генов Sulf . Для этой цели мы электропорировали Sulf1 и Sulf2 с EGFP в различные области мозга на E12.5 и исследовали EGFP-положительную область и траекторию CST на E18.5. Мы выполнили электропорацию на E12.5, потому что это было до того, как аксоны CST начали расширяться, и потому что желудочки эмбрионального мозга были широко открыты, что позволяло легко вводить экзогенные гены в различные области. Чтобы вызвать сильную и повсеместную экспрессию, мы использовали вектор pCX, несущий промотор CAG 9.0147 16 . Удерживая эмбрионы с электродами под разными углами, экзогенные гены можно было электропорировать в интересующие ограниченные области мозга (рис. 2g–t). Поскольку коэлектропорированные гены коэкспрессировались в одной и той же области мозга (рис. 2u – w и дополнительная рис. S2a – d), EGFP-положительные области представляли области мозга, в которые были введены генов Sulf .
Для этой цели мы электропорировали Sulf1 и Sulf2 с EGFP в различные области мозга на E12.5 и исследовали EGFP-положительную область и траекторию CST на E18.5. Мы выполнили электропорацию на E12.5, потому что это было до того, как аксоны CST начали расширяться, и потому что желудочки эмбрионального мозга были широко открыты, что позволяло легко вводить экзогенные гены в различные области. Чтобы вызвать сильную и повсеместную экспрессию, мы использовали вектор pCX, несущий промотор CAG 9.0147 16 . Удерживая эмбрионы с электродами под разными углами, экзогенные гены можно было электропорировать в интересующие ограниченные области мозга (рис. 2g–t). Поскольку коэлектропорированные гены коэкспрессировались в одной и той же области мозга (рис. 2u – w и дополнительная рис. S2a – d), EGFP-положительные области представляли области мозга, в которые были введены генов Sulf .
Электропорация pCX- Sulf1/2 в кору головного мозга (5 мышей; рис. 2g–j) и в область от верхнего двухолмия до мозжечка (3 мыши; рис. 2k–n) не спасла Фенотип ДКО. Напротив, когда Sulf1 / 2 были электропорированы в области, включая гипоталамус и средний мозг, дефекты CST полностью восстановились до нормы только на стороне электропорации (6 мышей; рис. 2o–t). Более того, мутант Sulf1 , лишенный ферментативной активности, не мог восстановить фенотип (4 мыши; дополнительная рис. S2e–h), тогда как дикий тип Sulf1 или Sulf2 мог восстановить дефекты (4 мыши для Sulf1 и 3 мыши для Sulf2 ; дополнительный рисунок S2i–p). Эти данные указывают на то, что активность Sulf необходима не в кортикальных аксонах, а в середине траектории CST.
2g–j) и в область от верхнего двухолмия до мозжечка (3 мыши; рис. 2k–n) не спасла Фенотип ДКО. Напротив, когда Sulf1 / 2 были электропорированы в области, включая гипоталамус и средний мозг, дефекты CST полностью восстановились до нормы только на стороне электропорации (6 мышей; рис. 2o–t). Более того, мутант Sulf1 , лишенный ферментативной активности, не мог восстановить фенотип (4 мыши; дополнительная рис. S2e–h), тогда как дикий тип Sulf1 или Sulf2 мог восстановить дефекты (4 мыши для Sulf1 и 3 мыши для Sulf2 ; дополнительный рисунок S2i–p). Эти данные указывают на то, что активность Sulf необходима не в кортикальных аксонах, а в середине траектории CST.
Поскольку дефекты CST наблюдались только тогда, когда все 4 аллеля Sulf были потеряны, вполне вероятно, что области мозга, экспрессирующие оба Sulf1 и Sulf2 связаны с дефектами. Учитывая, что электропорация генов Sulf в гипоталамус и средний мозг спасла фенотип ДКО, вполне вероятно, что сильное перекрывание экспрессии Sulf1 / 2 в желудочковой зоне третьего желудочка играет решающую роль. Таким образом, мы задались вопросом, может ли селективная электропорация генов Sulf в эти клетки спасти фенотип DKO. Для удобства мы обнаружили, что вектор pEF-BOS 17 может индуцировать относительно специфическую экспрессию в этих клетках, хотя основной механизм неизвестен. При электропорации в гипоталамус и средний мозг pEF-BOS- EGFP индуцировал слабую, но ограниченную экспрессию в клетках желудочковой зоны (рис. 3a,b,e), тогда как pCX- EGFP индуцировал широкое выражение (рис. 2o, p и дополнительный рисунок S2a, c). Поэтому мы электропорировали pEF-BOS- Sulf1 и pEF-BOS- Sulf2 в головной мозг Sulf1/2 DKO и обнаружили, что дефекты CST были полностью устранены (3 мыши; рис. 3c, d). Эти данные показывают, что экспрессия Sulf в желудочковой зоне третьего желудочка была достаточной для правильного управления аксонами CST.
Учитывая, что электропорация генов Sulf в гипоталамус и средний мозг спасла фенотип ДКО, вполне вероятно, что сильное перекрывание экспрессии Sulf1 / 2 в желудочковой зоне третьего желудочка играет решающую роль. Таким образом, мы задались вопросом, может ли селективная электропорация генов Sulf в эти клетки спасти фенотип DKO. Для удобства мы обнаружили, что вектор pEF-BOS 17 может индуцировать относительно специфическую экспрессию в этих клетках, хотя основной механизм неизвестен. При электропорации в гипоталамус и средний мозг pEF-BOS- EGFP индуцировал слабую, но ограниченную экспрессию в клетках желудочковой зоны (рис. 3a,b,e), тогда как pCX- EGFP индуцировал широкое выражение (рис. 2o, p и дополнительный рисунок S2a, c). Поэтому мы электропорировали pEF-BOS- Sulf1 и pEF-BOS- Sulf2 в головной мозг Sulf1/2 DKO и обнаружили, что дефекты CST были полностью устранены (3 мыши; рис. 3c, d). Эти данные показывают, что экспрессия Sulf в желудочковой зоне третьего желудочка была достаточной для правильного управления аксонами CST.
Электропорация Sulf Гены в радиальных глиальных клетках гипоталамуса восстанавливают дефекты CST у мышей Sulf1/2 DKO. ( a – d ) Опосредованное электропорацией восстановление дефектов CST у мышей Sulf1/2 DKO. Указанные плазмиды и pEF-BOS- EGFP электропорировали в мозг E12.5 Sulf1/2 DKO. На E18.5 исследовали экспрессию EGFP и траекторию CST. Спинной ( a ), латеральный ( b , c ) и вентральный ( d ) показаны виды. Открытые стрелки ( c , d ) указывают на CST, восстановленный электропорацией. Стрелки указывают места электропорации. Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Статистический анализ нейрофиламент-позитивных волокон в среднем мозге ( c ) показан в дополнительной таблице 1. ( e — e” ) Экспрессия EGFP в pEF-BOS- EGFP -электропорированном мозге.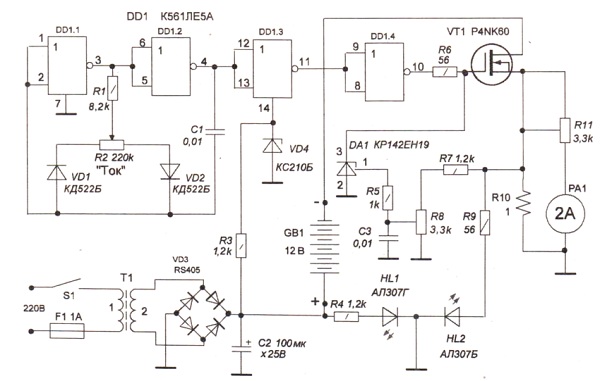 ( e’ ) показана иммуногистохимия с антителом против EGFP. ( e » ) показывает увеличенное изображение в выделенной области на ( e’ ). ( f – m ) Иммуногистохимия головного мозга E15.5 с анти-Sulf или анти-HS антителами. Сигналы с анти-Sulf1 в мозге Sulf2 KO ( f ) были устранены в мозге Sulf1/2 DKO ( г ), тогда как сигналы с анти-Sulf2 в мозге дикого типа ( h ) были упразднены в Sulf2 KO ( i ) головной мозг. Мозг Sulf2 KO и Sulf1/2 DKO использовали для окрашивания анти-Sulf1, поскольку антитело анти-Sulf1 слабо перекрестно реагирует с белком Sulf2. Сигналы с анти-HS AO4B08 ( j , k ) и анти-HS HS4E4 ( l , m ) в контроле ( Sulf1 -/- ) головного мозга ( j , l ) увеличивались и уменьшались в Sulf1/2 ДКО головного мозга ( к , м ) соответственно. Картинки ( ф 1 – м 1 ), ( ф 2 – м 2 ), ( ф 3 – м 3 ) и ( f 4 – и 4 ) показывают обведенные рамкой области с соответствующими номерами в отделе мозга на левом поле.
( e’ ) показана иммуногистохимия с антителом против EGFP. ( e » ) показывает увеличенное изображение в выделенной области на ( e’ ). ( f – m ) Иммуногистохимия головного мозга E15.5 с анти-Sulf или анти-HS антителами. Сигналы с анти-Sulf1 в мозге Sulf2 KO ( f ) были устранены в мозге Sulf1/2 DKO ( г ), тогда как сигналы с анти-Sulf2 в мозге дикого типа ( h ) были упразднены в Sulf2 KO ( i ) головной мозг. Мозг Sulf2 KO и Sulf1/2 DKO использовали для окрашивания анти-Sulf1, поскольку антитело анти-Sulf1 слабо перекрестно реагирует с белком Sulf2. Сигналы с анти-HS AO4B08 ( j , k ) и анти-HS HS4E4 ( l , m ) в контроле ( Sulf1 -/- ) головного мозга ( j , l ) увеличивались и уменьшались в Sulf1/2 ДКО головного мозга ( к , м ) соответственно. Картинки ( ф 1 – м 1 ), ( ф 2 – м 2 ), ( ф 3 – м 3 ) и ( f 4 – и 4 ) показывают обведенные рамкой области с соответствующими номерами в отделе мозга на левом поле. Звездочками показаны кровеносные сосуды. Масштабные линейки показывают 2,0 мм ( a , b ), 650 μm ( c , e , e’ ), 350 μm ( d ), 210 μm ( e” ), and 150 μm ( f – м ). См. также дополнительный рисунок S2.
Звездочками показаны кровеносные сосуды. Масштабные линейки показывают 2,0 мм ( a , b ), 650 μm ( c , e , e’ ), 350 μm ( d ), 210 μm ( e” ), and 150 μm ( f – м ). См. также дополнительный рисунок S2.
Увеличить
Для изучения локализации белка Sulf в головном мозге было проведено иммуноокрашивание. Оба белка Sulf1 и Sulf2 были обнаружены в клетках желудочковой зоны вдоль третьего желудочка (рис. 3f 4 ,h 4 ), что согласуется с локализацией Sulf1 и Sulf2 мРНК. Оба сигнала были устранены путем разрушения генов Sulf , что указывает на специфичность иммунного окрашивания (рис. 3g 4 , i 4 ). Интересно, что оба белка дополнительно обнаруживались на поверхности головного мозга: сильно вблизи ножки мозга и слабо в гипоталамусе (рис. 3f 2–3 ,h 2–3 ). Сульфатные белки, индуцированные электропорацией, демонстрировали сходные модели распределения (дополнительный рисунок S2b 9). 0911 3 , д 3 ). Поскольку EGFP-положительные клетки в pEF-BOS-EGFP-электропорированном мозге представляли собой радиальные глиальные клетки, простирающиеся длинными отростками от желудочковой зоны до пиальной поверхности (рис. 3e’–3e”), мы предположили, что Sulf-белки, продуцируемые радиальными глиальными клетками доставляются на пиальную поверхность.
0911 3 , д 3 ). Поскольку EGFP-положительные клетки в pEF-BOS-EGFP-электропорированном мозге представляли собой радиальные глиальные клетки, простирающиеся длинными отростками от желудочковой зоны до пиальной поверхности (рис. 3e’–3e”), мы предположили, что Sulf-белки, продуцируемые радиальными глиальными клетками доставляются на пиальную поверхность.
Чтобы проверить, изменяет ли разрушение генов Sulf паттерны сульфатирования HS локально, где присутствуют белки Sulf, мы провели иммунное окрашивание HS с использованием нескольких антител против фагового дисплея HS на E15.5, хотя наш дисахаридный анализ уже показал, что трисульфатированный Дисахариды HS были повышены во всем мозге новорожденных мышей DKO (дополнительная рис. S1a,b). Сигналы с антителами AO4B08 и RB4CD12, распознающими дисахариды HS, содержащие 2- O -, 6- O — и N -сульфатные группы 18,19 , были сильнее на поверхности мозга мышей DKO, чем у контрольных мышей, тогда как сигналы в кровеносных сосудах были сопоставимы между DKO и контрольными мышами (рис. 3j, k и дополнительный рисунок S2q – r). Увеличение сигналов AO4B08 и RB4CD12 было особенно заметным в ножке головного мозга и гипоталамусе. И наоборот, сигналы с HS4E4, который распознает дисахариды HS, содержащие 2- O — и N -сульфатные группы 18 , были слабее у мышей DKO (рис. 3l,m). Эти данные указывают на то, что доля трисульфатированных дисахаридов HS была увеличена на пиальной поверхности в результате разрушения Sulf1/2 . Поскольку изменения были наиболее сильными вокруг траектории CST, вполне вероятно, что это локальное изменение в HS способствует возникновению аномалий в аксонах CST.
3j, k и дополнительный рисунок S2q – r). Увеличение сигналов AO4B08 и RB4CD12 было особенно заметным в ножке головного мозга и гипоталамусе. И наоборот, сигналы с HS4E4, который распознает дисахариды HS, содержащие 2- O — и N -сульфатные группы 18 , были слабее у мышей DKO (рис. 3l,m). Эти данные указывают на то, что доля трисульфатированных дисахаридов HS была увеличена на пиальной поверхности в результате разрушения Sulf1/2 . Поскольку изменения были наиболее сильными вокруг траектории CST, вполне вероятно, что это локальное изменение в HS способствует возникновению аномалий в аксонах CST.
Какие механизмы лежат в основе дефектов CST у мышей Sulf1/2 DKO? Мы предположили, что увеличение количества трисульфатированного HS изменяет количество или локализацию некоторых белков-направителей аксонов. Чтобы определить ответственную молекулу (молекулы), мы сначала исследовали все известные белки управления аксонами, экспрессированные в гипоталамусе и среднем мозге на E15.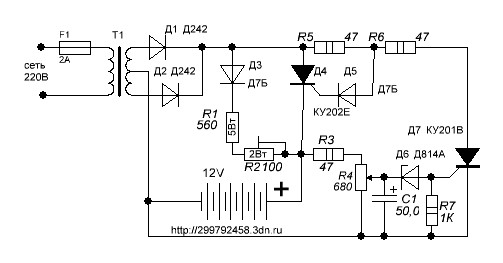 5, с помощью беспристрастного подхода с использованием протеомного анализа. Поскольку Sulfs модифицировал HS в базальной мембране, мозговые оболочки (обогащенные базальной мембраной) анализировали с использованием жидкостной хроматографии с масс-спектрометрией с ионной ловушкой (ЖХ-МС/МС). В таблице на дополнительном рисунке S3a показан список белков наведения аксонов, обнаруженных этим методом. Slit2, Sema3E, Sema4G, Sema5B и Sema6B были обнаружены только в мозге DKO, что позволяет предположить, что они были более распространены у мышей DKO. Напротив, Sema4D и EphrinB2 были обнаружены только в контрольном мозге, что позволяет предположить, что они были менее распространены у мышей DKO. Slit1 показал одинаковые спектральные подсчеты в контроле и мышах DKO.
5, с помощью беспристрастного подхода с использованием протеомного анализа. Поскольку Sulfs модифицировал HS в базальной мембране, мозговые оболочки (обогащенные базальной мембраной) анализировали с использованием жидкостной хроматографии с масс-спектрометрией с ионной ловушкой (ЖХ-МС/МС). В таблице на дополнительном рисунке S3a показан список белков наведения аксонов, обнаруженных этим методом. Slit2, Sema3E, Sema4G, Sema5B и Sema6B были обнаружены только в мозге DKO, что позволяет предположить, что они были более распространены у мышей DKO. Напротив, Sema4D и EphrinB2 были обнаружены только в контрольном мозге, что позволяет предположить, что они были менее распространены у мышей DKO. Slit1 показал одинаковые спектральные подсчеты в контроле и мышах DKO.
Чтобы точно определить молекулу(ы)-кандидата, мы исследовали их паттерны экспрессии и проверили, вызывает ли их сверхэкспрессия какие-либо изменения в траектории CST. Электропорация pCX- Sema3e в мозг дикого типа вызывала латеральный сдвиг CST в ножке мозга (3 мыши, рис. 4i,j), напоминающий фенотип слабого ДКО. мРНК Sema3e экспрессировалась вблизи ножки головного мозга (рис. 4a–c), что предполагает возможное участие в формировании CST. Однако Sema3e 9Сверхэкспрессия 0288 не вызывала таких дефектов CST, которые наблюдались в мозге Sulf1/2 DKO, что указывает на то, что избыток Sema3E сам по себе не может объяснить фенотип DKO. Электропорация pCX- Slit2 на E12.5 вызывала очень сильное отталкивание аксонов CST (рис. 4m), аналогично тяжелому фенотипу DKO и согласующееся с предыдущими наблюдениями 20,21 . Индукция более слабой экспрессии Slit2 электропорацией pEF-BOS- Slit2 (pEF-BOS индуцирует более слабую экспрессию, чем pCX) на E13.0 (более низкая эффективность электропорации, чем на E12.5) приводила к дефектам CST, которые были неотличимы от дефектов умеренного фенотипа ДКО (рис. 4p). 9мРНК 0287 Slit2 показала высокую экспрессию в желудочковой зоне третьего желудочка, особенно в заднем гипоталамусе (рис.
4i,j), напоминающий фенотип слабого ДКО. мРНК Sema3e экспрессировалась вблизи ножки головного мозга (рис. 4a–c), что предполагает возможное участие в формировании CST. Однако Sema3e 9Сверхэкспрессия 0288 не вызывала таких дефектов CST, которые наблюдались в мозге Sulf1/2 DKO, что указывает на то, что избыток Sema3E сам по себе не может объяснить фенотип DKO. Электропорация pCX- Slit2 на E12.5 вызывала очень сильное отталкивание аксонов CST (рис. 4m), аналогично тяжелому фенотипу DKO и согласующееся с предыдущими наблюдениями 20,21 . Индукция более слабой экспрессии Slit2 электропорацией pEF-BOS- Slit2 (pEF-BOS индуцирует более слабую экспрессию, чем pCX) на E13.0 (более низкая эффективность электропорации, чем на E12.5) приводила к дефектам CST, которые были неотличимы от дефектов умеренного фенотипа ДКО (рис. 4p). 9мРНК 0287 Slit2 показала высокую экспрессию в желудочковой зоне третьего желудочка, особенно в заднем гипоталамусе (рис. 4d–f и дополнительный рисунок S3p–s), что свидетельствует о колокализации и возможном сотрудничестве с Sulf1 / 2 . Напротив, экспрессия Slit1 не наблюдалась в вентрикулярной зоне вентральной части третьего желудочка (дополнительный рисунок S3l-o), и поэтому считалось, что Slit1 не имеет отношения к дефектам CST, хотя его избыточная экспрессия может вызывать отталкивание Аксоны CST (дополнительный рисунок S3t – u). Электропорация других генов-кандидатов не вызывала никаких аномалий CST в мозге дикого типа и не спасала фенотип DKO (дополнительный рисунок S3c, e, g, i, k).
4d–f и дополнительный рисунок S3p–s), что свидетельствует о колокализации и возможном сотрудничестве с Sulf1 / 2 . Напротив, экспрессия Slit1 не наблюдалась в вентрикулярной зоне вентральной части третьего желудочка (дополнительный рисунок S3l-o), и поэтому считалось, что Slit1 не имеет отношения к дефектам CST, хотя его избыточная экспрессия может вызывать отталкивание Аксоны CST (дополнительный рисунок S3t – u). Электропорация других генов-кандидатов не вызывала никаких аномалий CST в мозге дикого типа и не спасала фенотип DKO (дополнительный рисунок S3c, e, g, i, k).
Сверхэкспрессия Slit2 и Sema3e вызывает дефекты CST. ( a – f ) Гибридизация in situ Sema3e и Slit2 в коронарных срезах мозга E15.5. Sema3e был экспрессирован вблизи ножки мозга ( a – c , стрелки), тогда как Slit2 был высоко экспрессирован в вентрикулярной зоне заднего гипоталамуса и дорсальной срединной линии водопровода ( д – ф , наконечники стрел). Позиции разделов в ( a – f ) показаны на верхнем поле. ( g – p ) Влияние сверхэкспрессии Sema3e и Slit2 на аксоны CST. Указанные плазмиды и pCX- EGFP электропорировали в головной мозг дикого типа на E12.5 ( g – m ) или E13.0 ( n – p ). На E18.5 исследовали экспрессию EGFP и траекторию CST. 9Сверхэкспрессия 0287 Sema3e индуцировала латеральный сдвиг CST ( i , j , стрелки), который был подобен слабому фенотипу мышей Sulf1/2 DKO. Сильная сверхэкспрессия Slit2 с помощью электропорации pCX- Slit2 сильно отталкивала аксоны CST ( m , стрелки), что было сходно с тяжелым фенотипом мышей Sulf1/2 DKO. Затем более слабую сверхэкспрессию Slit2 индуцировали электропорацией pEF-BOS-9.0287 Slit2 на E13.0, когда эффективность электропорации снижалась из-за сужения желудочков (сравните сигналы EGFP, индуцированные pCX- EGFP , электропорированные на E12.
Позиции разделов в ( a – f ) показаны на верхнем поле. ( g – p ) Влияние сверхэкспрессии Sema3e и Slit2 на аксоны CST. Указанные плазмиды и pCX- EGFP электропорировали в головной мозг дикого типа на E12.5 ( g – m ) или E13.0 ( n – p ). На E18.5 исследовали экспрессию EGFP и траекторию CST. 9Сверхэкспрессия 0287 Sema3e индуцировала латеральный сдвиг CST ( i , j , стрелки), который был подобен слабому фенотипу мышей Sulf1/2 DKO. Сильная сверхэкспрессия Slit2 с помощью электропорации pCX- Slit2 сильно отталкивала аксоны CST ( m , стрелки), что было сходно с тяжелым фенотипом мышей Sulf1/2 DKO. Затем более слабую сверхэкспрессию Slit2 индуцировали электропорацией pEF-BOS-9.0287 Slit2 на E13.0, когда эффективность электропорации снижалась из-за сужения желудочков (сравните сигналы EGFP, индуцированные pCX- EGFP , электропорированные на E12. 5 [ 4g – h и 4k – l ] и на E13.0 [ 4n – o ]). Полученная таким образом умеренная экспрессия Slit2 индуцировала более слабые дефекты CST ( p , стрелки), что было похоже на умеренный фенотип мышей Sulf1/2 DKO. Также наблюдались дефекты в ретинотектальной проекции ( стр , стрелки). Стрелки в ( g – h ), ( k – l ) и ( n – o ) указывают места электропорации. Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Статистический анализ нейрофиламент-позитивных волокон в среднем мозге ( i , p ) показан в дополнительной таблице 1. Масштабные полосы показывают 550 мкм ( a – f ), 1,8 мм ( г , , 0387 h , k , l , n , o ), и 600 мкм ( i , j , j , 3 p , 3 p 9038). См. также дополнительный рисунок S3.
5 [ 4g – h и 4k – l ] и на E13.0 [ 4n – o ]). Полученная таким образом умеренная экспрессия Slit2 индуцировала более слабые дефекты CST ( p , стрелки), что было похоже на умеренный фенотип мышей Sulf1/2 DKO. Также наблюдались дефекты в ретинотектальной проекции ( стр , стрелки). Стрелки в ( g – h ), ( k – l ) и ( n – o ) указывают места электропорации. Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Статистический анализ нейрофиламент-позитивных волокон в среднем мозге ( i , p ) показан в дополнительной таблице 1. Масштабные полосы показывают 550 мкм ( a – f ), 1,8 мм ( г , , 0387 h , k , l , n , o ), и 600 мкм ( i , j , j , 3 p , 3 p 9038). См. также дополнительный рисунок S3.
Полноразмерное изображение
Таким образом, Slit2 оказался лучшим кандидатом, объясняющим дефекты CST, наблюдаемые у мышей Sulf1/2 DKO. Учитывая, что Slit2 связывается с HS с высокой аффинностью 22 6- O -сульфат-зависимым образом 23 , ожидается, что повышенный трисульфатированный HS будет связывать больше белка Slit2 в Sulf1/2 Мыши ДКО. В соответствии с этим прогнозом N-концевой фрагмент (активная форма) белка Slit2 был более распространен в мозговых оболочках мышей DKO, чем у контрольных мышей (рис. 5i и дополнительная рис. S4s). Таким образом, мы предположили, что увеличение белка Slit2 в вентральной области мозга вызывает дорсальное отталкивание аксонов CST у мышей DKO.
Учитывая, что Slit2 связывается с HS с высокой аффинностью 22 6- O -сульфат-зависимым образом 23 , ожидается, что повышенный трисульфатированный HS будет связывать больше белка Slit2 в Sulf1/2 Мыши ДКО. В соответствии с этим прогнозом N-концевой фрагмент (активная форма) белка Slit2 был более распространен в мозговых оболочках мышей DKO, чем у контрольных мышей (рис. 5i и дополнительная рис. S4s). Таким образом, мы предположили, что увеличение белка Slit2 в вентральной области мозга вызывает дорсальное отталкивание аксонов CST у мышей DKO.
Белок Slit2, аномально накопленный на пиальной поверхности заднего гипоталамуса Sulf1/2 DKO Мыши. ( a – e ) Связывание Robo2-Fc на срезах головного мозга контрольной группы ( Sulf1 -/- ) и мышей Sulf1/2 DKO и мышей Sulf1/2 DKO, подвергнутых электропорации с указанными плазмидами. ( а 1 – и 1 ), ( и 2 – и 2 ) и ( и 3 – и 3 ) указывают области, включающие верхнее двухолмие, ножку мозга и гипоталамус, соответственно (показаны в прямоугольниках на левой панели). Цифры ( а — с ) и на рисунках ( d , e ) показаны противоположные стороны срезов головного мозга. Con, сторона управления; Ep, электропорированная сторона. ( f ) Количественный анализ связывания Robo2-Fc.
( а 1 – и 1 ), ( и 2 – и 2 ) и ( и 3 – и 3 ) указывают области, включающие верхнее двухолмие, ножку мозга и гипоталамус, соответственно (показаны в прямоугольниках на левой панели). Цифры ( а — с ) и на рисунках ( d , e ) показаны противоположные стороны срезов головного мозга. Con, сторона управления; Ep, электропорированная сторона. ( f ) Количественный анализ связывания Robo2-Fc. Среднее значение интенсивности флуоресценции (условная единица; а.е.) на пиальной поверхности, полученное с помощью конфокальной микроскопии у контрольных мышей (n = 3, 2 Sulf1 -/- ; Сульф2 +/− и 1 Sulf1 -/- ), мышей Sulf1/2 DKO (n = 3) и мышей Sulf1/2 DKO, подвергнутых электропорации с pCX- Sulf1/2 (n = 4) или pCX- Sulf1 (n = 4) C87A ) (n = 4). Статистическую значимость рассчитывали с использованием ANOVA с апостериорным критерием Тьюки-Крамера (** P < 0,01; *** P < 0,001; **** P < 0,0001). ( г , ч ) Колокализация связывания Robo2-Fc и иммунного окрашивания против ламинина в ножке головного мозга ( g ) и гипоталамусе ( h ) мышей Sulf1/2 DKO. ( i ) Вестерн-блот-анализ белка Slit2 в мозговых оболочках, выделенных из гипоталамуса и среднего мозга мышей E15.
Среднее значение интенсивности флуоресценции (условная единица; а.е.) на пиальной поверхности, полученное с помощью конфокальной микроскопии у контрольных мышей (n = 3, 2 Sulf1 -/- ; Сульф2 +/− и 1 Sulf1 -/- ), мышей Sulf1/2 DKO (n = 3) и мышей Sulf1/2 DKO, подвергнутых электропорации с pCX- Sulf1/2 (n = 4) или pCX- Sulf1 (n = 4) C87A ) (n = 4). Статистическую значимость рассчитывали с использованием ANOVA с апостериорным критерием Тьюки-Крамера (** P < 0,01; *** P < 0,001; **** P < 0,0001). ( г , ч ) Колокализация связывания Robo2-Fc и иммунного окрашивания против ламинина в ножке головного мозга ( g ) и гипоталамусе ( h ) мышей Sulf1/2 DKO. ( i ) Вестерн-блот-анализ белка Slit2 в мозговых оболочках, выделенных из гипоталамуса и среднего мозга мышей E15.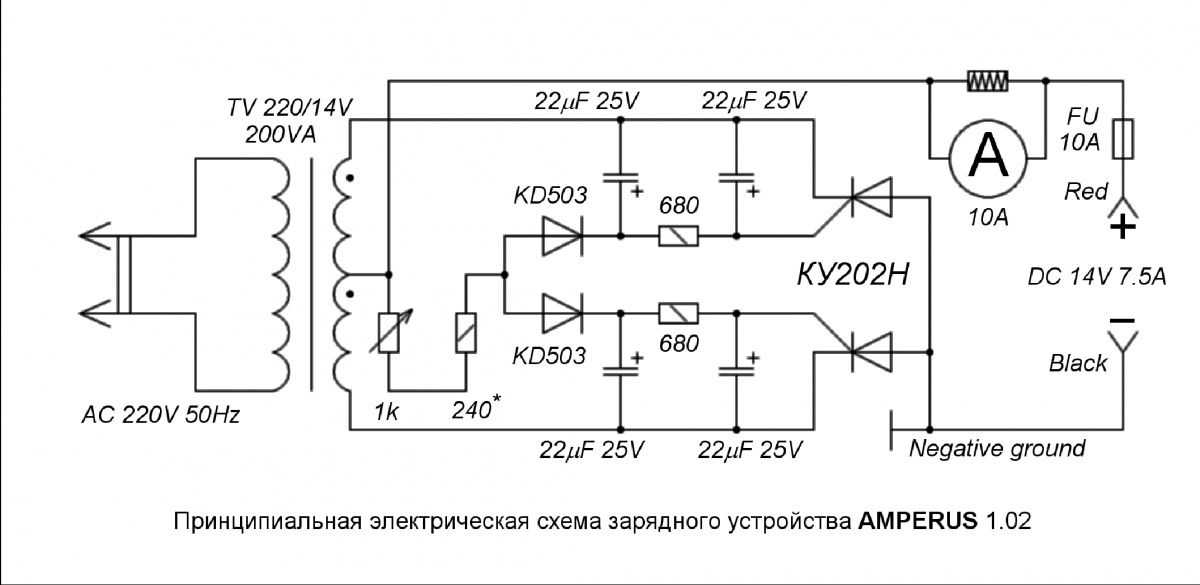 5. Slit2 был более обильным у мышей Sulf1/2 DKO, чем в контроле ( Sulf2 -/- ) мышей. FL и N обозначают полноразмерные (~180 кДа) и N-концевые фрагменты (~130 кДа) соответственно. Добавление блокирующего пептида устраняло полосы (правая панель), указывая на специфичность антитела. Полноразмерные пятна, которые использовались для этого изображения, показаны на дополнительном рисунке S7. ( j , k ) Связывание Robo2-Fc было полностью устранено в мозге Sulf1/Sulf2/Slit2 с тройным нокаутом (TKO). ( l , m ) Нейтрализация Slit восстанавливает дефекты CST у мышей Sulf1/2 DKO. Плазмиды pCX- Robo2-Fc и pCX- EGFP электропорировали в головной мозг E12.5 Sulf1/2 DKO и исследовали траекторию CST на E18.5. CST была почти нормализована электропорацией (незакрашенные стрелки), но располагалась немного латеральнее медиальной петли (ml). Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела.
5. Slit2 был более обильным у мышей Sulf1/2 DKO, чем в контроле ( Sulf2 -/- ) мышей. FL и N обозначают полноразмерные (~180 кДа) и N-концевые фрагменты (~130 кДа) соответственно. Добавление блокирующего пептида устраняло полосы (правая панель), указывая на специфичность антитела. Полноразмерные пятна, которые использовались для этого изображения, показаны на дополнительном рисунке S7. ( j , k ) Связывание Robo2-Fc было полностью устранено в мозге Sulf1/Sulf2/Slit2 с тройным нокаутом (TKO). ( l , m ) Нейтрализация Slit восстанавливает дефекты CST у мышей Sulf1/2 DKO. Плазмиды pCX- Robo2-Fc и pCX- EGFP электропорировали в головной мозг E12.5 Sulf1/2 DKO и исследовали траекторию CST на E18.5. CST была почти нормализована электропорацией (незакрашенные стрелки), но располагалась немного латеральнее медиальной петли (ml). Показаны передне-задняя (AP), дорсально-вентральная (DV) и медиально-латеральная (M-L) оси тела. Масштабные полосы показывают 100 мкм ( a – e , j , k ), 50 мкм ( g , h ) и 500 мкм ( l , m). См. также дополнительный рисунок S4–7.
Масштабные полосы показывают 100 мкм ( a – e , j , k ), 50 мкм ( g , h ) и 500 мкм ( l , m). См. также дополнительный рисунок S4–7.
Изображение в полный размер
Аномально высокое количество белка Slit2 накапливается на поверхности пиала мышей
Sulf1/2 DKO Чтобы проверить эту возможность, мы хотели обнаружить белок Slit2 в эмбриональном мозге. Однако, поскольку антитела для иммунного окрашивания Slit2 отсутствовали, мы использовали внеклеточную часть Robo2, рецептора Slit, который был помечен Fc-областью человеческого IgG (Robo2-Fc; ссылка 9).0147 24 ). Во-первых, мы подтвердили, что Robo2-Fc связывается с Slit2 в трансфицированных клетках (дополнительная рис. S4a – d, f). Затем мы проверили связывание Robo2-Fc на срезах головного мозга, подвергнутых электропорации с помощью pCX-FLAG- Slit2 . Когда срезы мозга инкубировали с Robo2-Fc, связывание было четко обнаружено только на стороне электропорации и было локализовано с эпитопом FLAG (дополнительный рисунок S4m-r), что указывает на то, что Robo2-Fc может обнаруживать белок Slit2 в срезах мозга. Связывание Robo2-Fc было сильно обнаружено на поверхности головного мозга в дополнение к клеточным телам электропорированных клеток в вентрикулярной зоне и паренхиме головного мозга.
Связывание Robo2-Fc было сильно обнаружено на поверхности головного мозга в дополнение к клеточным телам электропорированных клеток в вентрикулярной зоне и паренхиме головного мозга.
Затем мы проверили, изменило ли нарушение генов Sulf локализацию Slit. Связывание Robo2-Fc практически не обнаруживалось в головном мозге контрольной группы, за исключением слабых сигналов на пиальной поверхности верхнего двухолмия (рис. 5а). Напротив, у мышей Sulf1/2 DKO было обнаружено сильное связывание Robo2-Fc на пиальной поверхности, особенно в областях ножки мозга и гипоталамуса (рис. 5b). Количественное сравнение показало, что интенсивность сигнала в Sulf1/2 9У мышей 0288 DKO было значительно выше в ножке мозга и гипоталамусе, чем в контроле, но было сопоставимо в верхнем двухолмии (рис. 5f). Связывание Robo2-Fc было локализовано вместе с ламинином (рис. 5g–h), что позволяет предположить, что белок Slit был связан с базальной мембраной. Кроме того, связывание Robo2-Fc в мозге DKO было полностью устранено путем делеции гена Slit2 (а именно в мозге тройного нокаута), за исключением слабых сигналов в верхнем двухолмии (рис. 5j – k и дополнительный рисунок S5a). –e), предполагая, что сигналы связывания Robo2-Fc в ножке головного мозга и гипоталамусе указывают на локализацию белка Slit2. Эти данные ясно показали, что белок Slit2 избыточно накапливался в вентральной области мозга Sulf1/2 Мыши ДКО.
5j – k и дополнительный рисунок S5a). –e), предполагая, что сигналы связывания Robo2-Fc в ножке головного мозга и гипоталамусе указывают на локализацию белка Slit2. Эти данные ясно показали, что белок Slit2 избыточно накапливался в вентральной области мозга Sulf1/2 Мыши ДКО.
Повышенные уровни связывания Robo2-Fc у мышей Sulf1/2 DKO были восстановлены до контрольных уровней с помощью электропорации Sulf1/2 , которую проводили в тех же условиях, что и в экспериментах по восстановлению фенотипа, тогда как электропорация мутанта Sulf1 оказалась неэффективной (рис. 5c–e). Морфология базальной мембраны и радиальных глиальных клеток, по оценке иммуноокрашивания ламинином и нестином, была нормальной в Мыши Sulf1/2 DKO (дополнительный рисунок S5f – i). Кроме того, не наблюдалось увеличения экспрессии мРНК Slit2 у мышей Sulf1/2 DKO (данные не показаны). В совокупности эти данные показывают, что аномально высокие количества белка Slit2 накапливаются в вентральной области мозга, вызывая дефекты ведения аксонов CST у мышей Sulf1/2 DKO (рис.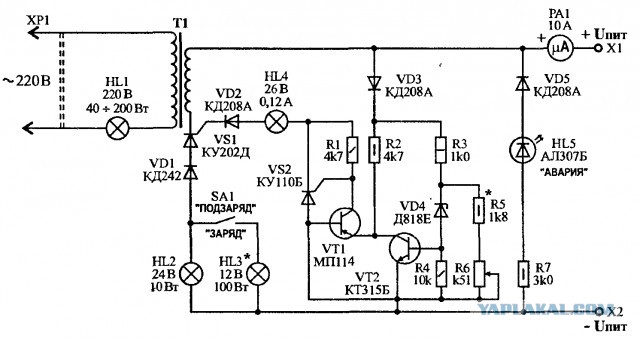 6).
6).
Краткий обзор фенотипов CST. У контрольных мышей белки Sulf1/2 и Slit2, продуцируемые радиальными глиальными клетками, присутствуют на пиальной поверхности. В 9У мышей 0287 Sulf1/2 DKO повышенное содержание 6- O -сульфатированного HS приводит к избыточному накоплению белка Slit2 (показан темно-синим цветом) в задней части гипоталамуса, что приводит к дорсальному смещению CST. Поскольку мыши DKO умирают в течение дня после рождения, CST каудальнее пирамидного перекреста не исследовали (пунктирные линии). У мышей Slit2 KO аксоны CST проникают в вентральную часть переднего мозга из-за отсутствия отталкивания Slit2.
Полноразмерное изображение
Аномальное накопление белка Slit2 ответственно за дефекты CST в
Sulf1/2 Мыши DKO Наконец, мы проверили, может ли снижение уровней Slit2 у мышей Sulf1/2 DKO восстановить дефекты CST. Во-первых, мы электропорировали Slit2 siRNA в мозг DKO, но не смогли значительно снизить уровни Slit2, и фенотип DKO не был восстановлен (данные не показаны). Затем мы получили мышей Sulf1/2 DKO с гетерозиготной делецией Slit2 и обнаружили, что дефекты CST не восстанавливались до нормы. Это согласуется с выводом о том, что сигналы связывания Robo2-Fc все еще обнаруживаются после удаления одного аллеля из Slit2 (дополнительный рисунок S5b, e). Наконец, мы попытались снизить активность Slit с помощью сверхэкспрессии Robo2-Fc, которая показала свою эффективность в нейтрализации активности Slit in vitro . 25,26 . Сильная сверхэкспрессия Robo2-Fc с помощью электропорации pCX- Robo2-Fc восстанавливала фенотип DKO на стороне электропорации (n = 2/3 у мышей Sulf1/2 DKO; n = 3/6 у мышей Sulf1 -/- ; Сульф2 -/- ; Щель2 +/- мышей; Рис. 5л–м). Однако даже у спасенных мышей восстановление не было полным: аксоны CST были обращены медиально к мосту, но располагались латеральнее медиального лемниска, напоминая слабый фенотип мышей Sulf1/2 DKO.
Затем мы получили мышей Sulf1/2 DKO с гетерозиготной делецией Slit2 и обнаружили, что дефекты CST не восстанавливались до нормы. Это согласуется с выводом о том, что сигналы связывания Robo2-Fc все еще обнаруживаются после удаления одного аллеля из Slit2 (дополнительный рисунок S5b, e). Наконец, мы попытались снизить активность Slit с помощью сверхэкспрессии Robo2-Fc, которая показала свою эффективность в нейтрализации активности Slit in vitro . 25,26 . Сильная сверхэкспрессия Robo2-Fc с помощью электропорации pCX- Robo2-Fc восстанавливала фенотип DKO на стороне электропорации (n = 2/3 у мышей Sulf1/2 DKO; n = 3/6 у мышей Sulf1 -/- ; Сульф2 -/- ; Щель2 +/- мышей; Рис. 5л–м). Однако даже у спасенных мышей восстановление не было полным: аксоны CST были обращены медиально к мосту, но располагались латеральнее медиального лемниска, напоминая слабый фенотип мышей Sulf1/2 DKO. Частота восстановления фенотипа у pCX- Robo2-Fc -электропорированных эмбрионов была значительно выше, чем частота появления слабого фенотипа у неэлектропорированных Sulf1/2 Мыши DKO (5/9 и 7/70 для мышей с электропорацией и без электропорации соответственно; P = 0,003, точный критерий Фишера). Эти данные показывают, что подавление активности Slit за счет сверхэкспрессии Robo2-Fc приводит к восстановлению дефектов CST у мышей Sulf1/2 DKO. Наблюдение, что Robo2-Fc не полностью устраняет дефекты CST, может быть объяснено более слабыми эффектами других молекул ведения аксонов (например, Sema3E). В совокупности наши результаты демонстрируют, что аномальное накопление белка Slit2 в основном ответственно за дефекты наведения аксонов CST у 9 животных.0287 Sulf1/2 Мыши ДКО.
Частота восстановления фенотипа у pCX- Robo2-Fc -электропорированных эмбрионов была значительно выше, чем частота появления слабого фенотипа у неэлектропорированных Sulf1/2 Мыши DKO (5/9 и 7/70 для мышей с электропорацией и без электропорации соответственно; P = 0,003, точный критерий Фишера). Эти данные показывают, что подавление активности Slit за счет сверхэкспрессии Robo2-Fc приводит к восстановлению дефектов CST у мышей Sulf1/2 DKO. Наблюдение, что Robo2-Fc не полностью устраняет дефекты CST, может быть объяснено более слабыми эффектами других молекул ведения аксонов (например, Sema3E). В совокупности наши результаты демонстрируют, что аномальное накопление белка Slit2 в основном ответственно за дефекты наведения аксонов CST у 9 животных.0287 Sulf1/2 Мыши ДКО.
Обсуждение
В этом исследовании мы продемонстрировали, что Sulf-опосредованное обрезание 6- O -сульфатных групп в HS необходимо для направления аксонов CST. В норме Sulfs, продуцируемые клетками радиальной глии, модифицируют паттерны сульфатирования HS в базальной мембране пиальных желез. Потеря Sulfs приводит к увеличению 6- O -сульфатированных HS, приводя к накоплению белка Slit2 и дорсальному смещению CST. Это резко контрастирует с фенотипом Мыши Slit/Robo KO, у которых аксоны CST проникают в вентральный мозг из-за отсутствия отталкивания 21,27 (рис. 6). Мы предлагаем новый регуляторный механизм, с помощью которого десульфатация HS обеспечивает точное направление аксонов за счет сдерживания накопления белка Slit2. Хотя мы представили недвусмысленные доказательства того, что Slit2 является основной причиной этого конкретного фенотипа CST, возможное участие др. молекул в других дефектах ведения аксонов заслуживает изучения в будущем.
Потеря Sulfs приводит к увеличению 6- O -сульфатированных HS, приводя к накоплению белка Slit2 и дорсальному смещению CST. Это резко контрастирует с фенотипом Мыши Slit/Robo KO, у которых аксоны CST проникают в вентральный мозг из-за отсутствия отталкивания 21,27 (рис. 6). Мы предлагаем новый регуляторный механизм, с помощью которого десульфатация HS обеспечивает точное направление аксонов за счет сдерживания накопления белка Slit2. Хотя мы представили недвусмысленные доказательства того, что Slit2 является основной причиной этого конкретного фенотипа CST, возможное участие др. молекул в других дефектах ведения аксонов заслуживает изучения в будущем.
Генетические исследования на мышах и рыбках данио продемонстрировали необходимость биосинтеза HS в ведении аксонов 2,4,28,29,30 . В частности, модификация HS специфическими сульфотрансферазами также вовлечена в ведение аксонов 2,4,31,32,33,34,35,36 . Эти исследования показывают, что присутствие HS и его сульфатных групп необходимо для передачи сигналов наведения аксонов. Учитывая, что сульфатные группы в определенных положениях в HS необходимы для взаимодействия между HS и сигнальными молекулами 23 , считается, что десульфатирование имеет такое же значение, как и сульфатирование, в регуляции функций HS. Соответственно, наше настоящее исследование продемонстрировало, что формирование HS путем удаления сульфатных групп в определенных положениях важно для ведения аксонов. Sulfs, таким образом, могут действовать как динамический регулятор, который контролирует HS-зависимую передачу сигналов пространственно-временным образом.
Учитывая, что сульфатные группы в определенных положениях в HS необходимы для взаимодействия между HS и сигнальными молекулами 23 , считается, что десульфатирование имеет такое же значение, как и сульфатирование, в регуляции функций HS. Соответственно, наше настоящее исследование продемонстрировало, что формирование HS путем удаления сульфатных групп в определенных положениях важно для ведения аксонов. Sulfs, таким образом, могут действовать как динамический регулятор, который контролирует HS-зависимую передачу сигналов пространственно-временным образом.
Хотя многие линии доказательств указывают на зависимость от HS передачи сигналов Slit/Robo, то, как HS взаимодействует с Slit/Robo и регулирует их передачу сигналов in vivo , остается в значительной степени неуловимым, особенно в мозге позвоночных. Мы разработали метод обнаружения белка Slit2 на срезах головного мозга и четко продемонстрировали локализацию белка Slit2 на базальной мембране пиальных мышц в мозге Sulf1/2 DKO. Более того, мы показали, что накопление Slit2 было связано с трисульфатированными дисахаридами HS. Учитывая, что Slit2 прочно связывается с 6- O -сульфатированный гепарин 23 , вполне вероятно, что накопление Slit2 в мозге ДКО было связано с повышением стабильности Slit2 под действием 6- O -сульфатированных ГС. Интересно, что связывание Robo2-Fc в контрольном мозге было ниже уровня обнаружения в исследованной области, указывая на быструю диффузию и/или деградацию белка Slit2 in vivo . Это означает, что отделение Slit2 от HS посредством десульфатации способствует тонкой настройке активности Slit2. В этом контексте примечательно, что в нашем протеомном анализе контрольного мозга фрагмент Slit2 был обнаружен в малой фракции (53–65 кДа), но не в крупной фракции, соответствующей активному N-концевому Фрагмент Slit2 (100–140 кДа).
Более того, мы показали, что накопление Slit2 было связано с трисульфатированными дисахаридами HS. Учитывая, что Slit2 прочно связывается с 6- O -сульфатированный гепарин 23 , вполне вероятно, что накопление Slit2 в мозге ДКО было связано с повышением стабильности Slit2 под действием 6- O -сульфатированных ГС. Интересно, что связывание Robo2-Fc в контрольном мозге было ниже уровня обнаружения в исследованной области, указывая на быструю диффузию и/или деградацию белка Slit2 in vivo . Это означает, что отделение Slit2 от HS посредством десульфатации способствует тонкой настройке активности Slit2. В этом контексте примечательно, что в нашем протеомном анализе контрольного мозга фрагмент Slit2 был обнаружен в малой фракции (53–65 кДа), но не в крупной фракции, соответствующей активному N-концевому Фрагмент Slit2 (100–140 кДа).
Точное определение местоположения разреза необходимо для точного направления растущих аксонов. В дополнение к HS, гликозилированный дистрогликан и коллаген типа IV были вовлечены во взаимодействие с белком Slit и Slit-опосредованным наведением аксонов 37,38 . В частности, у рыбок данио было показано, что белок Slit1 перемещается на поверхность тектума под действием радиальных глиальных клеток и закрепляется на базальной мембране посредством взаимодействия с коллагеном IV типа 37 . В сочетании с этими данными наши результаты позволяют предположить, что транспорт белка Slit на поверхность мозга радиальными глиальными клетками является обобщенным механизмом, контролирующим направление аксонов. В двух недавних работах сообщалось об аналогичном механизме, при котором белок нетрин-1, продуцируемый клетками-предшественниками желудочковой зоны, транспортируется на пиальную поверхность для направления комиссуральных аксонов в спинном и заднем мозге 39,40 , хотя участие HS еще предстоит изучить . Необходимы дальнейшие исследования, чтобы прояснить, как Sulfs играют совместную роль в закреплении направляющих белков в базальной мембране с дистрогликаном и коллагеном IV типа.
В частности, у рыбок данио было показано, что белок Slit1 перемещается на поверхность тектума под действием радиальных глиальных клеток и закрепляется на базальной мембране посредством взаимодействия с коллагеном IV типа 37 . В сочетании с этими данными наши результаты позволяют предположить, что транспорт белка Slit на поверхность мозга радиальными глиальными клетками является обобщенным механизмом, контролирующим направление аксонов. В двух недавних работах сообщалось об аналогичном механизме, при котором белок нетрин-1, продуцируемый клетками-предшественниками желудочковой зоны, транспортируется на пиальную поверхность для направления комиссуральных аксонов в спинном и заднем мозге 39,40 , хотя участие HS еще предстоит изучить . Необходимы дальнейшие исследования, чтобы прояснить, как Sulfs играют совместную роль в закреплении направляющих белков в базальной мембране с дистрогликаном и коллагеном IV типа.
Наши результаты также имеют важное значение в том, что активность Slit2 может регулироваться путем изменения микроструктуры HS во внеклеточной среде без изменения экспрессии Slit2 . Манипуляции с локализацией и активностью молекул, направляющих аксоны, с помощью Sulfs или родственных гепарину химических веществ 41 могут быть полезны для контроля действия химиопеллентов для стимулирования регенерации аксонов CST.
Манипуляции с локализацией и активностью молекул, направляющих аксоны, с помощью Sulfs или родственных гепарину химических веществ 41 могут быть полезны для контроля действия химиопеллентов для стимулирования регенерации аксонов CST.
Методы
Нокаутные мыши
Мышей с нокаутом Sulf получали, как описано ранее 19 . Использовали потомство мышей, подвергнутых обратному скрещиванию с C57BL/6N в течение 5 поколений (поколение N5). Мышей с нокаутом Slit2 получали из Региональных ресурсных центров по мутантным мышам. Полдень дня, когда наблюдалась вагинальная пробка, принимался за эмбриональный день 0,5 (Е0,5). Все эксперименты на животных были одобрены и проведены в соответствии с рекомендациями Комитета по уходу и использованию животных Университета Цукуба.
Дисахаридный анализ гепарансульфата и хондроитинсульфата
Дисахаридный анализ проводили, как описано ранее 19 , с использованием головного мозга новорожденных, поскольку большинство мышей DKO умерло в течение дня после рождения. Вкратце, экстрагированный ацетоном мозг новорожденных мышей обрабатывали 0,8 мг/мл протеазы (P5147; Sigma) при 55 °C в течение ночи, а затем 125 ед. бензоназы (Sigma) при 37 °C в течение 2 часов. После центрифугирования супернатанты очищали с помощью Vivapure D Mini M (Vivascience) и концентрировали с помощью Ultrafree-MC Biomax-5 (Millipore). Очищенные гликозаминогликаны обрабатывали при 37 °C в течение ночи смесью 1 мМЕ гепариназы I (Sigma), 1 мМЕ гепаритиназы I (Seikagaku) и 1 мМЕ гепаритиназы II (Seikagaku) или смесью 50 мМЕ хондроитиназы. ABC (Seikagaku) и 50 мМЕ хондроитиназы ACII (Seikagaku). Ненасыщенные дисахариды анализировали методом ионно-парной обращенно-фазовой хроматографии. Градиент NaCl (2–106 мМ) в 1,2 мМ тетра- n -бутиламмонийгидросульфат (Wako Pure Chemical Industries) и 8,5% ацетонитрил (Sigma) наносили на колонку Senshu Pak Docosil (4,6 × 150 мм, размер частиц 5 мкм; Senshu Scientific) при 55°C с использованием системы ВЭЖХ. , разделительный модуль Alliance 2695 (Waters Corporation).
Вкратце, экстрагированный ацетоном мозг новорожденных мышей обрабатывали 0,8 мг/мл протеазы (P5147; Sigma) при 55 °C в течение ночи, а затем 125 ед. бензоназы (Sigma) при 37 °C в течение 2 часов. После центрифугирования супернатанты очищали с помощью Vivapure D Mini M (Vivascience) и концентрировали с помощью Ultrafree-MC Biomax-5 (Millipore). Очищенные гликозаминогликаны обрабатывали при 37 °C в течение ночи смесью 1 мМЕ гепариназы I (Sigma), 1 мМЕ гепаритиназы I (Seikagaku) и 1 мМЕ гепаритиназы II (Seikagaku) или смесью 50 мМЕ хондроитиназы. ABC (Seikagaku) и 50 мМЕ хондроитиназы ACII (Seikagaku). Ненасыщенные дисахариды анализировали методом ионно-парной обращенно-фазовой хроматографии. Градиент NaCl (2–106 мМ) в 1,2 мМ тетра- n -бутиламмонийгидросульфат (Wako Pure Chemical Industries) и 8,5% ацетонитрил (Sigma) наносили на колонку Senshu Pak Docosil (4,6 × 150 мм, размер частиц 5 мкм; Senshu Scientific) при 55°C с использованием системы ВЭЖХ. , разделительный модуль Alliance 2695 (Waters Corporation). Постколоночную дериватизацию 2-цианоацетамидом (Wako Pure Chemical Industries) проводили при 125°C с использованием постколоночного реакционного модуля (Waters Corporation) и модуля контроля температуры II (Waters Corporation). Выходящий поток контролировали флуорометрически с использованием многоканального флуоресцентного детектора 2475 (возбуждение 346 нм, эмиссия 410 нм; Waters Corporation). Пики идентифицировали и количественно определяли путем сравнения с аутентичными маркерами ненасыщенных дисахаридов, набором ненасыщенных HS/HEP-дисахаридов (H Mix; Seikagaku), ΔUA2S-GlcNAc и ΔUA2S-GlcNAc6S (Dextra Laboratories) и набором ненасыщенных хондро-дисахаридов (C -Комплект) (Сейкагаку). Хроматограмму анализировали с использованием программного обеспечения Empower (Waters Corporation), а результаты подвергали статистическому анализу с использованием двустороннего дисперсионного анализа с апостериорным тестом Бонферрони.
Постколоночную дериватизацию 2-цианоацетамидом (Wako Pure Chemical Industries) проводили при 125°C с использованием постколоночного реакционного модуля (Waters Corporation) и модуля контроля температуры II (Waters Corporation). Выходящий поток контролировали флуорометрически с использованием многоканального флуоресцентного детектора 2475 (возбуждение 346 нм, эмиссия 410 нм; Waters Corporation). Пики идентифицировали и количественно определяли путем сравнения с аутентичными маркерами ненасыщенных дисахаридов, набором ненасыщенных HS/HEP-дисахаридов (H Mix; Seikagaku), ΔUA2S-GlcNAc и ΔUA2S-GlcNAc6S (Dextra Laboratories) и набором ненасыщенных хондро-дисахаридов (C -Комплект) (Сейкагаку). Хроматограмму анализировали с использованием программного обеспечения Empower (Waters Corporation), а результаты подвергали статистическому анализу с использованием двустороннего дисперсионного анализа с апостериорным тестом Бонферрони.
Гистология и иммуногистохимия
Криостатные (толщиной 10 мкм) срезы головного мозга, фиксированного параформальдегидом (PFA), использовали для иммуногистохимии. Для обнаружения белков Sulf или Slit и HS использовали свежезамороженные срезы, фиксированные 95% этанолом и 1% уксусной кислотой 42 . В качестве первичных антител использовали анти-нейрофиламент-М (1:1000; Zymed), анти-FLAG (1:500; Abcam, ab6711), анти-GFP (1:1000; Molecular Probes), анти-Sulf1 (1:50) ; Abcam, ab32763), анти-Sulf2 (1:50; Санта-Крус, M79), анти-HS (1:5; AO4B08; ссылки 18,19 ), антинестин (1:1000; Chemicon) и антиламинин (1:1000; Sigma). В качестве вторичных антител использовали конъюгированные с пероксидазой антимышиные IgG (1:200; Chemicon) и конъюгированные с Alexa488 или Alexa568 антикроличьи IgG (1:250; Molecular Probes). Хромогенную реакцию проводили с использованием набора VECTASTAIN Elite ABC и набора субстратов DAB (Vector Laboratories). Для иммунофлуоресценции ядра клеток окрашивали 3,3 мкМ йодида TO-PRO-3 (Molecular Probes). Было проведено иммуноокрашивание всего препарата (с небольшими модификациями) с использованием тех же реагентов после удаления мозговых оболочек 43 .
Для обнаружения белков Sulf или Slit и HS использовали свежезамороженные срезы, фиксированные 95% этанолом и 1% уксусной кислотой 42 . В качестве первичных антител использовали анти-нейрофиламент-М (1:1000; Zymed), анти-FLAG (1:500; Abcam, ab6711), анти-GFP (1:1000; Molecular Probes), анти-Sulf1 (1:50) ; Abcam, ab32763), анти-Sulf2 (1:50; Санта-Крус, M79), анти-HS (1:5; AO4B08; ссылки 18,19 ), антинестин (1:1000; Chemicon) и антиламинин (1:1000; Sigma). В качестве вторичных антител использовали конъюгированные с пероксидазой антимышиные IgG (1:200; Chemicon) и конъюгированные с Alexa488 или Alexa568 антикроличьи IgG (1:250; Molecular Probes). Хромогенную реакцию проводили с использованием набора VECTASTAIN Elite ABC и набора субстратов DAB (Vector Laboratories). Для иммунофлуоресценции ядра клеток окрашивали 3,3 мкМ йодида TO-PRO-3 (Molecular Probes). Было проведено иммуноокрашивание всего препарата (с небольшими модификациями) с использованием тех же реагентов после удаления мозговых оболочек 43 .
DiI Трассировка корково-спинномозгового тракта
DiI (1,1′-диоктадецил-3,3,3′,3′-тетраметилиндокарбоцианина перхлорат; Molecular Probes), растворенный в диметилформамиде, вводили в моторную кору новорожденных мышей с помощью использование стеклянных микропипеток. Мышей фиксировали перфузией 4% PFA/PBS примерно через 10 часов после инъекции. Препарированный мозг и срезы вибратома (толщиной 100 мкм) наблюдали и фотографировали с использованием флуоресцентного стереоскопического микроскопа (MZ FL III; Leica) и флуоресцентного микроскопа (Axioplan2; Zeiss) соответственно.
На месте Гибридизация Гибридизацию in situ проводили, как описано ранее 44 . Вкратце, криостатные срезы толщиной 10 мкм гибридизовали с 1 мкг/мл меченого дигоксигенином (DIG) антисмыслового РНК-зонда при 65 °C в течение 16 часов. После промывания предметные стекла инкубировали с антителом против DIG, конъюгированным со щелочной фосфатазой (Roche), при 4°C в течение 16 часов. Сигналы регистрировали с использованием пурпурного BM (Roche Diagnostics) в присутствии 2 мМ левамизола (Sigma) при комнатной температуре в течение 3–5 дней.
Сигналы регистрировали с использованием пурпурного BM (Roche Diagnostics) в присутствии 2 мМ левамизола (Sigma) при комнатной температуре в течение 3–5 дней.
Электропорация in utero выполнялась, как описано ранее 44 . кДНК субклонировали в вектор pCX или pEF-BOS 16,17 . Раствор ДНК (2,0–2,5 мкл), содержащий в общей сложности 600 нМ экспрессионных конструкций, вводили в латеральный желудочек мышиных эмбрионов E12.5 или E13.0. Пять прямоугольных электрических импульсов (35 В, длительность 50 мс, 1 импульс/с) подавали с помощью электропоратора (CUY21; Nepa Gene) и 3-мм электрода (CUY650P3; Nepa Gene).
Плазмидные конструкции для электропорации
Плазмиды, использованные в этом исследовании, были получены следующим образом. EGFP был получен из pEGFP-N3 (Clontech). Ранее были описаны крысы Sulf1 ( SulfFP1 ) и Sulf2 ( SulfFP2 ) 19,45 .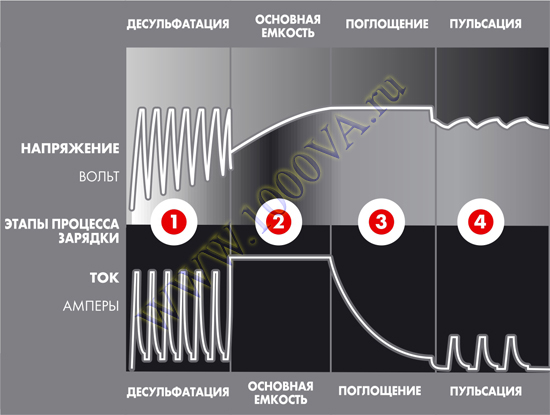 Точковую мутацию в Sulf1 ( C87A ) вводили с помощью ПЦР. кДНК мыши Slit1 (BC062091), Sema3e (ИЗОБРАЖЕНИЕ:5357516), Sema4d (ИЗОБРАЖЕНИЕ:6509473), Sema4g (ИЗОБРАЖЕНИЕ: 6395010), Sema5b (ИЗОБРАЖЕНИЕ: 5719939) и Efnb2 (ИЗОБРАЖЕНИЕ: 6827408) были получены из коллекции клонов консорциума IMAGE. Мыши Slit2 (G730002D07) и Sema6b (G730036J03) были получены от RIKEN Mouse FANTOM Clones (DNAFORM). Поскольку клоны Slit1 и Slit2 содержали короткие делеции, неправильные последовательности были заменены правильными последовательностями, которые были амплифицированы с помощью ОТ-ПЦР с последующим подтверждением последовательности. Крыса 9кДНК 0287 Robo1 и Robo2 амплифицировали с помощью ОТ-ПЦР и определяли их целые последовательности, чтобы подтвердить, что они содержат правильные последовательности.
Точковую мутацию в Sulf1 ( C87A ) вводили с помощью ПЦР. кДНК мыши Slit1 (BC062091), Sema3e (ИЗОБРАЖЕНИЕ:5357516), Sema4d (ИЗОБРАЖЕНИЕ:6509473), Sema4g (ИЗОБРАЖЕНИЕ: 6395010), Sema5b (ИЗОБРАЖЕНИЕ: 5719939) и Efnb2 (ИЗОБРАЖЕНИЕ: 6827408) были получены из коллекции клонов консорциума IMAGE. Мыши Slit2 (G730002D07) и Sema6b (G730036J03) были получены от RIKEN Mouse FANTOM Clones (DNAFORM). Поскольку клоны Slit1 и Slit2 содержали короткие делеции, неправильные последовательности были заменены правильными последовательностями, которые были амплифицированы с помощью ОТ-ПЦР с последующим подтверждением последовательности. Крыса 9кДНК 0287 Robo1 и Robo2 амплифицировали с помощью ОТ-ПЦР и определяли их целые последовательности, чтобы подтвердить, что они содержат правильные последовательности.
Sulf1 был помечен пептидом FLAG (DYKDDDDK) или пептидом Myc (EQKLISEEDL) плюс метка 6xHis на его С-конце.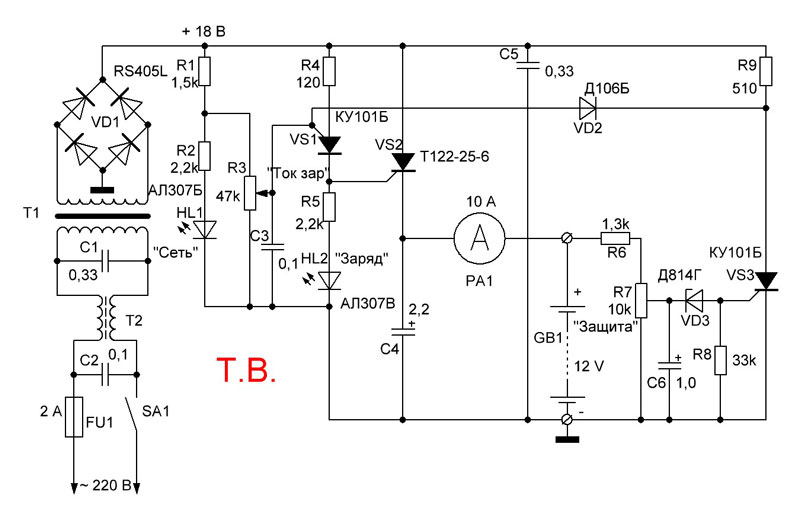 Sulf2 был помечен пептидом Myc на его С-конце. кДНК Sulf субклонировали в вектор pCX 16 и вектор pEF-BOS 17 . Для экспериментов по спасению pCX- Sulf1 -FLAG, pCX- Sulf2 -Myc, pEF-BOS- Sulf1 -FLAG и pEF-BOS- Sulf2 -Myc; для простоты они обозначены в тексте как pCX- Sulf1 , pCX- Sulf2 , pEF-BOS- Sulf1 и pEF-BOS- Sulf2 соответственно. В экспериментах, в которых исследовали локализацию белка Sulf, Sulf1 -Myc-His и Sulf2 -Myc субклонировали в вектор pCX, содержащий последовательность Козака (GCCACC АТГ ; подчеркивание — инициирующий кодон), сигнальная последовательность из гена CD8A человека (ALPVTALLLPLALLLHAARP), пептид FLAG и метка 6xHis. Sulf1 и Sulf2 присоединены к вышеуказанной последовательности с позиций 20-й и 25-й аминокислот соответственно (оба являются N-концами зрелого белка, предсказанного алгоритмом SignalP 3.0 [http://www.cbs.dtu.dk /services/SignalP/]).
Sulf2 был помечен пептидом Myc на его С-конце. кДНК Sulf субклонировали в вектор pCX 16 и вектор pEF-BOS 17 . Для экспериментов по спасению pCX- Sulf1 -FLAG, pCX- Sulf2 -Myc, pEF-BOS- Sulf1 -FLAG и pEF-BOS- Sulf2 -Myc; для простоты они обозначены в тексте как pCX- Sulf1 , pCX- Sulf2 , pEF-BOS- Sulf1 и pEF-BOS- Sulf2 соответственно. В экспериментах, в которых исследовали локализацию белка Sulf, Sulf1 -Myc-His и Sulf2 -Myc субклонировали в вектор pCX, содержащий последовательность Козака (GCCACC АТГ ; подчеркивание — инициирующий кодон), сигнальная последовательность из гена CD8A человека (ALPVTALLLPLALLLHAARP), пептид FLAG и метка 6xHis. Sulf1 и Sulf2 присоединены к вышеуказанной последовательности с позиций 20-й и 25-й аминокислот соответственно (оба являются N-концами зрелого белка, предсказанного алгоритмом SignalP 3.0 [http://www.cbs.dtu.dk /services/SignalP/]). Для простоты были созданы экспрессионные конструкции pCX-Kozak-SS-FLAG-His- Sulf1 -Myc-His и pCX-Kozak-SS-FLAG-His- Sulf2 -Myc обозначаются в тексте как pCX-FLAG- Sulf1 и pCX-FLAG- Sulf2 соответственно.
Для простоты были созданы экспрессионные конструкции pCX-Kozak-SS-FLAG-His- Sulf1 -Myc-His и pCX-Kozak-SS-FLAG-His- Sulf2 -Myc обозначаются в тексте как pCX-FLAG- Sulf1 и pCX-FLAG- Sulf2 соответственно.
The mouse cDNAs Slit1 , Slit2 , Sema3e , Sema4d , Sema4g , Sema5b , Sema6b , and Efnb2 were subcloned into a pCX vector (and a pEF-BOS vector для Slits ), которые содержали последовательность Козака, сигнальную последовательность из человеческого ген CD8A , пептид FLAG и метка 6xHis. Slit1, Slit2, Sema3E, Sema4D, Sema4G, Sema5B, Sema6B и EphrinB2 были подключены к вышеуказанной последовательности с позиций 33 rd , 26 th , 26 th , 24 th
, 1 4 , 27 th , 17 th и 30 th аминокислот соответственно (все являются N-концами зрелого белка, предсказанного алгоритмом SignalP 3. 0). Для простоты они обозначены в тексте как pCX-9.0287 SLIT1 , PCX- SLIT2 , PCX- SEMA3E , PCX- SEMA4D , PCX- SEMA4G , PCX- SEMA5B 9028, PCX-, PCX- SEMA5B 9028, PCX-, PCX-. В экспериментах по связыванию in vitro Robo2-Fc крысиный Slit2, меченный последовательностью HA (YPYDVPDYA), был субклонирован в вектор pCEP4 (Invitrogen), содержащий последовательность Kozak, сигнальную последовательность из человеческого CD8A гена , пептид FLAG. и тег 6xHis.
0). Для простоты они обозначены в тексте как pCX-9.0287 SLIT1 , PCX- SLIT2 , PCX- SEMA3E , PCX- SEMA4D , PCX- SEMA4G , PCX- SEMA5B 9028, PCX-, PCX- SEMA5B 9028, PCX-, PCX-. В экспериментах по связыванию in vitro Robo2-Fc крысиный Slit2, меченный последовательностью HA (YPYDVPDYA), был субклонирован в вектор pCEP4 (Invitrogen), содержащий последовательность Kozak, сигнальную последовательность из человеческого CD8A гена , пептид FLAG. и тег 6xHis.Анализ ЖХ-МС/МС
Анализ методом жидкостной хроматографии с ионной ловушкой (ЖХ-МС/МС) проводили, как описано ранее 46 . Вкратце, образцы разделяли с помощью SDS-PAGE и гель разрезали на 15 частей. Кусочки геля повторно пропитывали 25 мМ бикарбонатом триэтиламмония (TEAB), pH 8,0, содержащим 50% ацетонитрила, в течение 30 мин. После сушки в концентраторе Savant Speed-Vac (Thermo Fisher Scientific) гель инкубировали в 25 мМ TEAB, pH 8,0, содержащем 75–150 нг модифицированного трипсина (Roche Diagnostics), при 37 °C в течение 16–20 ч. Раствор дважды экстрагировали 100–300 мкл 0,1% трифторуксусной кислоты, содержащей 60% ацетонитрила. Эти 2 экстракта объединяли, сушили в концентраторе Speed-Vac и хранили при температуре -80 °C до анализа. Образец ресуспендировали в 0,1% муравьиной кислоте, содержащей 2% ацетонитрила, и наносили на систему ВЭЖХ DiNa (KYA Technologies Corporation). Использовали капиллярную колонку с обращенной фазой (Develosil ODS-HG5, внутренний диаметр 0,075 мм × 150 мм; Nomura Chemical) при скорости потока 200 или 300 нл/мин с линейным градиентом ацетонитрила 4–80%. Элюированные пептиды определяли непосредственно с помощью масс-спектрометра с ионной ловушкой (LXQ; Thermo Fisher Scientific) при напряжении распыления 1,9.кВ и энергии столкновения 35%. Метод массового сбора данных состоял из 1 полного сканирования МС с последующим сканированием МС/МС наиболее распространенных ионов-предшественников из сканирования обзора. Динамическое исключение для спектров МС/МС было установлено на 30 с. Данные анализировали с помощью программного обеспечения BioWorks (Thermo Fisher Scientific) и Mascot (Matrix Science).
Раствор дважды экстрагировали 100–300 мкл 0,1% трифторуксусной кислоты, содержащей 60% ацетонитрила. Эти 2 экстракта объединяли, сушили в концентраторе Speed-Vac и хранили при температуре -80 °C до анализа. Образец ресуспендировали в 0,1% муравьиной кислоте, содержащей 2% ацетонитрила, и наносили на систему ВЭЖХ DiNa (KYA Technologies Corporation). Использовали капиллярную колонку с обращенной фазой (Develosil ODS-HG5, внутренний диаметр 0,075 мм × 150 мм; Nomura Chemical) при скорости потока 200 или 300 нл/мин с линейным градиентом ацетонитрила 4–80%. Элюированные пептиды определяли непосредственно с помощью масс-спектрометра с ионной ловушкой (LXQ; Thermo Fisher Scientific) при напряжении распыления 1,9.кВ и энергии столкновения 35%. Метод массового сбора данных состоял из 1 полного сканирования МС с последующим сканированием МС/МС наиболее распространенных ионов-предшественников из сканирования обзора. Динамическое исключение для спектров МС/МС было установлено на 30 с. Данные анализировали с помощью программного обеспечения BioWorks (Thermo Fisher Scientific) и Mascot (Matrix Science).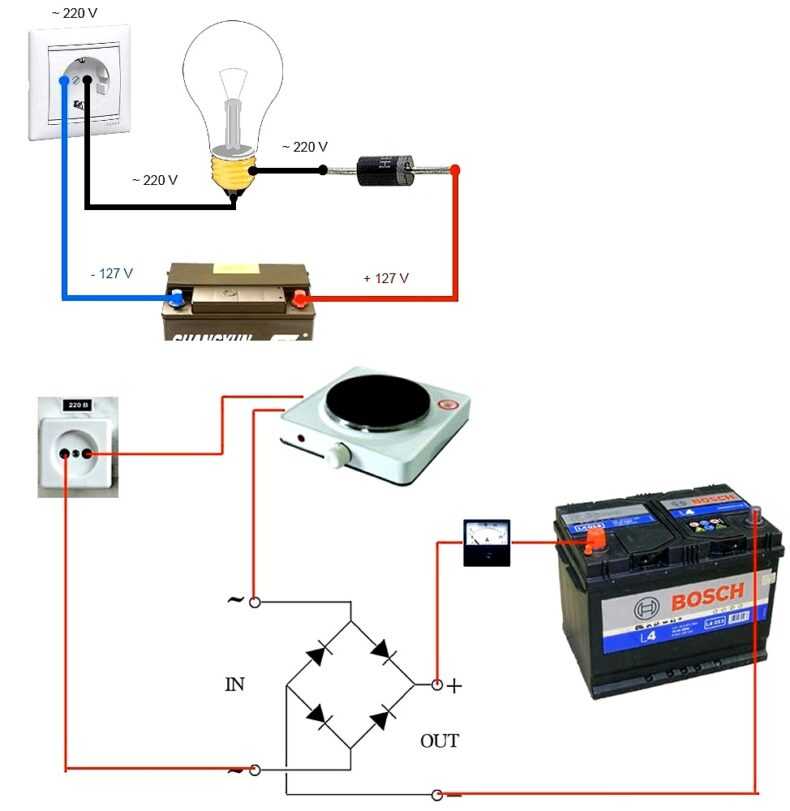
Анализ связывания Robo2-Fc
Клетки Cos-7 трансфицировали pMT21-Robo2-Fc с использованием реагента LipofectAMINE Plus (Life Technologies) или FuGene HD (Promega). После культивирования клеток в бессывороточной среде Opti-MEM I (Life Technologies) в течение 3 дней кондиционированную среду концентрировали примерно в 5 раз с использованием фильтра Amicon Ultra-15 (50k MCO; Millipore). Для in vitro , клетки 293EBNA (Life Technologies), трансфицированные pCEP4-FLAG- Slit1 или pCEP4-FLAG- Slit2 , инкубировали с Robo2-Fc в буфере PH (PBS с 1% инактивированной нагреванием нормальной козьей сыворотки). ) при комнатной температуре в течение 1 ч. После промывки клетки фиксировали 2% PFA/PBS, пермеабилизировали в PHT (PH с 0,1% Triton-X100) и инкубировали с Cy3-меченым антителом против IgG человека при комнатной температуре в течение 30 мин (1:350; Джексон ИммуноИсследования).
Для обнаружения in situ свежезамороженные срезы головы мыши E15.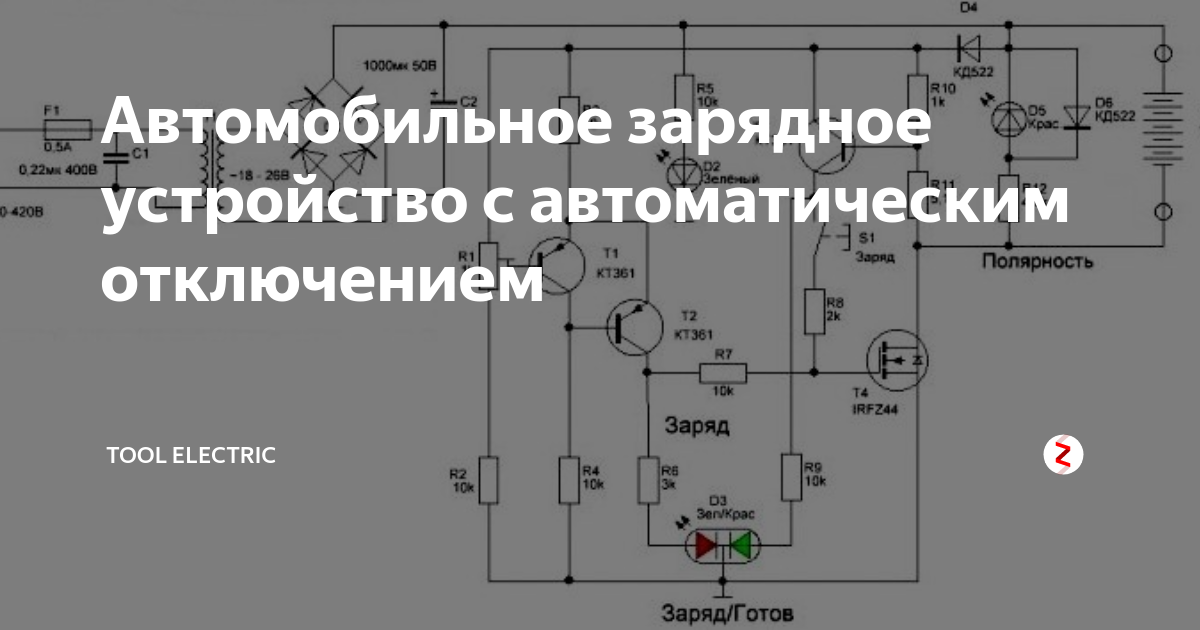 5 толщиной 10 мкм фиксировали в 1% уксусной кислоте и 95% этаноле при температуре -20 °C в течение ночи. После промывания PBS и блокирования PHT при комнатной температуре в течение 1 часа предметные стекла инкубировали с Robo2-Fc (концентрация примерно в 2,5 раза) при 4°C в течение ночи. Затем предметные стекла промывали PHT и инкубировали с биотин-SP-конъюгированным антителом против IgG человека (1:50; Jackson ImmunoResearch) при комнатной температуре в течение 45 мин, а затем со стрептавидином, конъюгированным с Alexa546 (1:50; Life Technologies) при комнатной температуре. комнатной температуре в течение 15 мин. В этом препарате сигнал флуоресценции электропорированного EGFP был устранен, и поэтому иммуноокрашивание не нарушалось.
5 толщиной 10 мкм фиксировали в 1% уксусной кислоте и 95% этаноле при температуре -20 °C в течение ночи. После промывания PBS и блокирования PHT при комнатной температуре в течение 1 часа предметные стекла инкубировали с Robo2-Fc (концентрация примерно в 2,5 раза) при 4°C в течение ночи. Затем предметные стекла промывали PHT и инкубировали с биотин-SP-конъюгированным антителом против IgG человека (1:50; Jackson ImmunoResearch) при комнатной температуре в течение 45 мин, а затем со стрептавидином, конъюгированным с Alexa546 (1:50; Life Technologies) при комнатной температуре. комнатной температуре в течение 15 мин. В этом препарате сигнал флуоресценции электропорированного EGFP был устранен, и поэтому иммуноокрашивание не нарушалось.
Серия флуоресцентных изображений z-stack (1024 × 1024 пикселей) была получена с использованием лазерного сканирующего микроскопа LSM510 с 10-кратным объективом (Carl Zeiss). Для количественного сравнения интенсивности флуоресценции образцов использовали одни и те же параметры (отверстие 80,3 мкм, оптимальный интервал 6,54 мкм, усиление детектора 1000, смещение усилителя -0,1, усиление усилителя 1, скорость сканирования 9, среднее число, 2) использовались для всех сканирований. Для каждого экспериментального условия использовали три секции. В каждом срезе для измерения выбирался один оптический срез с наибольшей интенсивностью. Прослеживали контур поверхности мозга и измеряли интенсивность флуоресценции в прослеживаемой области.
Для каждого экспериментального условия использовали три секции. В каждом срезе для измерения выбирался один оптический срез с наибольшей интенсивностью. Прослеживали контур поверхности мозга и измеряли интенсивность флуоресценции в прослеживаемой области.
Вестерн-блот-анализ
Мозговые оболочки или мозг, вырезанные из областей гипоталамуса и среднего мозга эмбрионов мыши E15.5, гомогенизировали в буфере для образцов (62,5 мМ трис-HCl, pH 6,8, 2% SDS, 5% сахарозы, 0,01% бромфенола). синий, 10% 2-меркаптоэтанол). Основными используемыми антителами были анти-Slit2 (1:200, G-19; Santa Cruz Biotechnology), анти-актин (1:1000; Sigma) и анти-ламинин (1:1000; Sigma). В качестве вторичных антител использовали конъюгированные с пероксидазой антикозьи или кроличьи IgG (1:2500; Jackson ImmunoResearch). Сигналы детектировали с использованием системы обнаружения вестерн-блоттинга ECL Plus (GE). Данные контрольного эксперимента, подтвердившего специфичность анти-Slit2-антитела (G-19) показаны на дополнительном рисунке S6.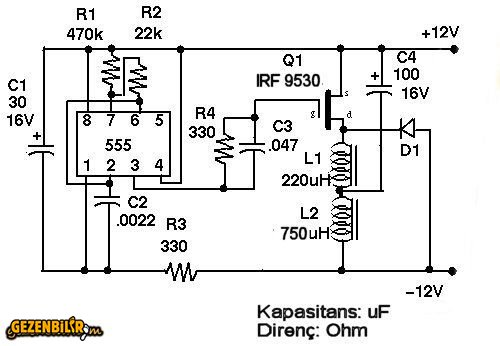
Статистика
Статистические методы не использовались для предварительного определения размера выборки, но наши размеры выборки аналогичны тем, которые обычно используются в этой области. Статистический анализ данных связывания Robo2-Fc и анализа дисахаридов проводили с помощью ANOVA с апостериорными тестами Тьюки-Крамера и Бонферрони, соответственно. Точный критерий Фишера использовали для анализа частоты восстановления фенотипа у эмбрионов, подвергшихся электропорации pCX- Robo2-Fc . Стьюдентный критерий Уэлча и парный t-критерий использовались для анализа средней интенсивности флуоресцентного сигнала, ширины пучков аксонов и площади положительной области нейрофиламента (подробности анализа описаны в дополнительной таблице 1).
Доступность данных
Данные, подтверждающие результаты этого исследования, можно получить у соответствующего автора по обоснованному запросу.
Ссылки
- «>
Холт, К. Э. и Диксон, Б. Дж. Сахарные коды для аксонов? Нейрон 46 , 169–172 (2005).
КАС Статья пабмед ПабМед Центральный Google ученый
Бишоп, Дж. Р., Шукс, М. и Эско, Дж. Д. Гепарансульфатные протеогликаны тонко настраивают физиологию млекопитающих. Природа 446 , 1030–1037 (2007).
ОБЪЯВЛЕНИЕ КАС Статья пабмед Google ученый
Масу, М. Протеогликаны и наведение аксонов: новые отношения между старыми партнерами.
 Дж. Нейрохим. 139 , 58–75 (2016).
Дж. Нейрохим. 139 , 58–75 (2016).КАС Статья пабмед Google ученый
Ламанна, В. К. и др. . Гепараном – загадка кодирования и расшифровки сульфатирования гепарансульфата. J. Биотехнология. 129 , 290–307 (2007).
КАС Статья пабмед Google ученый
Эль Масри, Р., Сеффух, А., Лортат-Джейкоб, Х. и Вивес, Р. Р. «Вход и выход» глюкозамин-6-О-сульфатирования: 6-е значение гепарансульфата. Гликоконж . Дж . под давлением.
Ламанна, В.К. и др. . Гепарансульфат 6-О-эндосульфатазы: дискретные Активность in vivo и функциональная кооперация. Биохим. Дж. 400 , 63–73 (2006).
КАС Статья пабмед ПабМед Центральный Google ученый
«>Холст, Ч.Р. и др. . Секретируемые сульфатазы Sulf1 и Sulf2 играют перекрывающиеся, но существенные роли в выживании новорожденных мышей. PLoS Один 2 , e575 (2007 г.).
ОБЪЯВЛЕНИЕ Статья пабмед ПабМед Центральный КАС Google ученый
Langsdorf, A., Do, A.T., Kusche-Gullberg, M., Emerson, C.P. Jr. & Ai, X. Сульфаты являются регуляторами передачи сигналов фактора роста для дифференцировки сателлитных клеток и регенерации мышц. Дев. биол. 311 , 464–477 (2007).

КАС Статья пабмед Google ученый
Рацка А. и др. . Избыточная функция гепарансульфат-6-О-эндосульфатаз Sulf1 и Sulf2 во время развития скелета. Дев. Дин. 237 , 339–353 (2008).
КАС Статья пабмед Google ученый
Калус И. и др. . Дифференциальное участие внеклеточных 6-O-эндосульфатаз Sulf1 и Sulf2 в развитии мозга, нейрональной и поведенческой пластичности. Дж. Сотовый. Мол. Мед. 13 , 4505–4521 (2009).
КАС Статья пабмед Google ученый
Калус И. и др. . Sulf1 и Sulf2 по-разному модулируют сульфатирование гепарансульфата и протеогликана во время постнатального развития мозжечка: доказательства нейропротекторной функции и функции, способствующей росту нейритов.
 ПлоС Один 10 , e0139853 (2015).
ПлоС Один 10 , e0139853 (2015).Артикул пабмед ПабМед Центральный КАС Google ученый
Канти, А. Дж. и Мерфи, М. Молекулярные механизмы направления аксонов в развивающемся корково-спинномозговом тракте. Прог. Нейробиол. 85 , 214–235 (2008).
КАС Статья пабмед Google ученый
Лейва-Диас, Э. и Лопес-Бендито, Г. В коре и вне ее: развитие основных связей переднего мозга. Неврология 254 , 26–44 (2013).
Артикул пабмед КАС Google ученый
Нива, Х., Ямамура, К. и Миядзаки, Дж. Эффективная селекция трансфектантов с высокой экспрессией с помощью нового эукариотического вектора.
 Джин 108 , 193–199 (1991).
Джин 108 , 193–199 (1991).КАС Статья пабмед Google ученый
Mizushima, S. & Nagata, S. pEF-BOS, мощный вектор экспрессии млекопитающих. Рез. нуклеиновой кислоты. 18 , 5322 (1990).
КАС Статья пабмед ПабМед Центральный Google ученый
Куруп, С. и др. . Характеристика антигепарансульфатного фагового дисплея антител AO4B08 и HS4E4. J. Biol. хим. 282 , 21032–21042 (2007 г.).
КАС Статья пабмед Google ученый
Нагамин С. и др. . Органоспецифические паттерны сульфатации гепарансульфата, генерируемого внеклеточными сульфатазами Sulf1 и Sulf2 у мышей. J.
 Biol. хим. 287 , 9579–9590 (2012).
Biol. хим. 287 , 9579–9590 (2012).КАС Статья пабмед ПабМед Центральный Google ученый
Шу, Т. и Ричарддс, Л.Дж. Направление корковых аксонов глиальным клином во время развития мозолистого тела. J. Neurosci. 21 , 2749–2758 (2001).
КАС пабмед Google ученый
Багри, А. и др. . Щелевые белки предотвращают пересечение срединной линии и определяют дорсо-вентральное положение основных путей аксонов в переднем мозге млекопитающих. Нейрон 33 , 233–248 (2002).
КАС Статья пабмед Google ученый
Ronca, F., Andersen, J.S., Paech, V. & Margolis, R.U. Характеристика взаимодействия белка Slit с глипиканом-1.
 Дж. Биол. хим. 276 , 29141–29147 (2001).
Дж. Биол. хим. 276 , 29141–29147 (2001).КАС Статья пабмед Google ученый
Шипп, Э. Л. и Хси-Уилсон, Л. К. Профилирование специфики сульфатирования взаимодействий гликозаминогликанов с факторами роста и хемотаксическими белками с использованием микрочипов. Хим. биол. 14 , 195–208 (2007).
КАС Статья пабмед Google ученый
Броуз, К. и др. . Белки Slit связываются с рецепторами Robo и играют эволюционно законсервированную роль в отталкивающем ведении аксонов. Сотовый 96 , 795–806 (1999).
КАС Статья пабмед Google ученый
Ву, В. и др. . Направленное управление миграцией нейронов в обонятельной системе с помощью белка Slit.
 Природа 400 , 331–336 (1999).
Природа 400 , 331–336 (1999).ОБЪЯВЛЕНИЕ КАС Статья пабмед ПабМед Центральный Google ученый
Уитфорд, К. Л. и др. . Регуляция развития корковых дендритов с помощью взаимодействия Slit-Robo. Нейрон 33 , 47–61 (2002).
КАС Статья пабмед Google ученый
Лопес-Бендито, Г. и др. . Robo1 и Robo2 сотрудничают, чтобы контролировать направление основных аксональных трактов в переднем мозге млекопитающих. J. Neurosci. 27 , 3395–3407 (2007).
Артикул пабмед КАС Google ученый
Инатани, М., Ири, Ф., Пламп, А.С., Тессье-Лавин, М. и Ямагучи, Ю. Морфогенез мозга млекопитающих и направление аксонов по срединной линии требуют гепарансульфата.
 Наука 302 , 1044–1046 (2003).
Наука 302 , 1044–1046 (2003).ОБЪЯВЛЕНИЕ КАС Статья пабмед Google ученый
Ли, Дж. С. и др. . Сортировка аксонов в зрительном тракте требует синтеза HSPG с помощью ext2 (dackel) и extl3 (boxer). Нейрон 44 , 947–960 (2004).
КАС Статья пабмед Google ученый
Ли, Дж. С. и Чиен, К. Б. Когда аксоны направляются сахарами: выводы из мутантов гепарансульфата протеогликана. Нац. Преподобный Жене. 5 , 923–935 (2004).
КАС Статья пабмед Google ученый
Bülow, H. E. & Hobert, O. Дифференциальные сульфатации и эпимеризация определяют специфичность гепарансульфата в развитии нервной системы.
 Нейрон 41 , 723–736 (2004).
Нейрон 41 , 723–736 (2004).Артикул пабмед Google ученый
Бюлов Х. Э. и Хоберт О. Молекулярное разнообразие гликозаминогликанов определяет развитие животных. год. Преподобный Cell Dev. биол. 22 , 375–407 (2006).
Артикул пабмед КАС Google ученый
Pratt, T., Conway, C.D., Tian, N.M., Price, D.J. & Mason, J.O. Паттерны сульфатации гепарана, генерируемые специфическими ферментами гепарансульфотрансфераз, направляют различные аспекты направления аксонов сетчатки в зрительном перекресте. J. Neurosci. 26 , 6911–6923 (2006).
КАС Статья пабмед Google ученый
Bülow, H.E. и др.
 . Модификации внеклеточного сахара предоставляют поучительную и специфичную для клеток информацию для выбора направления аксонов. Курс. биол. 18 , 1978–1985 (2008).
. Модификации внеклеточного сахара предоставляют поучительную и специфичную для клеток информацию для выбора направления аксонов. Курс. биол. 18 , 1978–1985 (2008).Артикул пабмед ПабМед Центральный КАС Google ученый
Conway, CD и др. . Модификации сахара гепарансульфатом опосредуют функции щелей и др. факторов, необходимых для развития спайки переднего мозга мышей. J. Neurosci. 31 , 1955–1970 (2011).
КАС Статья пабмед Google ученый
Клегг, Дж. М. и др. . Гепарансульфотрансферазы Hs6st1 и Hs2st контролируют Erk в отношении развития мозолистого тела мышей. J. Neurosci. 34 , 2389–2401 (2014).
КАС Статья пабмед ПабМед Центральный Google ученый
«>Райт, К. М. и др. . Дистрогликан организует локализацию сигнала направления аксона и поиск пути аксона. Нейрон 76 , 931–944 (2012).
КАС Статья пабмед ПабМед Центральный Google ученый
Варадараджан, С. Г. и др. . Нетрин1, продуцируемый нейронными предшественниками, а не клетками пластины пола, необходим для направления аксонов в спинной мозг. Нейрон 94 , 790–799 (2017).
КАС Статья пабмед Google ученый
«>Lau, E. & Margolis, R.U. Ингибиторы взаимодействия слитых белков с гепарансульфатным протеогликаном глипиканом-1: потенциальные средства для лечения травм спинного мозга. клин. Эксп. Фармакол. Физиол. 37 , 417–421 (2010).
КАС Статья пабмед Google ученый
Tuckett, F. & Morris-Kay, G. Alcian Blue Окрашивание гликозаминогликанов в эмбриональном материале: влияние различных фиксаторов. Гистохим. Дж. 20 , 174–182 (1988).
КАС Статья пабмед Google ученый
«>Окада Т., Кейно-Масу К. и Масу М. Миграция и нуклеогенез премозжечковых нейронов мыши, визуализированные с помощью in utero электропорации гена зеленого флуоресцентного белка. Неврологи. Рез. 57 , 40–49 (2007).
КАС Статья пабмед Google ученый
Охто, Т. и др. . Идентификация новой нелизосомальной сульфатазы, экспрессируемой в пластинке дна, сосудистых сплетениях и хрящах. Гены Клетки 7 , 173–185 (2002).
КАС Статья пабмед Google ученый
«>
Перримон, Н. и Бернфилд, М. Особенности гепарансульфатных протеогликанов в процессах развития. Природа 404 , 725–728 (2000).
ОБЪЯВЛЕНИЕ КАС Статья пабмед Google ученый
Ай, Х. и др. . SULF1 и SULF2 регулируют опосредованную гепарансульфатом передачу сигналов GDNF для иннервации пищевода. Разработка 134 , 3327–3338 (2007).
КАС Статья пабмед Google ученый
Сяо Т. и др. . Сборка специфичных для пластинки нейронных соединений с помощью щели, связанной с коллагеном IV типа. Сотовый 146 , 164–176 (2011).
КАС Статья пабмед ПабМед Центральный Google ученый
Доминики, К. и др. . Нетрин-1, полученный из пластинки дна, необязателен для направления комиссуральных аксонов. Природа 545 , 350–354 (2017).
ОБЪЯВЛЕНИЕ КАС Статья пабмед ПабМед Центральный Google ученый
Танигучи, М. и др. . Нарушение гена семафорина III/D вызывает серьезную аномалию в проекции периферического нерва. Нейрон 19 , 519–530 (1997).
КАС Статья пабмед Google ученый
Каметани, Ф. и др. . Идентификация сайтов фосфорилирования казеинкиназы-1 на TDP-43. Биохим. Биофиз. Рез. коммун. 382 , 405–409 (2009).
КАС Статья Google ученый
Ссылки для скачивания
Предоставление сервисных решений по управлению аккумуляторными батареями
Во всем мире используются свинцово-кислотные аккумуляторные батареи для запуска автомобильных двигателей стоимостью около 60 миллиардов долларов. Каждому из них суждено проработать определенное количество лет, а затем перестать работать. Потребитель обязан в силу владения автомобилем покупать сменные аккумуляторы. Потребитель — неохотный покупатель, который, скорее всего, купит по цене, что, в свою очередь, ставит производителей аккумуляторов под коммерческое давление. Скорее всего, поэтому средний свинцово-кислотный автомобильный аккумулятор имеет относительно скромный срок службы.
Реклама стоимостью в миллионы долларов настаивает на том, что сульфатация является основной причиной отказа батареи. Это легло в основу того, что многие люди считают правдой. Мы изучили весь спектр зарегистрированных ноу-хау на предмет продления срока службы свинцово-кислотных аккумуляторов. Мы прочитали множество патентов, статей, документов, отчетов, комментариев, писем и рекламных объявлений и провели сотни тестов. Это то, что мы нашли.
В развитых странах насчитывается от 500 до 800 автомобилей на 1000 человек населения, другими словами, почти одна свинцово-кислотная батарея на человека. Почти четыреста миллионов батарей. Розничные продавцы автозапчастей по праву должны продавать огромные объемы импульсных десульфататоров. Некоторые производители продукции для импульсной десульфатации должны были стать достаточно крупными, чтобы стать публичными предприятиями. Но ничего не произошло. Импульсные десульфаторы продаются сейчас так же, как и двадцать лет назад, когда они впервые появились, поштучно и по паре, преимущественно мелкими специалистами по доставке по почте.
Сначала нам очень нравилась концепция импульсной сульфатации, и мы думали, что поняли ее. Мы были очень удивлены при поиске в патентных базах данных по всему миру, обнаружив 61 патент, натянутый, как жемчуг на ожерелье во времени, — все они были выпущены после 1991 года — последовательно описывая каждое предыдущее изобретение как ошибочное, а затем каждый, в свою очередь, предлагал принципиально иная пульсирующая техника. Электрические, а также магнитные, механические и ультразвуковые — от интенсивных импульсов длительностью всего лишь наносекунды — импульсов длительностью миллисекунды — прямоугольная волна включена-выключена — прямоугольная волна включена и треугольная выключена, с различными интервалами. В некоторых конструкциях используется сама батарея для питания импульсного блока, чтобы посылать импульсы обратно самому себе — довольно иррационально рискуя разрядить батарею до тех пор, пока она не сможет выполнять свою намеченную задачу. Пульсация при различных состояниях заряда, пульсация с различной частотой, устойчивая пульсация, структурированная пульсация, резонансная пульсация.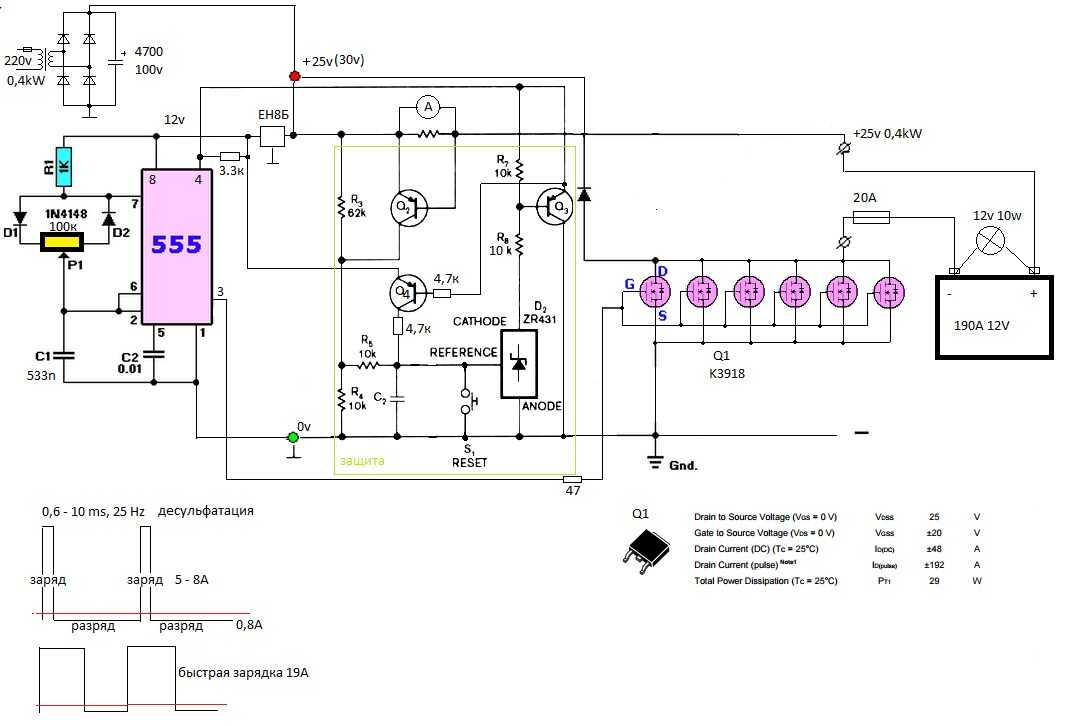 Некоторые утверждают, что лучше всего пульсировать на частоте кристаллического резонанса серы 3,26 МГц. То, что они увидели, это собственный резонанс разъемов батареи, сделали предположение. В свинцово-кислотном аккумуляторе нет серы, только сульфат водорода (серная кислота) и сульфат свинца (сульфат свинца).
Некоторые утверждают, что лучше всего пульсировать на частоте кристаллического резонанса серы 3,26 МГц. То, что они увидели, это собственный резонанс разъемов батареи, сделали предположение. В свинцово-кислотном аккумуляторе нет серы, только сульфат водорода (серная кислота) и сульфат свинца (сульфат свинца).
Импульсная зарядка — старая технология. Импульсная терапия появилась относительно недавно. Уилфорду Б. Беркетту ошибочно приписывают изобретение импульсного омоложения батареи в конце 1960-х — начале 1970-х годов. Он использовал импульсы для быстрой зарядки аккумуляторов. Омоложение батареи или десульфатация с помощью пульсации была изобретена Карлом Эдвардом Гали (1928-2009) (разработчиком микросхем на пенсии, Texas Instruments), патент США 5 063 341, подана 16 октября 1990 г., выдана 5 ноября 1991 г. [Нажмите, чтобы просмотреть первый патент, 1. USPTO: патент США 5 063 341 или 2. Google: патент США 5 063 341 и повторно рассмотренный патент, 3. US Re. 35643, 28 октября 1997 г. pdf. ] . Его патенты, очевидно, были не очень сильными. Импульсная технология десульфатации свинцово-кислотных аккумуляторов быстро начала привлекать большое количество энтузиастов, производителей и дистрибьюторов по всему миру.
pdf. ] . Его патенты, очевидно, были не очень сильными. Импульсная технология десульфатации свинцово-кислотных аккумуляторов быстро начала привлекать большое количество энтузиастов, производителей и дистрибьюторов по всему миру.
Разнообразие последующих импульсных патентов обеспечивает удобный и удивительно точный способ определения истинного уровня понимания технологии. Базы данных показывают, что предмет патента на импульсную технологию необычайно широко разбросан, подтверждая, что с этой технологией определенно что-то не так.
Мы считаем весьма знаменательным тот факт, что пульсация начала набирать популярность в начале 1990-х годов, только после того, как все основные производители аккумуляторов представили автомобильные аккумуляторы, не требующие особого ухода. Эти батареи имеют сетки из свинцово-кальциевого сплава. Свинцово-кальциевые батареи в подавляющем большинстве случаев выходят из строя из-за того, что известно в торговле как «пассивация» или «разомкнутая цепь». Технологи аккумуляторов описали это как «эффект отсутствия сурьмы».
Технологи аккумуляторов описали это как «эффект отсутствия сурьмы».
Свинцово-кальциевый сплав образует ультратонкий, очень плохо проводящий тетрагональный слой оксида свинца (альфа-PbO) на поверхностях сеток положительных пластин с течением времени, в результате чего положительный активный материал в положительных пластинах остается изолированным от несущей положительная сетчатая структура. Слой PbO начинается с PbSO4 и формируется с течением времени в результате реакций, приводящих к повышению pH в границах соединения. (См. ссылку внизу страницы.) Производители аккумуляторов используют олово для контроля этого оксидного слоя. Это далеко не просто. Добавление в сплав более 1,5 % олова снижает эффект пассивации – критически важно, что при 0,6 % олово фактически ухудшает эффект. Олово дорого, поэтому используется как можно меньше, что приводит к непредсказуемым результатам. Есть более 90 патентов, описывающих олово, а также другие металлы, сплавленные с положительными сетками или нанесенные на них, — предполагать, что это тоже является очень проблематичной технологией.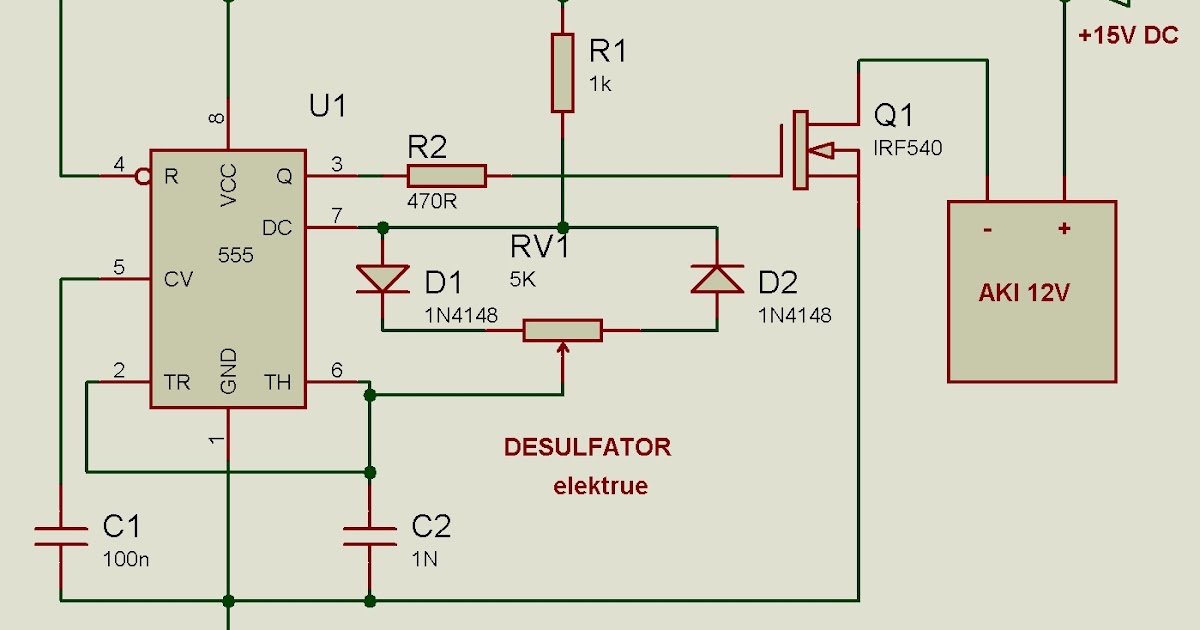 Серебро еще более выгодно, но мучительно дорого. До свинцово-кальциевого сплава предпочтительным был сплав свинца-сурьмы. Свинцово-сурьмяные всегда были в этом плане абсолютно на 100% безотказными.
Серебро еще более выгодно, но мучительно дорого. До свинцово-кальциевого сплава предпочтительным был сплав свинца-сурьмы. Свинцово-сурьмяные всегда были в этом плане абсолютно на 100% безотказными.
Тогда зачем менять? Очень хороший вопрос. В свинцово-кальциевых батареях используется в восемь раз меньше воды, чем в свинцово-сурьмяных, к тому же они могут быть полностью необслуживаемыми благодаря технологии рекомбинации водорода и кислорода. Стоимость свинцово-кальциевых сеток ниже свинцово-сурьмяных. Производители аккумуляторов очень быстро играют в «следуй за лидером», чтобы убедиться, что между аккумуляторами мало выбора. Очевидно, что отсутствие необходимости в обслуживании воспринимается как важное значение, а разумное время автономной работы — в меньшей степени. Эти Пиноккио быстро описывают AGM и Gel как обеспечивающие «оптимальную производительность» и «превосходную глубокую цикличность», но предпочитают не раскрывать фактические цифры срока службы при циклировании. Добро пожаловать в общество одноразовых!
Проблема заключается в том, что аккумулятор отказывается запускать двигатель. Затем, когда аккумулятор ставится на зарядку, его напряжение почти сразу повышается, как будто он уже полностью заряжен. Все внешние признаки (в том числе низкий SG в залитых батареях) идентичны сульфатации, но это точно не сульфатация. Применение сильных высокочастотных импульсов, импульсов с коротким временем нарастания, действующих в основном в том же направлении, что и зарядный ток батареи, разрушает сверхтонкий оксидный изолирующий слой и, таким образом, восстанавливает емкость батареи в ампер-часах до обслуживаемый уровень.
Затем, когда аккумулятор ставится на зарядку, его напряжение почти сразу повышается, как будто он уже полностью заряжен. Все внешние признаки (в том числе низкий SG в залитых батареях) идентичны сульфатации, но это точно не сульфатация. Применение сильных высокочастотных импульсов, импульсов с коротким временем нарастания, действующих в основном в том же направлении, что и зарядный ток батареи, разрушает сверхтонкий оксидный изолирующий слой и, таким образом, восстанавливает емкость батареи в ампер-часах до обслуживаемый уровень.
Наши исследователи провели серию экспериментов, чтобы выяснить из первых рук, какое влияние пульсация оказывает на сульфатированные аккумуляторы. Наше тестирование проводилось на элементах батареи, которые мы встроили в стеклянные контейнеры, чтобы мы могли точно видеть, от начала до конца, что происходит с пластинами батареи. Полностью заряженные, полностью разряженные и сульфатированные пластины имеют разные цвета, которые нетрудно отличить друг от друга. У нас были аккумуляторные пластины, которые бережно хранились неиспользованными в аккумуляторной кислоте в течение пяти лет. Пластины были 100% сульфатированы. Мы включили эти планшеты в наши тестовые ячейки.
У нас были аккумуляторные пластины, которые бережно хранились неиспользованными в аккумуляторной кислоте в течение пяти лет. Пластины были 100% сульфатированы. Мы включили эти планшеты в наши тестовые ячейки.
При тестировании мы использовали двухлучевой осциллограф с частотой 100 МГц и коаксиальный токовый шунт с малой индуктивностью. Острые наносекундные/микросекундные импульсы вызывали «пинг» или затухающие синусоидальные колебания. Мы внимательно рассмотрели эти колебания. Волна тока была на 90 градусов не в фазе с волной напряжения из-за резонанса индуктивности цепи и емкости цепи, показывая, что практически вся пульсирующая энергия в конечном итоге бесполезно рассеивается в проводке и сопротивлении цепи, вместо того, чтобы идти. в батарею. (В электротехнике сильного тока это известно как нулевой коэффициент мощности.) Более длительные миллисекундные импульсы создают волны тока и напряжения, которые находятся в фазе и, следовательно, гораздо более эффективны. Тестовые клетки подвергались пульсации всеми возможными способами в течение нескольких недель подряд.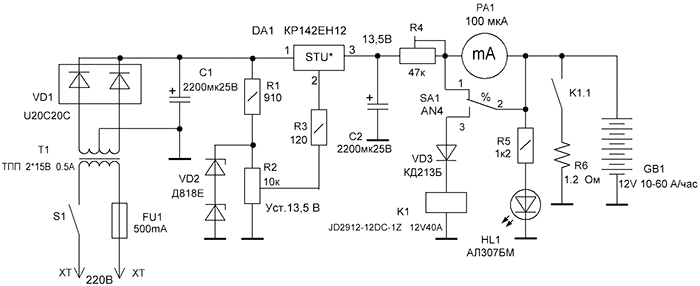 Повторяем, они не стали достаточно десульфатированными.
Повторяем, они не стали достаточно десульфатированными.
Ячейка свинцово-кислотной батареи в некоторых отношениях похожа на гальваническую ячейку. К счастью, растворимость свинца в серной кислоте настолько низка, что, когда свинцово-кислотный элемент подключается к источнику питания, он заряжается, и количество гальванического покрытия незначительно. Зарядка имеет преимущество перед гальванопокрытием, за исключением случаев, когда ячейка значительно превышает 2,6 вольта, например, когда она заряжается импульсами. Свинцово-кислотный элемент, который заряжается в импульсном режиме, становится более эффективным гальваническим элементом. Если переборщить с пульсацией, металлический свинец переместится с плюсов на минусы, позитивные сетки подвергнуться коррозии, а на негативных пластинах появятся мшистые дендриты. Гальваническое покрытие приводит к тому, что металлические нити постепенно проникают в поры сепараторов от отрицательной пластины к положительной, что приводит к короткому замыканию и преждевременному выходу элемента из строя. (См. Статью — Свинцово-кислотное и внутреннее гальваническое покрытие, фильм № 4). Импульсный режим повышает температуру батареи. Мощность, теряемая из-за внутреннего сопротивления батареи, возрастает пропорционально квадрату тока: W=I²R, умноженное на рабочий цикл. Импульсы, которые 10%-ON, 90%-OFF увеличивает потери тепла в десять раз.
(См. Статью — Свинцово-кислотное и внутреннее гальваническое покрытие, фильм № 4). Импульсный режим повышает температуру батареи. Мощность, теряемая из-за внутреннего сопротивления батареи, возрастает пропорционально квадрату тока: W=I²R, умноженное на рабочий цикл. Импульсы, которые 10%-ON, 90%-OFF увеличивает потери тепла в десять раз.
Мы не утверждаем, что пульсация вообще не работает. Средняя энергия импульсов импульсного устройства с электрическим питанием определенно может зарядить аккумулятор. Содержание энергии в импульсах индуктивного и емкостного разряда автоматически подстраивается под напряжение и силу тока батареи, и эта часть является хорошей идеей. Импульсный режим очень хорошо работает на батареях, которые «устали» и приобрели относительно мягкую форму сульфатации, рассеянной по их пластинам, и работает на батареях «разомкнутой цепи». Это определенно не работает на сильно сульфатированных аккумуляторах. Мы подвергли шесть аккумуляторов для гольф-мобилей, которые в последний раз использовались три года назад, десульфатации с использованием большого импульсного десульфатора промышленного класса. Напряжение всех шести было ниже 2 вольт. Все шесть остались сульфатированными.
Напряжение всех шести было ниже 2 вольт. Все шесть остались сульфатированными.
Сульфатация представляет собой проблему, но незначительную, затрагивающую в основном аккумуляторы автомобильного типа. Предприниматели, стремящиеся получить прибыль от продажи продуктов десульфатации, уже давно пропагандируют это как универсальную проблему, связанную со свинцово-кислотными продуктами. Это привлекает многих новичков, которые изо всех сил пытаются попасть в то, что они считают очень легкой сферой бизнеса, но обнаруживают, что зарабатывать деньги практически невозможно.
Если Том хочет продать комплект для десульфатации, а Дик готов заплатить запрашиваемую цену, это свободное предпринимательство на работе и никто не имеет права стоять на пути сделки . Если Гарри считает, что наборы для десульфатации не работают, и говорит об этом, не называя продавцов и покупателей, это свобода слова .
- Понимание аккумуляторным сообществом того, как работают свинцово-кислотные аккумуляторы, основано на многолетнем опыте, научных исследованиях, обширных испытаниях, достоверных данных и фактах —
- , но то, что сообщество аккумуляторов знает о свинцово-кислотных батареях, когда они используются пользователем, основано на воспоминаниях, интерпретациях, мнениях, анекдотах и убеждениях.

Если, как утверждается, десульфатация удаляет слой белого сульфата, который образуется на пластинах аккумулятора, то почему производители продуктов для десульфатации не предоставили надлежащих доказательств, которые легко понять и которым можно верить — одноразовый, непрерывный замедленная съемка, показывающая полностью сульфатированную батарею в прозрачном корпусе , проходящую десульфатацию и показывающую восстановление емкости?
Проблема с исследованиями, проводимыми университетами от имени корпораций, заключается в том, что они могут адаптировать свои протоколы оценки таким образом, чтобы предоставлять информацию, которая может подтверждать или опровергать утверждения, сделанные в отношении коммерческих продуктов. Остерегайтесь отзывов клиентов. Попробуйте взглянуть на ситуацию с точки зрения автора отзывов. Создается впечатление, что автор берет на себя ответственность за скрытые дефекты продукта производителя. Кто пойдет на такой риск?
Сульфатация — это термин, который вошел в обиход на заре появления свинцово-кислотных аккумуляторов. Значение этого слова расширилось и теперь подразумевает право включать и оправдывать все мыслимые причины возможного ухудшения характеристик и выхода из строя свинцово-кислотных аккумуляторов. Однако……….
Значение этого слова расширилось и теперь подразумевает право включать и оправдывать все мыслимые причины возможного ухудшения характеристик и выхода из строя свинцово-кислотных аккумуляторов. Однако……….
- Свинцово-кислотные аккумуляторы, за которыми осуществляется наилучший технический уход, регулярно доводятся до полного заряда, последовательно служат дольше всего — в конечном итоге изнашиваются в результате последствий положительной коррозии сетки.
- Свинцово-кислотные аккумуляторы, которые по целому ряду различных причин постоянно недозаряжены, не доводятся регулярно до полной зарядки — преждевременно выходят из строя в результате воздействия сульфатации.
Связанная статья: Демистификация средств защиты от сульфатации
Связанная статья: Почему важно понимать коррозию
Если вы планируете организовать такой бизнес, которым можно управлять из дома, всегда помните, что ваши прямые конкуренты будут делать то же самое . Неважно, насколько вы хороши, насколько вы лучше, в наше время, когда безработица стимулирует новые предприятия, такая конкуренция неизбежно ведет к снижению цен и уничтожению прибыли.
Неважно, насколько вы хороши, насколько вы лучше, в наше время, когда безработица стимулирует новые предприятия, такая конкуренция неизбежно ведет к снижению цен и уничтожению прибыли.
В начале 1980-х в мире насчитывалось 6,5 миллионов врачей, и все они были убеждены, что язва желудка вызывается стрессом. Два неизвестных врача, Барри Маршалл и Робин Уоррен из Перта, Австралия, обнаружили, что язва желудка вызывается бактерией под названием Helicobacter pylori . Больше никаких серьезных операций и пожизненной инвалидности. Курс антибиотиков решит проблему. Простой. Они игнорировались медиками в течение 10 лет. В конце концов было признано, что они были правы, и что 6,5 миллионов врачей все это время ошибались. Они оба получили Нобелевскую премию по медицине в 2005 году за свое открытие.
Это был не первый раз, когда все врачи в мире ошибались, и был один, кто возражал против распространенного заблуждения и был прав. Потребовались века и бесчисленное количество ненужных смертей, прежде чем врачи признали, что микробы вызывают болезни. Сегодня это звучит безумно, но это совершенно верно. Мораль этой истории такова: если кто-то скажет вам, что давнее убеждение ошибочно, и очень подробно объяснит, почему оно ошибочно, а вы проигнорируете совет, потому что хотите верить, что большинство всегда право, вы делаете ту же ошибку.
Сегодня это звучит безумно, но это совершенно верно. Мораль этой истории такова: если кто-то скажет вам, что давнее убеждение ошибочно, и очень подробно объяснит, почему оно ошибочно, а вы проигнорируете совет, потому что хотите верить, что большинство всегда право, вы делаете ту же ошибку.
Спасибо, что прочитали эту страницу.
СПРАВКА:
Исследования, проведенные группой выдающихся ученых Л.Т. Ламом, Х. Озгуном, О.В. Линем, Дж.А. Гамильтоном, Л.Х. Ву, Д.Г. В свинцово-кислотных батареях непроводящий барьерный слой оксида свинца постепенно разрушается, образуя расширяющиеся островки проводимости с применением пульсации. «Зарядка свинцово-кислотных аккумуляторов импульсным током -», Journal of Power Sources 53 (1995), стр. 226-227. [Если вы серьезно интересуетесь импульсной технологией, мы рекомендуем вам погуглить название должности и имя первого ученого в списке как одно предложение, чтобы получить отчет в формате PDF. (Ссылка на этот доклад — www.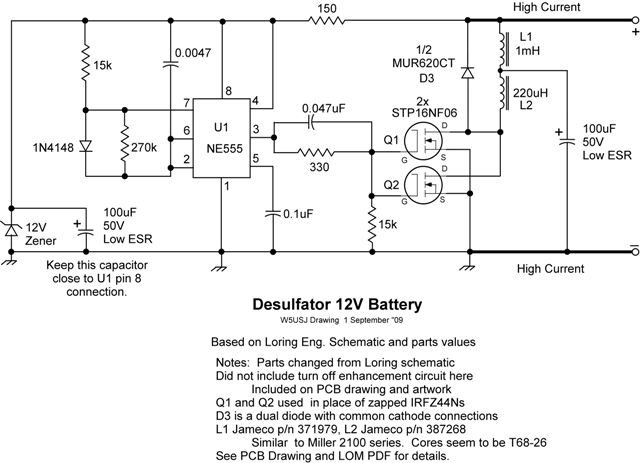 vershv.narod.ru/sdarticle.pdf).
vershv.narod.ru/sdarticle.pdf).
🛠️🔋 Десульфатация автомобильного аккумулятора
Десульфатация аккумулятора часто считается чистой магией, в которую либо веришь, либо нет. Причина такого отношения проста. Практически везде, где есть информация об этом методе реанимации автомобильного аккумулятора, шансы на успех не упоминаются. Многие пробуют и, не получив положительного результата, уходят в интернет, чреватым негативом. Там рождаются мифы, из-за которых естественно возникает недоверие к этой процедуре. А ведь десульфатация — это простая химия, которая при определенных условиях действительно помогает сэкономить.
Сульфатация пластин АКБ
Аккумуляторы со специфической сульфатацией пластин
Да простят автора Авто без СТО кандидаты хим. наук, но формул со сложной терминологией не будет. Феномен сульфатации свинцово-кислотных аккумуляторов можно легко объяснить с точки зрения человека. А это нужно для того, чтобы понять, как работает обратный процесс. Я имею в виду десульфатацию, ради которой вы пришли сюда.
Я имею в виду десульфатацию, ради которой вы пришли сюда.
Что такое батарея? Это пластиковый контейнер, разделенный на отсеки (баночки). В каждом таком отсеке размещены свинцовые пластины. Также вне зависимости от технологии есть электролит из воды и кислоты. Для того чтобы аккумулятор работал — заряжался и отдавал накопленную энергию, электролит должен контактировать со свинцом. Ключевым моментом здесь является контактная площадка.
От него зависят следующие показатели батареи:
- Номинальная емкость (А*ч) — чем больше площадь взаимодействия пластин с электролитом, тем больше энергии может накопить батарея.
- Максимальный пусковой ток (А) — тем выше, чем больше свинец контактирует с кислотой.
- Падение напряжения на нагрузке (В) — с увеличением площади контакта аккумулятор увереннее держит нагрузку.
Сульфатирование — образование сульфата свинца на пластинах при разрядке аккумулятора.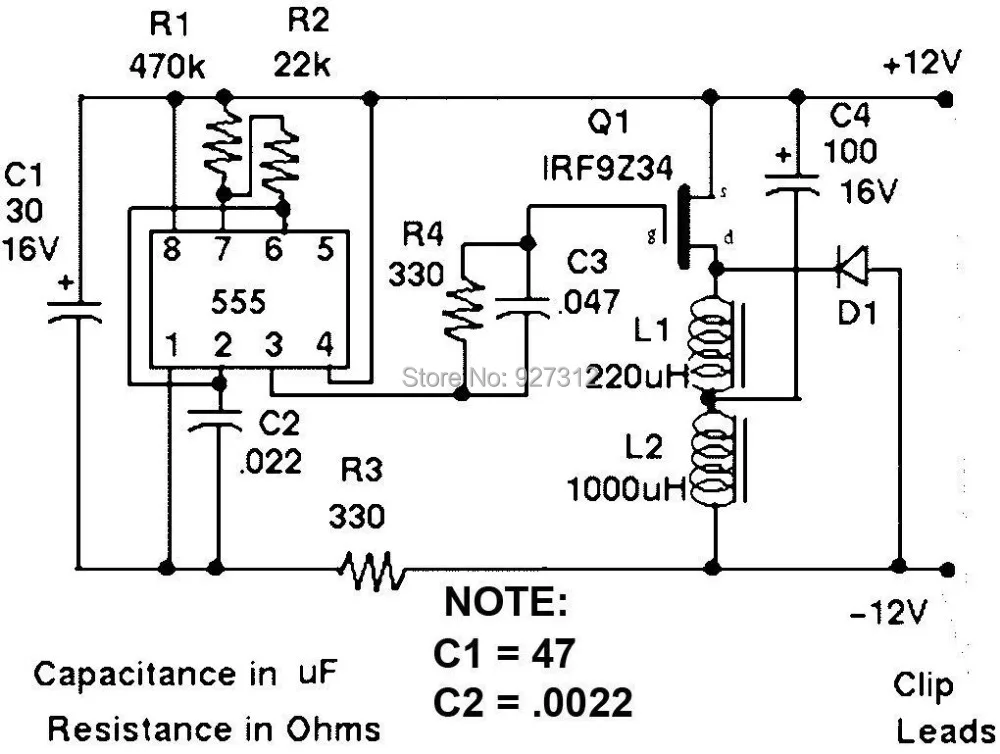 В результате на них появляется светло-серый налет. Если разряженную батарею сразу же зарядить, этот сульфат исчезает. Дальше все повторяется по циклу на протяжении всего срока службы батареи, и это норма.
В результате на них появляется светло-серый налет. Если разряженную батарею сразу же зарядить, этот сульфат исчезает. Дальше все повторяется по циклу на протяжении всего срока службы батареи, и это норма.
Проблемы начинаются при длительном простое аккумулятора в разряженном состоянии. Сульфат, образовавшийся на пластинах, затвердевает до такой степени, что уже не может раствориться при последующей зарядке. Соответственно, если косяк повторяется, к старому налету добавляется новый. В итоге получаем аккумулятор, пластины которого закрыты от электролита.
Сульфат свинца под микроскопомПлощадь контакта свинца и кислоты уменьшается. В результате пропадает емкость, уменьшается максимальный пусковой ток, а падения напряжения под нагрузкой стремятся к нулю вольт.
Принципы десульфатации аккумулятора
Десульфатация аккумулятора — это процесс, принципиально противоположный описанному выше сульфатированию. Когда аккумулятор эксплуатируется правильно — своевременно подзаряжается — то это происходит само собой, без всяких ухищрений и танцев с бубном.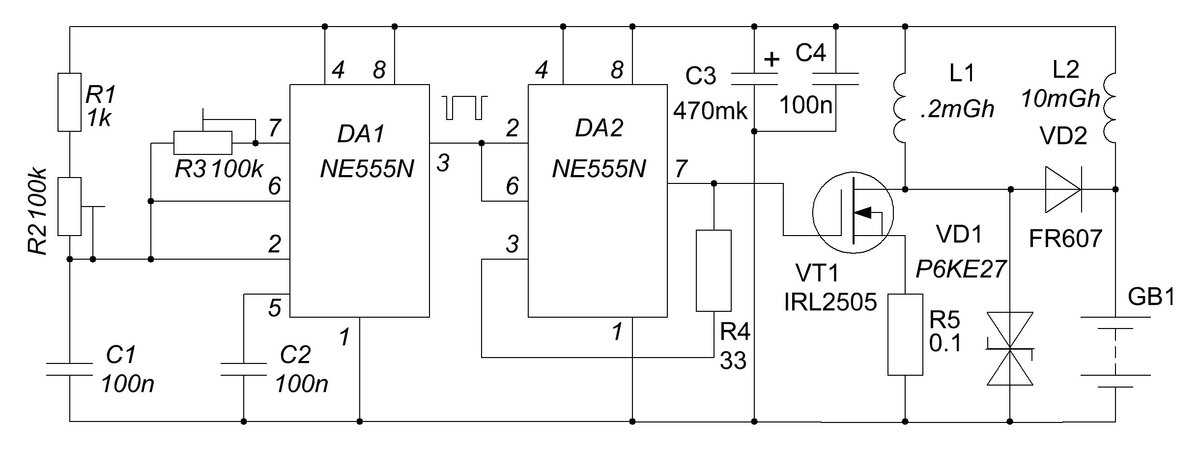 Однако в реальной жизни, к сожалению, многие автовладельцы обделяют своим вниманием аккумулятор, в результате чего большую часть жизни он катается под капотом в недозаряженном состоянии.
Однако в реальной жизни, к сожалению, многие автовладельцы обделяют своим вниманием аккумулятор, в результате чего большую часть жизни он катается под капотом в недозаряженном состоянии.
Задача, которую решает десульфатация, предельно проста. Он заключается в том, что необходимо как-то принудительно удалить вредный сульфат, из-за которого уменьшается площадь контакта с электролитом. Теоретически эту проблему можно решить несколькими способами. На практике не все работает. Но для более глубокого понимания темы давайте зацепим все основные методы десульфатации.
Одним из наиболее очевидных способов удаления сульфата со свинцовых пластин автомобильного аккумулятора является механическая очистка. Его принцип аналогичен очистке металла от следов коррозии. В Сети можно найти массу инструкций, которые по-серьезному щи подробно и понятно описывают этот процесс. Более того, авторы таких материалов обязуются гарантировать, что этот метод очень эффективен, и обязательно вернет к жизни сдохший от сульфатов аккумулятор. На самом деле механическая десульфатация — это нонсенс. Хотя бы потому, что для того, чтобы получить доступ к пластинам для их очистки, придется варварски распиливать корпус принципиально неразборной батареи.
На самом деле механическая десульфатация — это нонсенс. Хотя бы потому, что для того, чтобы получить доступ к пластинам для их очистки, придется варварски распиливать корпус принципиально неразборной батареи.
Еще один метод десульфатации, которым не стесняются делиться блогеры ради просмотров и лайков, чисто химический. Заключается он в том, что надо заправить убогий аккумулятор какой-нибудь ядреной химией, которая в силу своей агрессивности способна растворять сульфат. Что не советуют лить — от банальной газировки до препаратов типа Трилон-Б. Абсолютно ни один адекватный автолюбитель, конечно, не осмелился бы так жестко использовать химию. И Авто без СТО тоже настоятельно советует не чудить.
Никакую дичь в батарею не лить — это утопия Из адекватных технологий десульфатации можно выделить только один метод, для реализации которого ничего не нужно пилить, сверлить и заливать в банки. Он заключается в том, что сульфаты разрушаются в процессе естественной зарядки аккумулятора, но выполняемой особым образом. Как именно это делается, описано ниже.
Как именно это делается, описано ниже.
Шансы на успешную десульфатацию
Часто десульфатация не помогает
Но сначала стоит немного рассмотреть вопрос, на который почему-то обычно вообще не обращают внимания. Между тем всегда полезно задать этот вопрос перед десульфатацией аккумулятора. Возможно, правильный ответ на него поможет вам сэкономить массу времени, нервов, здоровья и денег. Суть в том, поможет ли десульфатация вашей батареи?
Оценить шансы на успех этой процедуры достаточно просто. Десульфатацию стоит делать, если :
- Аккумулятор не «старше» 5 лет (со дня выпуска, не покупки).
- Электролит прозрачный, не имеет коричневого оттенка.
- Ваш аккумулятор исправен, и вы проверяли уровень электролита не реже двух раз в год.
- Аккумулятор не простаивал в разряженном состоянии более 3-х месяцев.
- В аккумуляторе точно нет закороченных банок.
Во всех остальных случаях не верьте ни в какие чудодейственные методы и «особые» воспоминания, о которых также речь ниже.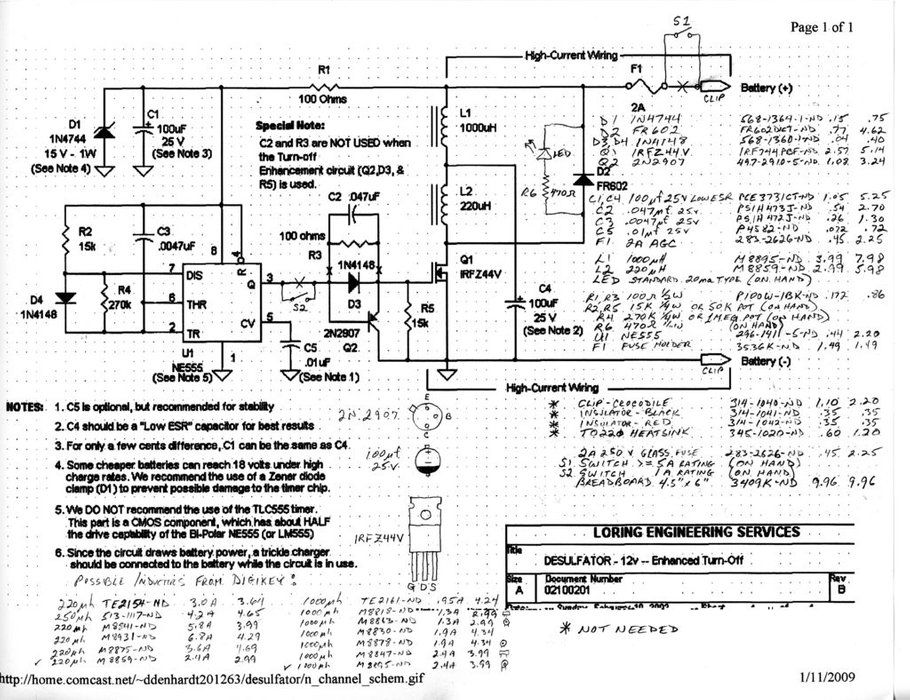 Ничто не поможет вашей батарее. Вы просто тратите свое время и деньги.
Ничто не поможет вашей батарее. Вы просто тратите свое время и деньги.
О ЗУ с функцией десульфатации аккумулятора
В наше время бурного развития электроники никого не удивишь зарядным устройством с функцией десульфатации. Хотя и сейчас нетрудно найти автомобилистов, отзывающихся о подобных устройствах со скепсисом. На самом деле такие ЗУ есть, и они не только стоят дороже обычных, но и реально справляются с сульфатами на пластинах аккумуляторов. Но не всегда. Как и везде, чудес в этом деле тоже не бывает, и шансы на успешное восстановление аккумулятора зависят не только от зарядного устройства.
Типовое зарядное устройство с функцией десульфатацииКратко рассмотрим, чем реально отличаются ЗУ с подобной функцией от обычных моделей.
Важное уточнение! Ниже перечислены отличия, большая часть которых присутствует только в тех моделях, которые имеют функцию десульфатации не только в виде надписи на корпусе, но и в начинке.
К сожалению, рынок буквально переполнен зарядными устройствами, на которых красуется надпись «десульфатация», однако после вскрытия оказывается, что внутри обычная пустышка.
Первое, что отличает зарядные устройства с функцией десульфатации, это продуманная схема стабилизации и ограничения зарядных характеристик — напряжения и тока. Это крайне важное условие успешного восстановления аккумулятора, так как в основе рассматриваемой технологии восстановления аккумулятора лежат специальные настройки и точная дозировка заданных параметров.
Второе отличие в том, что зарядное устройство не только заряжает, но и «умеет» разряжать аккумулятор. Причем прямо в процессе десульфатации. Существует множество способов реализации такой функции, начиная с простейших реле и заканчивая программой, зашитой в микропроцессор.
Третий , чем отличаются ЗУ с функцией десульфатации — заряд осуществляется так называемым пульсирующим током. Если объяснять на пальцах, то это режим, когда ток в аккумулятор загоняют не постоянно, а периодически, малыми дозами. Это позволяет избежать быстрой подзарядки аккумулятора и добиться лучшего «сбивания» сульфатов.
Если объяснять на пальцах, то это режим, когда ток в аккумулятор загоняют не постоянно, а периодически, малыми дозами. Это позволяет избежать быстрой подзарядки аккумулятора и добиться лучшего «сбивания» сульфатов.
Четвертое отличие , которым могут похвастаться далеко не все модели, это наличие функции оценки реальной емкости аккумулятора. На сайте Авто без СТО об этом неоднократно упоминается в других материалах об автомобильных аккумуляторах. Суть в том, что емкость б/у аккумулятора всегда меньше, чем указано на корпусе. Соответственно и ток заряда нужен меньше. В противном случае батарея будет заряжаться очень быстро, но как бы поверхностно. Это значит, что о качественной десульфатации не может быть и речи.
Именно из-за этих отличий зарядные устройства с функцией десульфатации заметно дороже обычных. Часто даже дороже, чем новый аккумулятор. Стоит ли это покупать? Если у вас в хозяйстве всего одна-две батареи, то ждать, пока окупится такая память, придется очень долго.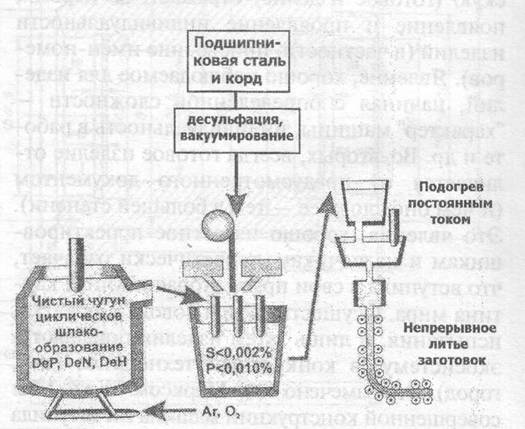 Кроме того, при большом желании и знании теории, изложенной ниже, можно восстановить аккумулятор простейшим зарядным устройством. Естественно, если ваша батарея проходит вышеописанный пятибалльный тест. Если аккумуляторов, которые нужно обслуживать, много, или вы делаете это для людей за деньги, то покупка «умного» мощного зарядного устройства для вас просто необходима.
Кроме того, при большом желании и знании теории, изложенной ниже, можно восстановить аккумулятор простейшим зарядным устройством. Естественно, если ваша батарея проходит вышеописанный пятибалльный тест. Если аккумуляторов, которые нужно обслуживать, много, или вы делаете это для людей за деньги, то покупка «умного» мощного зарядного устройства для вас просто необходима.
Десульфатация аккумулятора с помощью простого зарядного устройства
Если все же вы решили приобрести зарядное устройство с функцией десульфатации, то вам не нужно разбираться в сути этой процедуры. Устройство, соответствующее заявленному описанию, все сделает само. Однако можно попробовать восстановить аккумулятор с помощью обычной зарядки. Это вполне возможно, хотя и требует определенных знаний и большого количества времени. Если вы хотите попробовать, вот проверенное руководство.
Так выглядит процесс десульфатации «на автомате» Для начала следует уточнить, какое зарядное устройство подходит для десульфатации, так как это сможет сделать не каждый. Все, что вам нужно, это возможность контролировать и регулировать параметры зарядки. А именно напряжение и ток. Для контроля достаточно обычного мультиметра (лучше два, чтобы контролировать и напряжение, и ток одновременно). Но для регулировки должна быть предусмотрена установка напряжения.
Все, что вам нужно, это возможность контролировать и регулировать параметры зарядки. А именно напряжение и ток. Для контроля достаточно обычного мультиметра (лучше два, чтобы контролировать и напряжение, и ток одновременно). Но для регулировки должна быть предусмотрена установка напряжения.
Алгоритм десульфатации следующий:
- Определить фактическую емкость аккумулятора . Это можно сделать с помощью обычной лампы автомобильной фары – полностью зарядить аккумулятор в обычном режиме, а затем разрядить лампу до тех пор, пока напряжение на клеммах не упадет до 10,5 В. Средний ток, потребляемый лампой, рассчитывается путем деления мощности на Напряжение. Далее, зная силу тока и время, рассчитать емкость (пример для наглядности ниже).
- Ограничение зарядного тока . Оптимальный ток как для обычной зарядки аккумулятора, так и для десульфатации составляет 10% от емкости. Не выше.
- Предельное напряжение .
 Оно не должно превышать 14,4 В на протяжении всей процедуры. На первом этапе, когда батарея полностью разряжена, напряжение при вышеуказанном токе будет в районе 12,7-13,0 В. Далее, по мере заряда, оно будет повышаться.
Оно не должно превышать 14,4 В на протяжении всей процедуры. На первом этапе, когда батарея полностью разряжена, напряжение при вышеуказанном токе будет в районе 12,7-13,0 В. Далее, по мере заряда, оно будет повышаться. - Зарядить аккумулятор. Но не до конца, как в обычном режиме, а на 30-60 минут.
- Немного разрядите аккумулятор. Можно использовать ту же лампочку. Отсоедините аккумулятор от зарядного устройства и зарядите его лампой на 5-10 минут.
- Повторяйте шаги 4 и 5 до полной зарядки. То есть заряжать аккумулятор, периодически разряжая его. Продолжайте до полной зарядки аккумулятора в этом режиме. О полном заряде можно судить по току, который упал до 0,1 А при напряжении 14,4 В.
- При необходимости повторить. Как правило, если аккумулятор не сильно сульфатирован, для его восстановления достаточно одного такого цикла. Если батарея сильно убита, то желательно повторить процедуру 2-3 раза.
 Но не более.
Но не более.
Во время ручной десульфатации избегайте:
- перегрева батареи;
- «кипящий»;
- ток выше 10% емкости;
- напряжения выше 14,4 В.
По завершению десульфатации, ради интереса, можно повторно замерить емкость аккумулятора. Если она увеличилась, то вы не зря парились. После очередного разряда можно зарядить аккумулятор в обычном режиме, либо пройти тренировочный цикл по вышеописанному алгоритму еще раз.
Пример емкости . Допустим, у вас есть аккумулятор с заявленной на корпусе емкостью 70 Ач, и лампочка в фаре на 50 Вт. Среднее напряжение разряда можно принять равным 11 В, так как оно будет постепенно уменьшаться с 12,7 В до 10,5 В. В этом случае средний ток разряда будет 50:11 = 4,5 А. Допустим, ваш аккумулятор был разряжен таким лампочка до 10,5 В 12 часов. Умножаем ток на время, то есть 4,5*12, и получаем реальную приблизительную емкость — 54 А*ч.
Соответственно такая батарея должна как заряжаться, так и тренироваться током не более 5,4 А (10% от емкости).
Результаты
Десульфатация автомобильного аккумулятора — это не волшебство и не миф. Это вполне реальный метод восстановления, который можно реализовать двумя способами. Первый — купить специальную память с соответствующим режимом и довериться электронике. Второй – провести процедуру в ручном режиме по описанному выше алгоритму. Конечно, не забывайте оценивать свои шансы на успех, чтобы не тратить время зря. Напишите в комментариях под статьей, что вы думаете о десульфатации автомобильного аккумулятора, поделитесь своими успехами и неудачами по этому поводу.
ВИДЕО: десульфатация аккумулятора (2 части)
youtube.com/embed/qlU3ew4bwPw» frameborder=»0″ allowfullscreen=»allowfullscreen» loading=»lazy»>
ОБЗОР ДЕСУЛЬФАЦИИ СВИНЦОВО-КИСЛОТНОЙ АККУМУЛЯТОРНОЙ БАТАРЕИ ДЛЯ HEV
- Идентификатор корпуса: 212476662
@inproceedings{Singh3015REVIEWOD,
title={ОБЗОР ДЕСУЛЬФАЦИИ СВИНЦОВО-КИСЛОТНЫХ АККУМУЛЯТОРОВ ДЛЯ ГЭМ},
автор = {Анупама Сингх и доктор П. Б. Карандикар},
год = {2015}
} - Анупама Сингх, доктор П. Б. Карандикар
- Опубликовано в 2015 г.
- Инженерное дело
В современном мире электромобили с гибридным приводом (EHV) представляют собой преобладающую технологию транспортных средств, в которой основной частью является электрическая батарея. Свинцово-кислотная батарея является широко используемой батареей в EHV из-за ее стоимости и эффективности. Настоящим недостатком свинцово-кислотных аккумуляторов является то, что они легко сульфатируются из-за неправильной зарядки или разрядки. Следовательно, схема десульфатации или контроллер заряда размещается вместе с перезаряжаемой свинцово-кислотной батареей для надлежащей зарядки, и впоследствии сульфатация снижается…
Следовательно, схема десульфатации или контроллер заряда размещается вместе с перезаряжаемой свинцово-кислотной батареей для надлежащей зарядки, и впоследствии сульфатация снижается…
Десульфатация свинцово-кислотных аккумуляторов высокочастотным импульсом
- W. Jamratnaw
Машиностроение
2017 14-я Международная конференция по электротехнике/электронике, компьютерам, телекоммуникациям и информационным технологиям (ECTI-CON)
- 2 3017290
- 0
- 0
После того, как свинцово-кислотная батарея была заряжена высокочастотными импульсами, внутреннее сопротивление батареи стало ниже, а напряжение полностью заряженной батареи и ток холодного пуска были выше, что привело к повышению производительности батареи.
Повторное использование наследия для модернизации микросетей — доступное решение для тестирования и восстановления перепрофилированных свинцово-кислотных аккумуляторов
В этом документе предлагается быстрая, недорогая и массовая процедура тестирования для определения характеристик свинцово-кислотных аккумуляторов, измерения емкости и восстановления без какой-либо их известной истории или таблицы с использованием процесса глубокого циклирования.
Новый пирометаллургический метод переработки свинцовой аккумуляторной пасты без образования SO2: термодинамическое и экспериментальное исследование
- Yun Li, Yongming Chen, A. Jokilaakso
Материаловедение, машиностроение
- 2018
Представлен инновационный процесс переработки свинца из отходов пасты для свинцово-кислотных аккумуляторов. Новшеством в этом процессе является предотвращение образования и выбросов SO2 за счет использования метода восстановительной фиксации серы.…
Новый процесс переработки пасты для свинцово-кислотных аккумуляторов без образования SO2 — механизм реакции и промышленная пилотная кампания
- Yun Li, Shenghai Yang, A. Jokilaakso
Материаловедение, машиностроение
Журнал чистого производства
- 2019
Система восстановления свинцово-кислотных аккумуляторных батарей с использованием двухпозиционного заряда постоянного тока и коротких-больших импульсов разряда
- I.
 Mizumoto, Y. Yoshii, K. Yamamoto, H. Oguma
Mizumoto, Y. Yoshii, K. Yamamoto, H. Oguma Engineering, Environmental Science
Electronics Letters
- 2018
Мы сообщаем о методе восстановления разложившихся свинцово-кислотных батарей – выключенный метод заряда постоянным током и короткий–большой импульсный разряд. Когда увеличение внутреннего импеданса находится в пределах ∼20% от…
, показывающий 1-10 из 66 ссылок
Сорт Byrelevancemost, повлиявший на работу,
Идентификация и восстановление сульфатирования в батареях свинцовой кислоты с использованием клеточного напряжения и зондирования давления
- Ying Shi, Christopher A. Ferone, C. rahn
- Ying Shi, Christopher A. Ferone, C. rahn
- 9
- Ying Shi, Christopher A. Ferone, C. Rahn
- Ying Shi, Christopher A. Ferone. Инженерное дело
- 2013
Восстановление емкости сульфатированного свинцово-кислотного аккумулятора с использованием управления зарядкой с обратной связью по давлению
- Ин Ши, Кристофер А.
 Фероне, К. Ран
Фероне, К. Ран Инженерия, наука об окружающей среде
- 2012
Свинцово-кислотные аккумуляторы с клапанным регулированием (VRLA) могут разлагаться из-за различных механизмов, включая коррозию, жесткую сульфатацию, потерю воды, осыпание и активное разложение массы. Жесткое сульфатирование может быть…
Характеристики заряда и разряда свинцово-кислотного аккумулятора и аккумулятора LiFePO4
В данной статье предложены характеристики заряда и разряда свинцово-кислотного аккумулятора и аккумулятора LiFePO4. Цель этой статьи состоит в том, чтобы предложить зарядное устройство импульсного тока с более высоким пиковым значением…
Стратегия контроля аккумуляторной батареи маховика для электромобилей
Электромобили (EV) являются идеальным транспортным средством для уменьшения загрязнения воздуха и выбросов углекислого газа. Однако современные источники энергии не подходят для электромобилей по плотности энергии,…
Усовершенствованная динамическая модель свинцово-кислотных аккумуляторов с использованием данных производителей
Моделирование и моделирование свинцово-кислотных аккумуляторов имеет первостепенное значение для транспортных систем, таких как гибрид электромобили, тележки для гольфа, электрические скутеры и инвалидные коляски; и для батареи…
Использование свинцово-кислотных аккумуляторов при разработке систем возобновляемой энергии в Китае
- Ю Чанг, Сяньсянь Мао, Яньфан Чжао, С.
 Фэн, Хонгю Чен, Д. Финлоу
Фэн, Хонгю Чен, Д. Финлоу Инженерия, наука об окружающей среде
- 2009
Вспомогательная система питания на основе ультраконденсаторов для электромобиля: реализация и оценка
Результаты показали значительное снижение затрат при включении конфигураций AES по сравнению с системой, работающей только на топливных элементах, и снижение затрат было выше при использовании ультраконденсаторов. для этой цели.
Расчет нечеткой оценки SOC для герметичных свинцово-кислотных аккумуляторов электромобилей в Reflex TM
В этом документе предлагается нечеткая оценка состояния заряда (SOC) для зарядки аккумуляторов ReflexTM, которая обеспечивает быструю и эффективную зарядку герметичных свинцово-кислотных аккумуляторов. аккумуляторы, используемые в электромобилях. The…
Сравнение стратегий бортовой зарядки для гибридных автомобилей с увеличенным запасом хода со свинцово-кислотными батареями
- N.


 OEM добро пожаловать б. высокоэффективный c. экономия энергии г. ISO9001, CE Насос сероочистки серии DT 1, Обзор производства: В ограничительных деталях насоса используется передовая технология моделирования потока, чтобы гарантировать…
OEM добро пожаловать б. высокоэффективный c. экономия энергии г. ISO9001, CE Насос сероочистки серии DT 1, Обзор производства: В ограничительных деталях насоса используется передовая технология моделирования потока, чтобы гарантировать… ниже, чем с металлической футеровкой, а срок ее…
ниже, чем с металлической футеровкой, а срок ее… Наша компания может обрабатывать импортные и отечественные насосы десульфурации, и мы можем обработать детали насоса десульфурации, если вы…
Наша компания может обрабатывать импортные и отечественные насосы десульфурации, и мы можем обработать детали насоса десульфурации, если вы… Они конструированы для поставлять истирательную, большую частицу и суспензий высокой плотности. Эти насосы нет необходимости любой воды уплотнения и запечатывания вала. Они также…
Они конструированы для поставлять истирательную, большую частицу и суспензий высокой плотности. Эти насосы нет необходимости любой воды уплотнения и запечатывания вала. Они также… 2) антикоррозионная и противоизносных металла и резины материалы, которые специально разработаны для насосов ДДГ оказались на практике, что они могут обеспечить…
2) антикоррозионная и противоизносных металла и резины материалы, которые специально разработаны для насосов ДДГ оказались на практике, что они могут обеспечить…
 Принцип задержания H2S и NH3 основывается на использовании в качестве фильтра колоний глубоководных океанских сульфатредуцирующих и / или анаммокс-бактерий, способных на «природную» утилизацию токсичных газов.
Принцип задержания H2S и NH3 основывается на использовании в качестве фильтра колоний глубоководных океанских сульфатредуцирующих и / или анаммокс-бактерий, способных на «природную» утилизацию токсичных газов.
 Макки3,
Макки3, edu; ФАКС (212) 923-2090.
edu; ФАКС (212) 923-2090. 1101/гад.1711308 Гены и Дев. 2008.
22:
2645-2650 Copyright © 2008, Cold Spring Harbour Laboratory Press
1101/гад.1711308 Гены и Дев. 2008.
22:
2645-2650 Copyright © 2008, Cold Spring Harbour Laboratory Press
 Дж. Нейрохим. 139 , 58–75 (2016).
Дж. Нейрохим. 139 , 58–75 (2016).
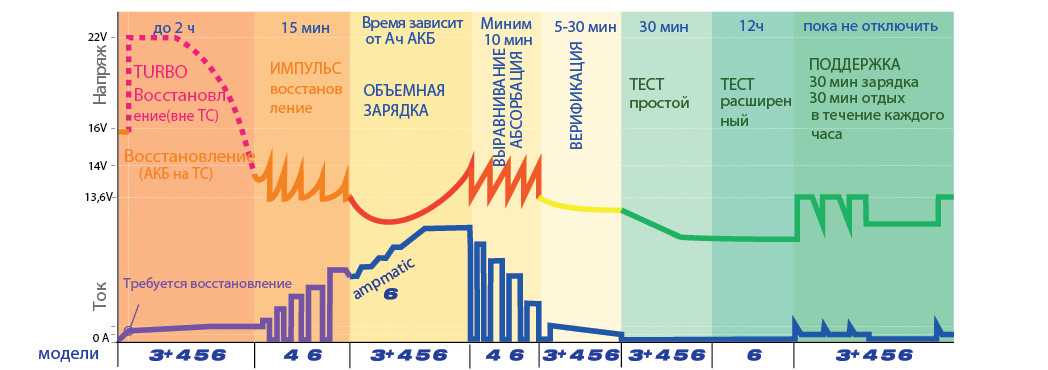 ПлоС Один 10 , e0139853 (2015).
ПлоС Один 10 , e0139853 (2015). Джин 108 , 193–199 (1991).
Джин 108 , 193–199 (1991). Biol. хим. 287 , 9579–9590 (2012).
Biol. хим. 287 , 9579–9590 (2012). Дж. Биол. хим. 276 , 29141–29147 (2001).
Дж. Биол. хим. 276 , 29141–29147 (2001). Природа 400 , 331–336 (1999).
Природа 400 , 331–336 (1999). Наука 302 , 1044–1046 (2003).
Наука 302 , 1044–1046 (2003).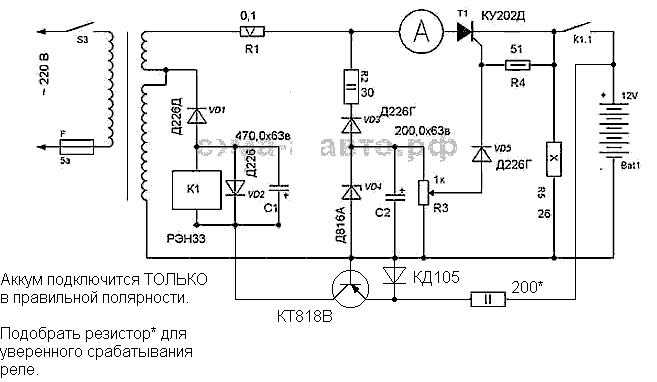 Нейрон 41 , 723–736 (2004).
Нейрон 41 , 723–736 (2004). . Модификации внеклеточного сахара предоставляют поучительную и специфичную для клеток информацию для выбора направления аксонов. Курс. биол. 18 , 1978–1985 (2008).
. Модификации внеклеточного сахара предоставляют поучительную и специфичную для клеток информацию для выбора направления аксонов. Курс. биол. 18 , 1978–1985 (2008).
 К сожалению, рынок буквально переполнен зарядными устройствами, на которых красуется надпись «десульфатация», однако после вскрытия оказывается, что внутри обычная пустышка.
К сожалению, рынок буквально переполнен зарядными устройствами, на которых красуется надпись «десульфатация», однако после вскрытия оказывается, что внутри обычная пустышка.  Оно не должно превышать 14,4 В на протяжении всей процедуры. На первом этапе, когда батарея полностью разряжена, напряжение при вышеуказанном токе будет в районе 12,7-13,0 В. Далее, по мере заряда, оно будет повышаться.
Оно не должно превышать 14,4 В на протяжении всей процедуры. На первом этапе, когда батарея полностью разряжена, напряжение при вышеуказанном токе будет в районе 12,7-13,0 В. Далее, по мере заряда, оно будет повышаться. Но не более.
Но не более. Соответственно такая батарея должна как заряжаться, так и тренироваться током не более 5,4 А (10% от емкости).
Соответственно такая батарея должна как заряжаться, так и тренироваться током не более 5,4 А (10% от емкости).  Mizumoto, Y. Yoshii, K. Yamamoto, H. Oguma
Mizumoto, Y. Yoshii, K. Yamamoto, H. Oguma Фероне, К. Ран
Фероне, К. Ран Фэн, Хонгю Чен, Д. Финлоу
Фэн, Хонгю Чен, Д. Финлоу