| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Б330231101010PGAK Бак топливный ГАЗ-3302,33023 металлический 70л (235х380х830) БАКОР — Б33023-1101010-PG-AK 33023-1101010
Распечатать
Главная Запчасти для наших машин и тракторов
12
1
Применяется: ГАЗ
Код для заказа: 648529
Добавить фото
6 500 ₽
Дадим оптовые цены предпринимателям и автопаркам ?
Наличные при получении VISA, MasterCard, МИР Долями Оплата через банк
Производитель: БАКОР
Получить информацию о товаре или оформить заказ вы можете по телефону 8 800 6006 966.
Есть в наличии
Самовывоз
Уточняем
Доставка
Уточняем
Доступно для заказа —
Данные обновлены: 06.04.2023 в 00:30
- Все характеристики
- Отзывы о товаре
- Вопрос-ответ
- Описание
- Аналоги
- Где применяется
Характеристики
Сообщить о неточности
в описании товара
648529
АртикулыБ33023-1101010-PG-AK, 33023-1101010
ПроизводительБАКОР
Каталожная группа: .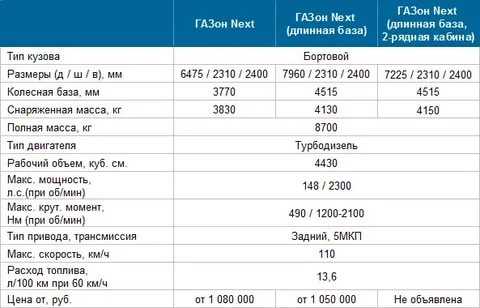 .Система питания двигателя
.Система питания двигателя
Двигатель
0.38
Высота, м:0.235
Длина, м:0.83
Вес, кг:16
Описание
Бак топливный для Газели с карбюраторным двигателем.
Объем бака, л = 70
Объем бака, м3 = 0,115
Размер: 235х380х830 Все топливные баки БАКОР имеют оригинальную упаковку, а также комлектуются: крышкой заливной горловины и сливной пробкой.
Отзывы о товаре
Вопрос-ответ
Задавайте вопросы и эксперты
помогут вам найти ответ
Чтобы задать вопрос, необоходимо
авторизоваться/зарегистрироваться
на сайте
Чтобы добавить отзыв, необходимо
авторизоваться/зарегистрироваться
на сайте
Чтобы подписаться на товар, необходимо
авторизоваться/зарегистрироваться
на сайте
| |||||||||||||||||||||
10.7: Преобразование молей в объем газа
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 53771
Как узнать, сколько газа находится в этих контейнерах?
Небольшие газовые баллоны часто используются для подачи газов для химических реакций. Газометр даст некоторую информацию о том, сколько газа в баке, но нужны количественные оценки, чтобы реакция могла протекать до конца. Знание того, как рассчитать необходимые параметры для газов, очень полезно, чтобы избежать их исчерпания раньше, чем хотелось бы.
Преобразование между молями и объемом газа
Молярный объем при нормальных условиях можно использовать для преобразования молей в объем газа и из объема газа в моли. Равенство \(1 \: \text{mol} = 22,4 \: \text{L}\) является основой для коэффициента преобразования.
Пример \(\PageIndex{1}\): преобразование объема газа в моли
Многие металлы реагируют с кислотами с образованием газообразного водорода. В ходе определенной реакции образуется \(86,5 \: \text{L}\) газообразного водорода при нормальных условиях. Сколько молей водорода было получено?
Решение
Шаг 1: Перечислите известные количества и спланируйте задачу. Известно- \(86.5 \: \text{L} \: \ce{H_2}\)
- \(1 \: \text{моль} = 22,4 \: \text{L}\)
- моль H 2
Применить коэффициент преобразования литров в моли.
Шаг 2: Расчет.
\[86,5 \: \text{L} \: \ce{H_2} \times \frac{1 \: \text{моль} \: \ce{H_2}}{22,4 \: \text{L} \: \ce{H_2}} = 3,86 \: \text{mol} \: \ce{H_2}\nonumber \]
Шаг 3: Подумайте о своем результате.Объем добываемого газа почти в четыре раза превышает молярный объем. Тот факт, что газ является водородом, не играет никакой роли в расчетах.
Пример \(\PageIndex{2}\): преобразование молей в объем газа
Какой объем \(4,96 \: \text{моль}\) из \(\ce{O_2}\) занимает при STP?
Решение
Шаг 1: Перечислите известные количества и спланируйте проблему .
Известен- \(4.96 \: \text{mol} \: \ce{O_2}\)
- \(1 \: \text{моль} = 22,4 \: \text{L}\)
- Объем O 2
\[4,96 \: \text{моль} \times 22,4 \: \text{л/моль} = 111,1 \: \text{л}\номер \]
Шаг 3: Подумайте о своем результате.
Объем кажется правильным, учитывая количество молей.
Пример \(\PageIndex{3}\): Преобразование объема в массу
Если мы знаем объем пробы газа на STP, мы можем определить, сколько массы присутствует. Предположим, у нас есть \(867 \: \text{L}\) из \(\ce{N_2}\) в STP. Какова масса газообразного азота?
Решение
Шаг 1: Перечислите известные количества и спланируйте задачу. Известно- \(867 \: \text{L} \: \ce{N_2}\)
- \(1 \: \text{моль} = 22,4 \: \text{L}\)
- Молярная масса \(\ce{N_2} = 28,02 \: \text{г/моль}\)
- Масса N 2
Начнем с определения количества молей присутствующего газа. Мы знаем, что 22,4 литра газа при нормальных условиях равны одному молю, поэтому:
\[867 \: \text{L} \times \frac{1 \: \text{mol}}{22,4 \: \text{L}} = 38,7 \: \text{mol}\nonumber \]
Мы также знаем молекулярную массу \(\ce{N_2}\) \(\left( 28,0 \: \text{г/моль} \right)\), поэтому мы можем вычислить вес газообразного азота в 867 литры:
\[38,7 \: \text{моль} \times \frac{28 \: \text{г}}{1 \: \text{моль}} = 1083,6 \: \text{г} \: \ ce{N_2}\nonumber \]
Шаг 3: Подумайте о своем результате.
В многошаговой задаче убедитесь, что единицы проверены.
Резюме
- Показаны преобразования между молями и объемом газа.
Обзор
- Почему в приведенных выше задачах газ всегда имел нормальную температуру и давление?
- Контейнер содержит 45,2 л газа N 2 при нормальных условиях. Сколько молей газа N 2 в сосуде?
- Если газ в предыдущей задаче был CH 4 газ при STP вместо N 2 газ, то сколько молей CH 4 газ будет?
Эта страница под названием 10.7: Conversions Between Moles and Gas Volume используется в соответствии с лицензией CK-12 и была создана, изменена и/или курирована Фондом CK-12 с помощью исходного контента, который был отредактирован в соответствии со стилем и стандартами LibreTexts.

 А в сочетании с промтоварным кузовом и газовым оборудованием данный автомобиль станет выгодным партнером, для самых различных нужд.
А в сочетании с промтоварным кузовом и газовым оборудованием данный автомобиль станет выгодным партнером, для самых различных нужд. 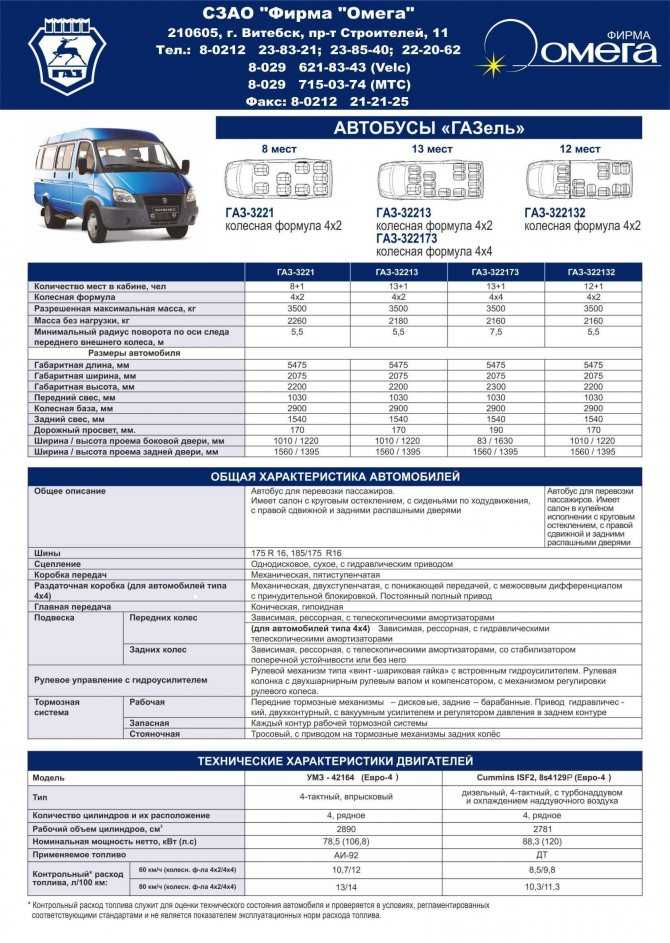 ru
ru Усолье-Сибирском
Усолье-Сибирском
 Усолье-Сибирском
Усолье-Сибирском

 Москва
Москва
 Замечено, что если мы имеем
определенное количество (масса или объем) присутствующего газа, значение
температура и давление не зависят от количества газа,
мы рассматриваем. Например, предположим, что у нас есть бак с бензином.
Если мы вставим тарелку в бак
что сокращает объем вдвое, температуру в
каждая половина остается неизменной, как и давление. Значение
давление и температура не зависят от количества газа, используемого в
измерение. С другой стороны, масса газа зависит
на громкости. Разрезание объема на две части сокращает массу на две части.
масса каждой секции бака равна половине массы всего бака.
масса зависит от объема, а объем, в свою очередь, зависит от
масса. Если мы сохраним давление и температуру этого газа и
заполнить объект, который может изменять свой объем, например, воздушный шар или
цилиндр со скользящим концом, конечный объем напрямую зависит от
количество газа, которое мы закачиваем. Вы можете попробовать этот эксперимент на
анимированная газовая лаборатория. Обратите внимание, что если
мы держим объем постоянным и вводим массу, значение давления
и изменение температуры, но в примере на этом слайде общее
масса сохраняется постоянной.
Замечено, что если мы имеем
определенное количество (масса или объем) присутствующего газа, значение
температура и давление не зависят от количества газа,
мы рассматриваем. Например, предположим, что у нас есть бак с бензином.
Если мы вставим тарелку в бак
что сокращает объем вдвое, температуру в
каждая половина остается неизменной, как и давление. Значение
давление и температура не зависят от количества газа, используемого в
измерение. С другой стороны, масса газа зависит
на громкости. Разрезание объема на две части сокращает массу на две части.
масса каждой секции бака равна половине массы всего бака.
масса зависит от объема, а объем, в свою очередь, зависит от
масса. Если мы сохраним давление и температуру этого газа и
заполнить объект, который может изменять свой объем, например, воздушный шар или
цилиндр со скользящим концом, конечный объем напрямую зависит от
количество газа, которое мы закачиваем. Вы можете попробовать этот эксперимент на
анимированная газовая лаборатория. Обратите внимание, что если
мы держим объем постоянным и вводим массу, значение давления
и изменение температуры, но в примере на этом слайде общее
масса сохраняется постоянной.
 Для многих жидкостей
динамические (подвижные) приложения, масса варьируется от одного места к
другой, и аэродинамики обычно используют плотность как интенсивную
свойство.
Для многих жидкостей
динамические (подвижные) приложения, масса варьируется от одного места к
другой, и аэродинамики обычно используют плотность как интенсивную
свойство.