Неисправность коробки передач Toyota Сorolla — причины, способы устранения неисправности КПП Тойота Королла
Если какая-либо из передач на автомобиле модели «Тойота Королла» отказывается включаться, можно устранить неисправность самостоятельно. В ситуации, когда это сделать не удается, стоит обратиться в специализированные технические центры официального дилера японской марки Тойота Люберцы и Тойота Измайлово.
Возможные причины неисправности
Нарушения в переключении передач на автомобилях, оснащенных механическими коробками передач ММТ, могут происходит по ряду причин.
- Может быть нарушено функционирование цилиндров системы сцепления — рабочего или главного.
- Возможно, состояние трубопровода, соединяющего рабочий и главный цилиндры системы, нарушено.
- Еще одна причина — нарушения в состоянии троса, отвечающего за включение передачи.
- Могут быть изношены элементы сцепления (1 ряд): речь идет о фрикционных настройках, маховиках, ведомом диске сцепления, выжимном подшипнике или нажимном диске;
- Износившиеся элементы системы сцепления (синхронизаторы, шестерни, подшипники) также могут стать причиной невозможности включить передачу.

При наличии роботизированной коробки передач ММТ нарушения в переключении передач, как правило, возникают, когда
- сцепление (ряд 1) перегревается: об это свидетельствует звуковой сигнал и включение лампы на приборной панели, сообщающей о том, что возникла неисправность;
- выходит из строя актуатор выжима;
- нарушается работа актуатора выбора передачи;
- детали системе сцепления изношены: нажимной диск, выжимной подшипник, фрикционные накладки ведомого диска сцепления, маховик.
Если в автомобиле установлены автоматическая коробка передач, нарушения в переключении сцепления могут быть вызваны
- неисправностью гидротрансформатора;
- нарушениями в работе гидроблока;
- проблемами в работе блока управления трансмиссией;
- снижением уровня трансмиссионной жидкости в коробке передач.
Самостоятельное устранение неисправности
В некоторых случаях нарушение можно исправить самостоятельно. Так, если возник перегрев сцепления, рекомендуется остановить автомобиль, заглушить двигатель и подождать, пока сцепление остынет. Затем можно двигаться снова.
Так, если возник перегрев сцепления, рекомендуется остановить автомобиль, заглушить двигатель и подождать, пока сцепление остынет. Затем можно двигаться снова.
В ситуации, когда в автоматической коробке передач чрезмерно снижается уровень трансмиссионной жидкости, ее необходимо долить до нужного уровня. Проверить показатели при помощи щупа.
Устранение неполадок в техническом центре
При обращении автовладельца в наши технические центры с данной проблемой специалисты сначала диагностируют состояние системы, определяют причину поломки — тот элемент, который неисправен.
Далее выполняется замена поврежденной детали или узла. Работа трансмиссии тестируется.
Для записи обращайтесь к менеджерам продаж нашей компании по телефону или через форму заказа обратного звонка.
Запись на ТО
Почему не работает коробка передач и как произвести ремонт КПП | ГК Витес
16 Sep 2022
Мы оказываем консультации и принимаем заявки на ремонт грузовиков и заявки на подбор запчастей дистанционно и рады видеть Вас в числе наших клиентов и партнеров!
Опытные автовладельцы знают, что в плане нагрузки на узлы и агрегаты на втором месте сразу после двигателя находится коробка переключения передач.
В данной статье будут рассмотрены основные виды неисправностей МКПП и полезные советы по продлению срока исправной службы коробок.
«Механика» в прошлом? – Нет!
Сколько бы ни говорили представители «прогрессивного» подхода в автомобилестроении о том, что дни механической коробки передач сочтены, и уже совсем скоро она «выйдет из оборота», у механики всё ещё есть ряд неоспоримых преимуществ в сравнении с АКПП. Стоит перечислить основные из них:
Приемлемая цена. Как правило, вариант с МКПП обходится покупателю авто гораздо дешевле.
МКПП всё ещё лидируют по показателям экономичного расхода топлива.
МКПП сложнее перегреть.
МКПП выдерживает более тяжёлые нагрузки.
Механика проще в конструкции и прочнее, нежели автомат.

По причине двух последних пунктов МКПП всё ещё популярны в конструкциях грузовых автомобилей и тяжелых кроссоверов, не говоря уже о многих «легковушках».
Немного о сцеплении
Неопытные водители часто путают неисправности в работе КПП с неисправностями сцепления. Хоть сцепление и находится в непосредственной близости к коробке передач, оно являет собой отдельный механизм, который тоже влияет на качественную работу коробки.
Чаще всего среди неисправностей сцепления встречается износ фрикционных накладок диска сцепления
Что делать если не работает коробка передач?
Скорее всего, каждый водитель понимает, что такое КПП. Коробка переключения передач является элементом трансмиссии и также требуется для изменения передаточного числа и, следовательно, крутящего момента, передаваемого от мотора на ведущие колеса транспортного средства. Кроме того, КПП позволяет автомобилю двигаться задним ходом.
Коробка переключения передач является элементом трансмиссии и также требуется для изменения передаточного числа и, следовательно, крутящего момента, передаваемого от мотора на ведущие колеса транспортного средства. Кроме того, КПП позволяет автомобилю двигаться задним ходом.
В отличие от мотора, КПП имеет чрезвычайно долгий срок службы и может нормально работать в течение всего периода службы машины. Однако это разрешено только в том случае, если трансмиссия обслуживается быстро и эффективно. В ином случае трансмиссия может сломаться независимо от ее срока службы. В этом случае также требуется полный ремонт КПП. Восстановить как автоматическую, так и механическую коробку передач крайне сложно, поэтому не стоит доверять ее непрофессионалам. Легкомысленное и не профессиональное отношение к ремонту коробки передач опасно в случае других поломок, а также больших затрат на восстановление специалистами.
Не работает КПП — возможные причины неисправности
По мнению ряда специалистов, большинство неисправностей МКПП связаны именно со стилем вождения (агрессивный либо спортивный) и неправильными условиями эксплуатации.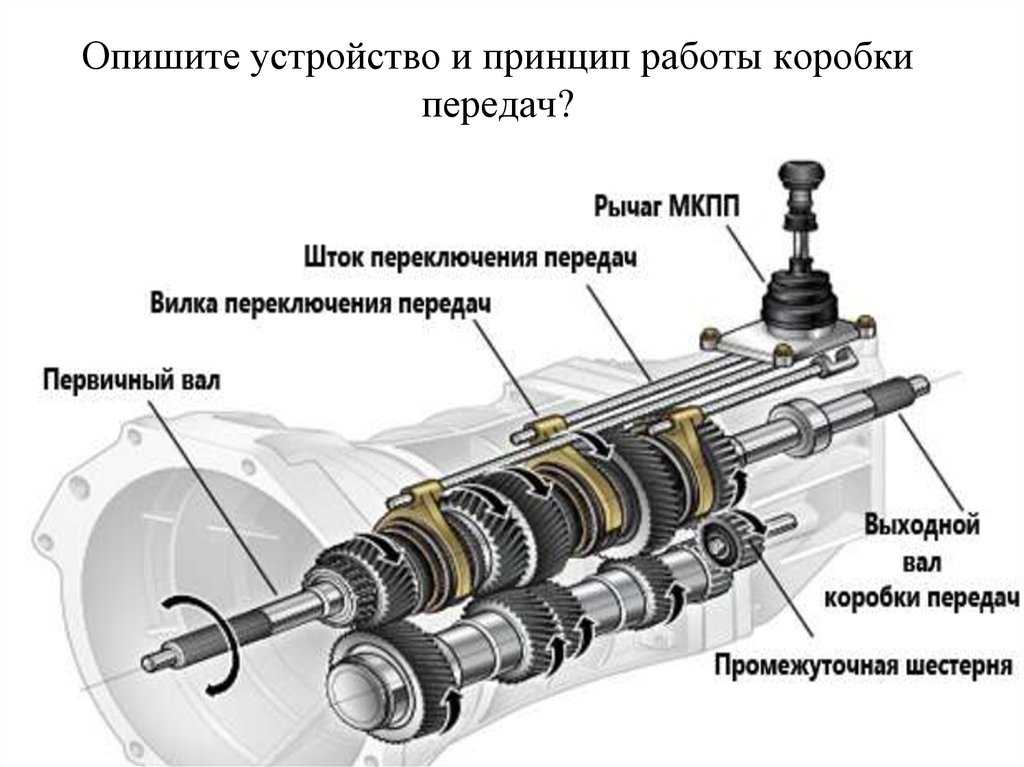 К «классическим» нарушениям в работе МКПП относят:
К «классическим» нарушениям в работе МКПП относят:
Мы оказываем консультации и принимаем заявки на ремонт грузовиков и заявки на подбор запчастей дистанционно и рады видеть Вас в числе наших клиентов и партнеров!
Смотрите также
16.09.2022 Wabco — гарантия безопасного вождения
16.09.2022 Ремонт и замена турбокомпрессора
16.09.2022 Ремонт рулевого управления, гидроусилителя руля
Вернуться к спискуНарушения контрольных точек иммунной системы при воспалительных миопатиях: обзор
Сохранить цитату в файл
Формат: Резюме (текст)PubMedPMIDAbstract (текст)CSV
Добавить в коллекции
- Создать новую коллекцию
- Добавить в существующую коллекцию
Назовите свою коллекцию:
Имя должно содержать менее 100 символов
Выберите коллекцию:
Не удалось загрузить вашу коллекцию из-за ошибки
Повторите попытку
Добавить в мою библиографию
- Моя библиография
Не удалось загрузить делегатов из-за ошибки
Повторите попытку
Ваш сохраненный поиск
Название сохраненного поиска:
Условия поиска:
Тестовые условия поиска
Эл. адрес:
(изменить)
адрес:
(изменить)
Который день? Первое воскресеньеПервый понедельникПервый вторникПервая средаПервый четвергПервая пятницаПервая субботаПервый деньПервый рабочий день
Который день? ВоскресеньеПонедельникВторникСредаЧетвергПятницаСуббота
Формат отчета: РезюмеРезюме (текст)АбстрактАбстракт (текст)PubMed
Отправить максимум: 1 шт. 5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
Отправить, даже если нет новых результатов
Необязательный текст в электронном письме:
Создайте файл для внешнего программного обеспечения для управления цитированием
Полнотекстовые ссылки
Эльзевир Наука
Полнотекстовые ссылки
Обзор
. 2018 авг; 17 (8): 746-754.
2018 авг; 17 (8): 746-754.
doi: 10.1016/j.autrev.2018.01.026. Epub 2018 6 июня.
Сандрин Гербелет 1
Принадлежности
- 1 Кафедра неврологии, Гентский университет и Гентская университетская больница, C. Heymanslaan 10, 9000 Гент, Бельгия. Электронный адрес: [email protected].
- 2 Кафедра неврологии, Гентский университет и Гентская университетская больница, C. Heymanslaan 10, 9000 Гент, Бельгия.
- PMID: 29885538
- DOI:
10.
 1016/j.autrev.2018.01.026
1016/j.autrev.2018.01.026
Обзор
Sandrine Herbelet et al. Аутоиммунный преп. 2018 авг.
. 2018 авг; 17 (8): 746-754.
doi: 10.1016/j.autrev.2018.01.026. Epub 2018 6 июня.
Авторы
Сандрин Гербелет 1 , Ян Л. Де Бликер 2
Принадлежности
- 1 Кафедра неврологии, Гентский университет и Гентская университетская больница, C. Heymanslaan 10, 9000 Гент, Бельгия. Электронный адрес: [email protected].
- 2 Кафедра неврологии, Гентский университет и Гентская университетская больница, C.

- PMID: 29885538
- DOI: 10.1016/j.autrev.2018.01.026
Абстрактный
Дерматомиозит (DM), полимиозит (PM), миозит с тельцами включения (IBM), иммуноопосредованная некротическая миопатия (IMNM) и перекрестный миозит (OM) классифицируются как воспалительные миопатии (IM) с участием аутоиммунных признаков, таких как аутореактивные лимфоциты и аутоантитела. Аутоиммунитет может быть определен как потеря самопереносимости и атака аутоантигенов иммунной системой. Самопереносимость достигается группой иммунных механизмов, возникающих в центральных и периферических лимфоидных органах и тканях, называемых иммунными контрольными точками, которые работают синергетически для защиты организма от вредных иммунных реакций. Аутоиммунные расстройства появляются, когда иммунные контрольные точки не работают. В этом обзоре обсуждаются различные сбои иммунных контрольных точек при DM, PM, IBM и IMNM. Изучение вклада исследований в каждую из этих иммунных контрольных точек может помочь осветить перспективы исследований в этой области и получить более полную картину патологии ИМ.
Аутоиммунные расстройства появляются, когда иммунные контрольные точки не работают. В этом обзоре обсуждаются различные сбои иммунных контрольных точек при DM, PM, IBM и IMNM. Изучение вклада исследований в каждую из этих иммунных контрольных точек может помочь осветить перспективы исследований в этой области и получить более полную картину патологии ИМ.
Ключевые слова: Дерматомиозит; Иммуноопосредованная некротизирующая миопатия; сбои контрольных точек иммунитета; миозит с тельцами включения; Полимиозит.
Copyright © 2018 Elsevier B.V. Все права защищены.
Похожие статьи
Патогенетические аспекты дерматомиозита, полимиозита и перекрестного миозита.
Герарди РК. Герарди РК. Пресс Мед. 2011 апр; 40 (4 часть 2): e209-18. doi: 10.1016/j.
 lpm.2010.12.013. Epub 2011 3 марта.
Пресс Мед. 2011.
PMID: 21376512
Обзор.
lpm.2010.12.013. Epub 2011 3 марта.
Пресс Мед. 2011.
PMID: 21376512
Обзор.Воспалительные миопатии и перекрывающиеся синдромы: обновление гистологического и серологического профиля.
Колафранческо С., Приори Р., Валезини Г. Колафранческо С. и соавт. Best Pract Res Clin Rheumatol. 2015 дек;29(6):810-25. doi: 10.1016/j.berh.2016.02.005. Epub 2016 16 марта. Best Pract Res Clin Rheumatol. 2015. PMID: 27107515 Обзор.
[Идиопатические воспалительные миопатии. Обзор].
Акоста И., Матамала Дж.М., Хара П., Пино Ф., Галлардо А., Вердуго Р. Акоста I и др. Преподобный Мед Чил. 2019 март; 147(3):342-355. doi: 10.4067/S0034-988720100342. Преподобный Мед Чил. 2019. PMID: 31344172 Обзор.
 Испанский.
Испанский.[Аутоантитела воспалительных миопатий: обновление].
Сузуки С. Судзуки С. Мозговой нерв. 2016 дек;68(12):1443-1451. doi: 10.11477/mf.1416200614. Мозговой нерв. 2016. PMID: 27916754 Японский язык.
Видеокапилляроскопические изменения ногтевого валика при дерматомиозите, антисинтетазном синдроме, перекрестном миозите и иммуноопосредованной некротизирующей миопатии.
Soubrier C, Seguier J, Di Costanzo MP, Ebbo M, Bernit E, Jean E, Veit V, Swiader L, Salort-Campana E, Attarian S, De Paula AM, Kaplanski G, Durand JM, Harlé JR, Schleinitz N . Soubrier C, et al. Клин Ревматол. 2019 дек;38(12):3451-3458. doi: 10.1007/s10067-019-04710-2. Epub 2019 22 августа. Клин Ревматол. 2019. PMID: 31440919
Посмотреть все похожие статьи
Цитируется
Непереносимость статинов, антитела к HMGCR и миозит, ассоциированный с ингибитором контрольной точки иммунного ответа: аутоиммунная токсичность «двух ударов» или клиническая предрасположенность?
фон Ицштейн М.
 С., Хан С., Попат В., Лу Р., Хан С.А., Фаттах Ф.Дж., Парк Дж.Ю., Бермас Б.Л., Карп Д.Р., Ахмед М., Салтарски Дж.М., Глория-МакКатчен И., Се И., Ли К.З., Уэйкленд Е.К., Гербер ДЭ.
фон Ицштейн М.С. и соавт.
Онколог. 2020 авг; 25(8):e1242-e1245. doi: 10.1634/теонколог.2019-0911. Epub 2020 3 июня.
Онколог. 2020.
PMID: 32400023
Бесплатная статья ЧВК.
С., Хан С., Попат В., Лу Р., Хан С.А., Фаттах Ф.Дж., Парк Дж.Ю., Бермас Б.Л., Карп Д.Р., Ахмед М., Салтарски Дж.М., Глория-МакКатчен И., Се И., Ли К.З., Уэйкленд Е.К., Гербер ДЭ.
фон Ицштейн М.С. и соавт.
Онколог. 2020 авг; 25(8):e1242-e1245. doi: 10.1634/теонколог.2019-0911. Epub 2020 3 июня.
Онколог. 2020.
PMID: 32400023
Бесплатная статья ЧВК.Аутоиммунитет в 2018 году.
Селми К. Селми С. Клин Рев Аллергия Иммунол. 2019 июнь; 56 (3): 375-384. doi: 10.1007/s12016-019-08745-w. Клин Рев Аллергия Иммунол. 2019. PMID: 31168760
Типы публикаций
термины MeSH
вещества
Полнотекстовые ссылки
Эльзевир Наука
Укажите
Формат: ААД АПА МДА НЛМ
Добавить в коллекции
- Создать новую коллекцию
- Добавить в существующую коллекцию
Назовите свою коллекцию:
Имя должно содержать менее 100 символов
Выберите коллекцию:
Не удалось загрузить вашу коллекцию из-за ошибки
Повторите попытку
Отправить по телефону
19.
 5: Нарушение контрольных точек клеточного цикла может вызвать рак
5: Нарушение контрольных точек клеточного цикла может вызвать рак- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 16538
- Джеральд Бергтром
- Университет Висконсин-Милуоки 9001
- Теперь отделено от Mdm2, Phospho-p53 активно активирует несколько генов, включая ген p21 .
- Белок P21 связывается с cdks ; циклинов не могут связываться с P21-cdks .
- Active Phospho-Chk2 катализирует фосфорилирование циклина; фосфоциклинов не могут связываться с p21-cdks .
- Неспособность циклинов связывать cdks специфически блокирует клеточный цикл между G 1 и S , а также фазы G 2 -к- M .

- , позволяя репарировать ДНК или другие клетки до возобновления нормального клеточного цикла, предотвращая нерегулируемые клеточные деления; после восстановления p53 и другие белки инактивируются и/или разрушаются, и клеточный цикл может возобновиться.
- Неспособность восстановить/исправить проблемы клеточного цикла запускает события, ведущие к апоптозу, тем самым также блокируя онкогенез путем уничтожения поврежденных клеток.
- Лучевая терапия основана на том факте, что большинство клеток в нашем организме не делятся, и направлена мутагенная радиация на опухоли в надежде, что реплицирующаяся ДНК будет мутирована в столь многих местах (т. е. в генах), что опухолевые клетки не смогут дольше выживают или размножаются должным образом.
- Химиотерапия используется для борьбы с опухолями, плохо реагирующими на облучение или труднодоступными для лучевых технологий, а также для борьбы с раковыми заболеваниями, которые даже не образуют очаговых опухолей (таких как лимфомы и лейкемии с вовлечением лимфоцитов и клеток крови) . Эти виды химиотерапии также направлены на нарушение репликации или митотической активности. Например, вспомните кордицепин (дидезоксиаденозинтрифосфат или ддАТФ). Присутствуя во время репликации, ddATP встраивается в растущую цепь ДНК, после чего в цепь ДНК не могут быть добавлены дополнительные нуклеотиды.
 Это делает ddATP мощным химиотерапевтическим разрушителем репликации. Таксол — еще один химиопрепарат, который действует в данном случае не за счет ингибирования репликации S-фазы, а за счет блокирования деполимеризации микротрубочек веретенообразных волокон, тем самым блокируя митотические анафазы и телофазы в последней части М- и С-фаз цикла. Колхицин (растительный алкалоид) атакует раковые (и другие делящиеся) клетки, блокируя образование микротрубочек и тем самым предотвращая образование веретенообразных волокон в митотической профазе.
Это делает ddATP мощным химиотерапевтическим разрушителем репликации. Таксол — еще один химиопрепарат, который действует в данном случае не за счет ингибирования репликации S-фазы, а за счет блокирования деполимеризации микротрубочек веретенообразных волокон, тем самым блокируя митотические анафазы и телофазы в последней части М- и С-фаз цикла. Колхицин (растительный алкалоид) атакует раковые (и другие делящиеся) клетки, блокируя образование микротрубочек и тем самым предотвращая образование веретенообразных волокон в митотической профазе. - , хотя они могут «вылечить» вас, они, скорее всего, не подействуют на кого-то другого.
- Подобно лучевой терапии и химиотерапии, иммунотерапия имеет свои неприятные, а иногда и серьезные побочные эффекты.
Если контрольная точка выходит из строя, или если клетка подвергается физическому повреждению хромосом во время клеточного деления, или если она страдает от изнурительной соматической мутации в предыдущей фазе S , она может самоуничтожиться в ответ на последующую биохимическую аномалию. Это еще один пример апоптоз . С другой стороны, когда клетки умирают от внешнего повреждения, они подвергаются некрозу , скорее случайной , чем запрограммированной смерти. В клетках, показанных ниже, химически индуцировали апоптоз или некроз, после чего идентифицировали как апоптоз или некроз с использованием флуоресцентных маркеров (йодид пропидия, зеленый; акридиновый оранжевый, оранжевый).
В клетках, показанных ниже, химически индуцировали апоптоз или некроз, после чего идентифицировали как апоптоз или некроз с использованием флуоресцентных маркеров (йодид пропидия, зеленый; акридиновый оранжевый, оранжевый).
Только зелено-флуоресцирующие (апоптотические) клетки в конечном итоге образуют апоптотические тельца. Напротив, некротические (флуоресцирующие оранжевым цветом) клетки теряют свои плазматические мембраны, не образуют таких «тел» и в конечном итоге распадаются. (400-кратное увеличение). Различия в ультраструктуре между некрозом и апоптозом также видны на электронных микрофотографиях колбочек и палочек (слева и справа соответственно) ниже. Звездочка указывает на цитоплазматическое набухание, характерное для некротического конуса. Белые стрелки указывают на ядра, характерные для апоптоза палочек.
Как мы уже отмечали, циклирующие клетки продолжают делиться до тех пор, пока не достигнут G 0 в терминально дифференцированном состоянии. Большинство терминально дифференцированных клеток очищаются апоптозом , когда они достигают конца своей эффективной жизни, чтобы быть замененными стволовыми клетками. Мы также отметили, что случайная передача сигналов может вывести клетки из G 0 , что приведет к возобновлению клеточной пролиферации. Хотя эти клетки явно аномальны, они не обнаруживаются механизмами защиты от апоптоза. Таким образом, они подвергаются неконтролируемому клеточному делению, становясь раковыми клетками. Точно так же физически поврежденные или мутировавшие клетки могут иногда не подвергаться апоптозному клиренсу. Когда они это сделают, они также могут стать раковыми клетками. Апоптотический клиренс и неконтролируемая пролиферация раковых клеток сравниваются ниже
Большинство терминально дифференцированных клеток очищаются апоптозом , когда они достигают конца своей эффективной жизни, чтобы быть замененными стволовыми клетками. Мы также отметили, что случайная передача сигналов может вывести клетки из G 0 , что приведет к возобновлению клеточной пролиферации. Хотя эти клетки явно аномальны, они не обнаруживаются механизмами защиты от апоптоза. Таким образом, они подвергаются неконтролируемому клеточному делению, становясь раковыми клетками. Точно так же физически поврежденные или мутировавшие клетки могут иногда не подвергаться апоптозному клиренсу. Когда они это сделают, они также могут стать раковыми клетками. Апоптотический клиренс и неконтролируемая пролиферация раковых клеток сравниваются ниже
346 Апоптоз (запрограммированная гибель клеток) и некроз
A. Белок P53 опосредует нормальный контроль клеточного цикла
Раковый рост может возникнуть, если нормальная делящаяся клетка подвергнется соматической мутации, которая нарушит нормальный контроль клеточного цикла. Подумайте, например, о чрезмерном выражении cdk . В качестве альтернативы представьте уровней циклина в дочерних клетках, которые никогда не падают; такие клетки никогда не перестанут циркулировать.
Подумайте, например, о чрезмерном выражении cdk . В качестве альтернативы представьте уровней циклина в дочерних клетках, которые никогда не падают; такие клетки никогда не перестанут циркулировать.
Другие возможности включают ячейку в G 0 , который стимулируется к возобновлению цикла из-за неподходящей встречи с гормоном или другим сигналом. Если их не обнаружить, эти аномалии могут трансформировать клетки в раковые. Белок p53 (показан ниже) представляет собой ДНК-связывающий белок, регулирующий гены, который выявляет некоторые из этих аномалий и позволяет делящимся клеткам восстанавливать повреждения, прежде чем пройти через контрольные точки клеточного цикла… или, если это не удастся, приведет к апоптозу. клетки.
Неудивительно, что мутации в гене белка P53 (называемого у людей TP53 ) связаны со многими видами рака человека (поджелудочной железы, легких, почечных клеток, молочной железы и т. д.). Половина случаев рака у человека связана с мутацией генов p53 . Таким образом, p53 является одним из класса белков-супрессоров опухолей . Исследования людей с состоянием, известным как LFS ( синдром Ли-Фраумени ), выявили по крайней мере одну мутацию р53 аллель . Мутация приводит к ~ 100% риску развития рака в течение всей жизни, начиная с детства. В культивируемых клетках мутагенизированные гены p53 проявляют ключевые характеристики раковых клеток, включая нерегулируемую клеточную пролиферацию и подавление апоптоза.
д.). Половина случаев рака у человека связана с мутацией генов p53 . Таким образом, p53 является одним из класса белков-супрессоров опухолей . Исследования людей с состоянием, известным как LFS ( синдром Ли-Фраумени ), выявили по крайней мере одну мутацию р53 аллель . Мутация приводит к ~ 100% риску развития рака в течение всей жизни, начиная с детства. В культивируемых клетках мутагенизированные гены p53 проявляют ключевые характеристики раковых клеток, включая нерегулируемую клеточную пролиферацию и подавление апоптоза.
1. Как работает p53
Белок p53 обычно связан с активным белком Mdm2 . Чтобы включить контрольные точки клеточного цикла, p53-Mdm2 должен быть отделен и храниться отдельно, чтобы дать p53 время для действия. В делящихся клетках физический стресс или химический стресс, например, повреждение ДНК во время роста клеток, могут активировать АТМ-киназа . Киназа ATM, в свою очередь, фосфорилирует Mdm2 , заставляя его диссоциировать от p53. Эта же киназа также фосфорилирует другую киназу, Chk2 , а также теперь «свободную» p53 . События, инициированные киназой ATM, более подробно описаны ниже.
Киназа ATM, в свою очередь, фосфорилирует Mdm2 , заставляя его диссоциировать от p53. Эта же киназа также фосфорилирует другую киназу, Chk2 , а также теперь «свободную» p53 . События, инициированные киназой ATM, более подробно описаны ниже.
Каждый из белков и ферментов, фосфорилированных киназой ATM, играет роль в функционировании контрольной точки клеточного цикла и остановке клеточного цикла при исправлении ошибок:
Эти опосредованные киназой события в контрольных точках клеточного цикла проиллюстрированы ниже.
Клеточный цикл остается остановленным, пока клетка пытается завершить основные биохимические процессы, необходимые для исправления вызванных стрессом или других физических или химических аберраций, прежде чем перейти к следующей фазе цикла. Если репарация ДНК или другие исправления успешны, клетка может перейти к следующей фазе.
Если нет, протеасомы нацелены на деградацию комплекса Chk2-циклин . Аналогичным образом любой P53 , остающийся связанным с нефосфорилированным Mdm2 , также подвергается разрушению протеасомами. В результате любая клетка, неспособная исправить последствия стресса или химического повреждения или восстановить повреждение ДНК, становится мишенью для апоптоза .
Уровни и активность p53 , а также других белков, обсуждавшихся выше, контролируют как количество 9Белок 0137 p53 , способный реагировать на аномалии клеточного цикла, и сам ответ. Фосфорилирование (активация) р53 приводит не только к быстрой остановке клеточного цикла, но и к активации генов, кодирующих белки, необходимые для репарации ДНК и белков, необходимых для апоптоза (в случае неудачи попыток репарации) . Взаимодействия p53 с различными белками, приводящие к альтернативным клеточным судьбам, суммированы ниже.
Фосфорилирование (активация) р53 приводит не только к быстрой остановке клеточного цикла, но и к активации генов, кодирующих белки, необходимые для репарации ДНК и белков, необходимых для апоптоза (в случае неудачи попыток репарации) . Взаимодействия p53 с различными белками, приводящие к альтернативным клеточным судьбам, суммированы ниже.
Подводя итог, можно сказать, что p53 подавляет рост злокачественных опухолей либо путем
Теперь должно быть ясно, почему мутант p53 , который уменьшает или устраняет выработку белка p21 или блокирует выработку необходимого белка репарации ДНК, позволяет поврежденным клеткам проникать в S и поддерживать их репликацию и деление, превращая их в раковые клетки. Интересно, что по сравнению с людьми от рака умирают лишь немногие киты или слоны, несмотря на то, что у них в тысячи раз больше клеток, чем у людей. Причина, по-видимому, в том, что, по крайней мере, у слонов целых 20 копий (40 аллелей) генов p53! Таким образом, мутация в одном аллеле одного из них может оказывать незначительное влияние, в то время как преобладают опухоле-репрессирующие эффекты остальных генов р53. Прочтите об этом недавнем исследовании на сайте Киты и слоны не болеют раком!
Интересно, что по сравнению с людьми от рака умирают лишь немногие киты или слоны, несмотря на то, что у них в тысячи раз больше клеток, чем у людей. Причина, по-видимому, в том, что, по крайней мере, у слонов целых 20 копий (40 аллелей) генов p53! Таким образом, мутация в одном аллеле одного из них может оказывать незначительное влияние, в то время как преобладают опухоле-репрессирующие эффекты остальных генов р53. Прочтите об этом недавнем исследовании на сайте Киты и слоны не болеют раком!
2. Центральное место действия p53 в регуляции клеточного цикла
Из-за его многочисленных ролей в регуляции и содействии репарации ДНК, а также в контроле контрольных точек клеточного цикла p53 был назван « Хранителем генома »! Вот еще одно свидетельство этой центральной роли.
a) «Онкогенные вирусы»
Вирусы, вызывающие рак, включают вирус папилломы человека ( HPV ), вирус Эпштейна-Барр ( EBV ), вирус иммунодефицита человека ( ВИЧ ), вирусы гепатита В и С ( HBV, HCV ), вирус герпеса человека 8 ( HHV-8 ) и обезьяний вирус 40 ( SV40 ).
Доказана связь между SV40, p53 и раком. SV40 является вирусным контаминантом вакцин против полиомиелита, которые использовались в 1960-х годах. Вирус является онкогенным у млекопитающих, хотя связь SV40 и рака у людей не доказана. В инфицированных клетках ДНК SV40 проникает в ядро, где может интегрироваться в геном клетки-хозяина. Инфекции SV40 обычно латентны (т. е. не причиняют вреда). Однако активация может привести к клеточной трансформации и росту злокачественных сарком в мышцах, а также опухолей в других органах. РНК-полимераза II в инфицированных клетках транскрибирует гены SV40, продуцируя белки, которые реплицируют и инкапсулируют вирусную ДНК в мембрану для создания новых вирусных частиц. Однако относительно небольшой геном SV40 не кодирует все ферменты и факторы, необходимые для репликации вирусной ДНК. Инфицированные клетки сами обеспечивают эти факторы, производя их только в течение 9 дней.0137 S фаза. В это время большой Т-антиген SV40 (образующийся вскоре после инфицирования) проникает в ядро клетки-хозяина, где он регулирует транскрипцию генов, необходимых для репликации вируса и образования вирусных частиц. Большой Т-антиген также связывается с p53 , препятствуя транскрипции белков, гены которых регулируются p53 . Неспособная выполнять функции контрольной точки, клетка-хозяин бесконтрольно делится, образуя раковые опухоли. Дерегуляция клеточного цикла на большой Т-антиген обеспечивает переход к S-фазе и нерегулируемую корепликацию ДНК вируса и клетки-хозяина.
Большой Т-антиген также связывается с p53 , препятствуя транскрипции белков, гены которых регулируются p53 . Неспособная выполнять функции контрольной точки, клетка-хозяин бесконтрольно делится, образуя раковые опухоли. Дерегуляция клеточного цикла на большой Т-антиген обеспечивает переход к S-фазе и нерегулируемую корепликацию ДНК вируса и клетки-хозяина.
b) p53 и передача сигнала
Стресс может активировать пути передачи сигнала. Например, мутации, влияющие на сигнальный путь MAPK (MAP kinase), могут приводить к онкогенезу. Это можно объяснить наблюдением, что при активации путь MAPK приводит к усиленной продукции киназы, которая фосфорилирует p53 . Активный фосфо-р53 , в свою очередь, усиливает активацию пути передачи сигнала МАРК. Вы можете вспомнить, что передача сигнала MAPK обычно заканчивается митогенным ответом.
Другим примером взаимодействия p53 является белок FAK ( киназа фокальной адгезии ). Активность FAK повышается за счет интегрина опосредованной передачи сигнала. Напомним, что мембранные интегрины связывают фибронектин , способствуя образованию внеклеточного матрикса, или ЕСМ . Повышенная активность FAK участвует в регуляции адгезии клетка-клетка и клетка-ВКМ в фокальных точках адгезии . Другая роль FAK заключается в непосредственном связывании с неактивным p53 и увеличении связывания p53-Mdm2. Как мы только что видели, устойчивый p53-Mdm2 нацелен на убиквитинирование… и окончательное уничтожение! Фактически, аномально высокие уровни FAK связаны со многими различными линиями опухолевых клеток (толстая кишка, молочная железа, щитовидная железа, яичники, меланома, саркома…). Это происходит, когда p53 не может должным образом активировать контрольные точки клеточного цикла.
Активность FAK повышается за счет интегрина опосредованной передачи сигнала. Напомним, что мембранные интегрины связывают фибронектин , способствуя образованию внеклеточного матрикса, или ЕСМ . Повышенная активность FAK участвует в регуляции адгезии клетка-клетка и клетка-ВКМ в фокальных точках адгезии . Другая роль FAK заключается в непосредственном связывании с неактивным p53 и увеличении связывания p53-Mdm2. Как мы только что видели, устойчивый p53-Mdm2 нацелен на убиквитинирование… и окончательное уничтожение! Фактически, аномально высокие уровни FAK связаны со многими различными линиями опухолевых клеток (толстая кишка, молочная железа, щитовидная железа, яичники, меланома, саркома…). Это происходит, когда p53 не может должным образом активировать контрольные точки клеточного цикла.
Хотя взаимодействия, подразумеваемые здесь, сложны и активно изучаются, эти действия p53 определенно подтверждают его центральную роль как защитника генома и защитника клеточного деления .
B. Рост и поведение раковых клеток
Различные типы раковых клеток имеют разные ростовые и другие поведенческие свойства. Возможно, вы слышали о медленно растущих и быстрорастущих раковых заболеваниях. Колонка раки обычно медленно растут. Периодические колоноскопии , выявляющие и удаляющие колоректальные опухоли у людей среднего и пожилого возраста, могут предотвратить заболевание (хотя риски заболевания и сама процедура должны быть сбалансированы). Рак поджелудочной железы быстро растет и обычно остается незамеченным, пока не достигнет поздней стадии. Двумя целями медицинских исследований являются обнаружение различных видов рака на достаточно ранней стадии для успешного вмешательства и, конечно же, поиск эффективных методов лечения.
Единственная мутировавшая клетка в ткани может стать точкой роста опухоли , по сути, массы клеток, клонированных из исходной мутировавшей. Доброкачественные опухоли или новообразования (например, груди и матки миомы у женщин или обычные родинки у любого из нас) перестают расти и не опасны для жизни. Их часто удаляют хирургическим путем для удобства пациента (или потому, что клетки в некоторых других доброкачественных опухолях могут стать раковыми).
Их часто удаляют хирургическим путем для удобства пациента (или потому, что клетки в некоторых других доброкачественных опухолях могут стать раковыми).
Злокачественные опухоли (также называемые злокачественными новообразованиями ) являются раковыми и могут расти за пределами самой опухоли. Когда опухолевые клетки выделяются, они могут попадать в кровоток и перемещаться в другие части тела, явление, называемое метастазированием . Раковые клетки, которые метастазируют, могут стать очагом образования новых опухолей во многих различных тканях. Поскольку раковые клетки продолжают циклически повторять свою ДНК, они могут подвергаться еще большему количеству соматических мутаций. Эти дальнейшие изменения могут способствовать метастазированию и росту раковых клеток в разных частях тела.
C. Стратегии лечения рака
Существует множество различных видов рака, возникающих в различных тканях организма. Все они разделяют свойство неконтролируемого клеточного деления, хотя и по разным молекулярным и не всегда понятным причинам. Две основные стратегии лечения рака, разработанные в 20 веке, направлены на то, чтобы каким-то образом нарушить репликацию.
Две основные стратегии лечения рака, разработанные в 20 веке, направлены на то, чтобы каким-то образом нарушить репликацию.
Эти методы лечения не эффективны против всех видов рака, и, конечно же, они не нацелены на определенные виды раковых клеток. Их успех основан просто на том факте, что раковые клетки быстро и постоянно размножаются, в то время как другие типы клеток этого не делают. Многие, если не все, побочные эффекты лучевой и химиотерапии возникают в результате повреждения нормальных делящихся клеток (например, клетки волосяных фолликулов вызывают выпадение волос у многих больных раком, истощение клеток крови, которые не могут быть заменены стволовыми клетками в костной ткани). костный мозг).
костный мозг).
В настоящее время многие исследования сосредоточены на мобилизации собственной иммунной системы организма для создания более специфических, целенаправленных методов лечения рака. В захватывающей истории более 100 лет назад доктор Уильям Б. Коли ввел неизлечимому больному раком стрептококковые бактерии, которые затем избавились от опухоли после выздоровления от инфекции (подробности см. Испытания). Феномен «Dr. Токсины Коли изначально считались противоопухолевым эффектом бактерий. Но к 1948 это широко связывали с иммунным ответом, активируемым инфекцией. В 1990-х годах ученые вновь обратились к иммунному ответу на рак, и на рубеже 21-го века исследования иммунотерапии рака набрали обороты (и более существенное финансирование исследований!).
Недавние эксперименты по иммунотерапии на животных и клинические испытания на людях являются многообещающими. Несколько видов иммунотерапии уже одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA). Стратегии иммунотерапии рака основаны на том факте, что ваше тело иногда распознает маркеры раковых клеток (например, молекулы клеточной поверхности) как чужеродные, тем самым создавая иммунную защиту против этих клеток. Но этот ответ иногда недостаточно силен, чтобы уничтожить новые, быстро делящиеся раковые клетки. Рак, по-видимому, возникает, когда иммунный ответ слаб. Существуют разные, иногда пересекающиеся подходы к иммунотерапии рака. Все они основаны на том факте, что раковые клетки каким-то образом мутировали и производят аберрантные белки, которые иммунная система может воспринимать как достаточно чужеродные, чтобы вызвать иммунный ответ, каким бы слабым он ни был. Некоторые виды иммунотерапии стремятся усилить этот иммунный ответ. Другие стремятся изолировать или создать уникальные антигены раковых клеток, которые будут иммунизировать пациента при введении этих раковых антигенов. Некоторые виды иммунотерапии приведены в таблице на следующей странице. Как видно из таблицы, иммунотаргетирование раковых клеток уже доказало свою высокую эффективность.
Стратегии иммунотерапии рака основаны на том факте, что ваше тело иногда распознает маркеры раковых клеток (например, молекулы клеточной поверхности) как чужеродные, тем самым создавая иммунную защиту против этих клеток. Но этот ответ иногда недостаточно силен, чтобы уничтожить новые, быстро делящиеся раковые клетки. Рак, по-видимому, возникает, когда иммунный ответ слаб. Существуют разные, иногда пересекающиеся подходы к иммунотерапии рака. Все они основаны на том факте, что раковые клетки каким-то образом мутировали и производят аберрантные белки, которые иммунная система может воспринимать как достаточно чужеродные, чтобы вызвать иммунный ответ, каким бы слабым он ни был. Некоторые виды иммунотерапии стремятся усилить этот иммунный ответ. Другие стремятся изолировать или создать уникальные антигены раковых клеток, которые будут иммунизировать пациента при введении этих раковых антигенов. Некоторые виды иммунотерапии приведены в таблице на следующей странице. Как видно из таблицы, иммунотаргетирование раковых клеток уже доказало свою высокую эффективность. В некоторых случаях терапия представляет собой пример персонализированная медицина , в которой лечение индивидуально адаптировано для вас как пациента. Проблемы с иммунотерапией заключаются в том, что они требуют много времени и труда, а их производство дорого.
В некоторых случаях терапия представляет собой пример персонализированная медицина , в которой лечение индивидуально адаптировано для вас как пациента. Проблемы с иммунотерапией заключаются в том, что они требуют много времени и труда, а их производство дорого.
Более подробное обсуждение иммунотерапии рака находится на Cancer.gov веб-сайт компании Cancer Treatment Immunotherpay.
ПРИМЕЧАНИЕ. Термин ингибитор контрольных точек в контексте иммунотерапии отличается от термина контрольных точек , описывающего порталы для прохождения эукариотического клеточного цикла.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- Джеральд Бергтром
- Лицензия
- СС BY
- Показать оглавление
- нет
- Теги



 1016/j.autrev.2018.01.026
1016/j.autrev.2018.01.026
 lpm.2010.12.013. Epub 2011 3 марта.
Пресс Мед. 2011.
PMID: 21376512
Обзор.
lpm.2010.12.013. Epub 2011 3 марта.
Пресс Мед. 2011.
PMID: 21376512
Обзор. Испанский.
Испанский. С., Хан С., Попат В., Лу Р., Хан С.А., Фаттах Ф.Дж., Парк Дж.Ю., Бермас Б.Л., Карп Д.Р., Ахмед М., Салтарски Дж.М., Глория-МакКатчен И., Се И., Ли К.З., Уэйкленд Е.К., Гербер ДЭ.
фон Ицштейн М.С. и соавт.
Онколог. 2020 авг; 25(8):e1242-e1245. doi: 10.1634/теонколог.2019-0911. Epub 2020 3 июня.
Онколог. 2020.
PMID: 32400023
Бесплатная статья ЧВК.
С., Хан С., Попат В., Лу Р., Хан С.А., Фаттах Ф.Дж., Парк Дж.Ю., Бермас Б.Л., Карп Д.Р., Ахмед М., Салтарски Дж.М., Глория-МакКатчен И., Се И., Ли К.З., Уэйкленд Е.К., Гербер ДЭ.
фон Ицштейн М.С. и соавт.
Онколог. 2020 авг; 25(8):e1242-e1245. doi: 10.1634/теонколог.2019-0911. Epub 2020 3 июня.
Онколог. 2020.
PMID: 32400023
Бесплатная статья ЧВК.
 Это делает ddATP мощным химиотерапевтическим разрушителем репликации. Таксол — еще один химиопрепарат, который действует в данном случае не за счет ингибирования репликации S-фазы, а за счет блокирования деполимеризации микротрубочек веретенообразных волокон, тем самым блокируя митотические анафазы и телофазы в последней части М- и С-фаз цикла. Колхицин (растительный алкалоид) атакует раковые (и другие делящиеся) клетки, блокируя образование микротрубочек и тем самым предотвращая образование веретенообразных волокон в митотической профазе.
Это делает ddATP мощным химиотерапевтическим разрушителем репликации. Таксол — еще один химиопрепарат, который действует в данном случае не за счет ингибирования репликации S-фазы, а за счет блокирования деполимеризации микротрубочек веретенообразных волокон, тем самым блокируя митотические анафазы и телофазы в последней части М- и С-фаз цикла. Колхицин (растительный алкалоид) атакует раковые (и другие делящиеся) клетки, блокируя образование микротрубочек и тем самым предотвращая образование веретенообразных волокон в митотической профазе.