Плотность электролита в разряженном аккумуляторе — как определить плотность автомобильного электролита в АКБ
В каждой свинцово-кислотной батарее с жидким диэлектриком существует такой параметр, как плотность электролита в аккумуляторе. Он показывает концентрацию активного вещества в растворе, выполняющего роль транспортера зарядов между электродами. Важно, чтобы в нем было определенное количество серной кислоты по отношению к дистиллированной воде. Рассмотрим основные проблемы с плотностью и методы ее нормализации.
Устройство аккумулятора
Чтобы понять, что такое плотность электролита в аккумуляторе, нужно знать устройство АКБ. Батарея представляет собой пластиковый ящик, внутри которого имеется 6 отсеков с перегородками. В каждом из них находится пакет парных пластин, анод и катод. Между пластинами находится сепаратор или одна из них погружена в него. Каждый электрод представляет собой решетку с окнами определенной конфигурации. Ее рассчитывают так, чтобы электроны лучше распределялись по поверхности пластин, тем самым, отдавая больший ток в нагрузку. Пакеты пластин сформированы в энергетические ячейки, соединенные между собой последовательно. Каждая ячейка или банка выдает 2,1 В, все 6 — 12,6 В. Выводы размещены снаружи корпуса и имеют конусовидную форму в европейских и азиатских батареях.
Пакеты пластин сформированы в энергетические ячейки, соединенные между собой последовательно. Каждая ячейка или банка выдает 2,1 В, все 6 — 12,6 В. Выводы размещены снаружи корпуса и имеют конусовидную форму в европейских и азиатских батареях.
Конструкция батарей может несколько отличаться от одной серии батарей к другой. В АКБ современного типа имеется лабиринтная структура в крышке для рециркуляции электролита. Также есть индикатор заряда, но нет пробок для обслуживания путем доливки дистиллированной воды. Мы же говорим о тех, в которые можно доливать дистиллят и измерить плотность электролита в источнике питания.
Особенности обслуживания АКБ
Каким-либо образом повлиять на работоспособность автомобильного аккумулятора мы не в состоянии, за исключением проведения правильного обслуживания. Достаточно регулярно проверять величину напряжения и плотность электролита. Особенно важно это делать на 3-4 году эксплуатации батареи. У современного источника тока Ca/Ca, AGM или Gel это проделать невозможно.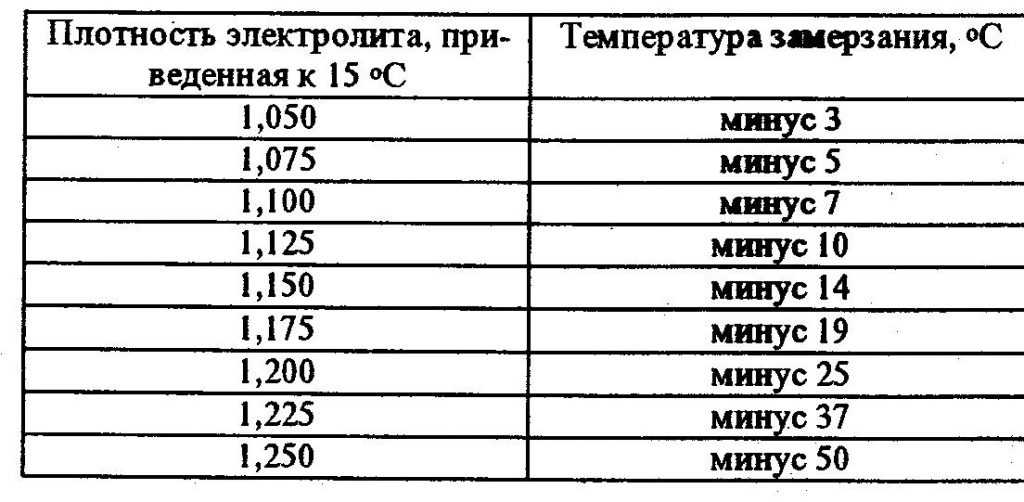 В EFB АКБ еще имеется индикатор, в других нет даже его, так как жидкого электролита в аккумуляторе тоже нет.
В EFB АКБ еще имеется индикатор, в других нет даже его, так как жидкого электролита в аккумуляторе тоже нет.
Использование ареометра
Замер плотности электролита в аккумуляторе свинцово-сурьмянистом и сурьмянисто-кальциевом выполняется при помощи специального прибора — ареометра. Он представляет собой запаянную с двух сторон стеклянную трубку. У нее имеется утонченная нижняя часть и зауженная верхняя. На узкой части есть шкала с разметкой под конкретные типы измеряемых жидкостей. В толстой части внутри находится дробь. Устройство погружается в емкость с электролитом при измерении плотности, работает по закону Архимеда. Погружаемое в жидкость тело вытесняет пропорциональное количество вещества.
Для измерения плотности электролита в аккумуляторе нужно знать ее нормированное значение. Данный показатель зависит от условий, состава, интенсивности эксплуатации и уровня заряда батареи. Она должна быть такой, как указано в таблице.
|
Значение плотности, г/см3 |
Величина напряжения, В |
Уровень заряда, % |
|
<1,12 |
<11,6 |
глубокий разряд |
|
1,15 |
11,8-11,9 |
25 |
|
1,19 |
12,0-12,1 |
50 |
|
1,22 |
12,3-12,4 |
75 |
|
1,26 |
12,6-12,7 |
100 |
Теоретически определить плотность раствора в батарее можно по этим данным, но так ли это на самом деле? Определить соответствие реально только с помощью ранее описанного прибора.
Важно. Зимой уровень плотности будет завышен на 0,2-0,4г/см3. Это считается нормальным показателем. Дистиллированная вода замерзает, из-за чего расстояние между молекулами увеличивается, и соотношение серной кислоты к объему воды именно в жидком виде повышается, так как сама кислота зимой не замерзает. Также значение плотности электролита в аккумуляторной батарее зависит от температуры окружающей среды. Указанные в таблице значения определены при +25 градусах. Если за бортом -30 градусов и батарея разряжена на 25%, то нормальной плотностью является 1,28 г/см3.
Низкая плотность занижает показатель заряда, высокая плотность приводит к ускоренному процессу разрушения электродных пластин и активной пасты. Следует поддерживать ее на среднем уровне, указанном в табличных данных.
Процедура измерения плотности ареометром
По ранее представленным данным мы уже знаем, какой должна быть плотность электролита при определенном значении напряжения на клеммах аккумулятора.
Процесс измерения значения плотности электролита в батарее:
- Зарядите аккумулятор полностью.
- Перенесите батарею в теплое место, где температура не ниже +20 градусов, и оставьте ее стоять на 6-10 часов.
- Выверните пробки в источнике питания. В сурьмянистых и недорогих гибридных они видны прямо на крышке, в более дорогих находятся под специальной планкой.
- Погрузите прибор в автомобильный аккумулятор и наберите немного электролитического раствора. Используем устройство с грушей и плавающим внутри ареометром.
- Подождите, когда индикатор стабилизируется, и запомните значение по шкале напротив него.
- Проделайте аналогичную операцию с каждой из 6-ти банок и запишите все показания.
По мере испарения воды, что происходит постоянно при каждом цикле зарядки автомобильного источника тока, уровень раствора падает и плотность увеличивается, так как концентрация кислоты по отношению к воде растет. Раствор нужно разбавить ровно на то количество воды в долях, на которые выше плотность по отношению к нормальному состоянию.
Раствор нужно разбавить ровно на то количество воды в долях, на которые выше плотность по отношению к нормальному состоянию.
Полезно узнать, сколько раствора и воды должно быть в батарее. Уровень воды зависит от емкости аккумулятора. Если у вас стоит батарея 55 А/ч, то общее количество раствора составляет 2,5 л. Воды, соответственно, 1,63 л. В АКБ 65 А/ч содержится 3,5 л раствора и 2,28 л воды. Низкая плотность говорит о большом уровне дистиллята, высокая — о низкой концентрации.
Какой аккумулятор устанавливается на Шевроле Лачетти >
Инструкция по эксплуатации тяговых аккумуляторных батарей
Обслуживание и уход за батареями.
Правила ухода за тяговой аккумуляторной батареей, рекомендованные всеми производителями ведущих марок АКБ.
В качестве примера рассмотрена классическая батарея немецкого концерна Hawker Gmbh — Perfect Plus. Ничего сложного в уходе за батареей нет. Необходимо лишь четко по инструкции и в определенные сроки производить ряд операций, которые позволят максимально долго работать приобретенной Вами батарее, а значит, — сэкономит Ваши средства.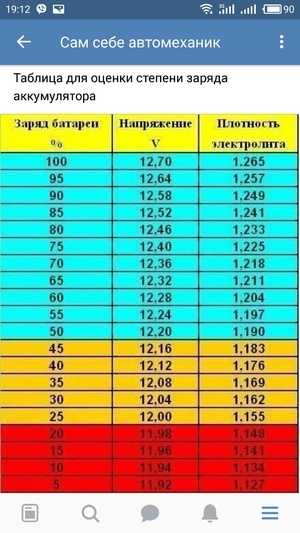
Особые свойства свинцовых батарей:
Емкость 5-ти часовая, т.е. номинальная емкость может быть получена при разряде постоянным током в течение 5 часов до установленного конечного напряжения разряда 1,7 В/элемент при исходной температуре ЗО С.
Напряжение Номинальное напряжение одного аккумулятора составляет 2 В. Нормы номинального напряжения тяговых батарей: 24 В, 48 В, 72В, 80 В.
Рабочее напряжение одной тяговой батарей зависит от величины тока разряда, степени разряда и температуры. Установленное конечное напряжение разряда при 5-ти часовом разряде составляет 1,7 В/элемент.
Плотность электролита в полностью заряженном состоянии, при температуре ЗО С составляет 1,29 кг/л.
Стойкость и срок службы батарей. Под стойкостью понимается результат длительного испытания в лабораторных условиях, при которых батарея подвергается циклам заряд-разряд по точно определенной программе.
 Следует получить как минимум такое количество циклов, которое не приведет к снижению емкости ниже 80% от ее номинальной величины. Соответствующая методика изложена в DIN 43539, часть 3.
Следует получить как минимум такое количество циклов, которое не приведет к снижению емкости ниже 80% от ее номинальной величины. Соответствующая методика изложена в DIN 43539, часть 3.
Действительный срок службы может быть больше или меньше чем стойкость, так как многочисленные факторы воздействия при эксплуатации ведут к нагрузкам, отличным от нагрузок в лабораторных условиях.
Факторы воздействия, ведущие к увеличению срока службы батареи:
безупречные уход и обслуживание
нормальная нагрузка
нормальные рабочие температуры (от 20 С до 40 С)
безупречные зарядные устройства
избегать глубоких разрядов
своевременное устранение неисправностей
Воздействия, ведущие к сокращению срока службы:
частые глубокие разряды, т.е. снятие более 80% номинальной емкости
повышенные рабочие температуры (> 40 С) в течение длительного времени
заряд недопустимо высоким током после достижения напряжения газообразования (2,4 В/элемент)
- нахождение батареи в разряженном состоянии
наличие примеси, попавшей в электролит (например воды для долива, не соответствующей требованиям)
перегрузка или короткое замыкание
Обслуживание и уход за тяговыми батареями Общие правила эксплуатации:
Никогда не оставлять батарею в разряженном состоянии, а сразу провести повторный заряд.

Для достижения оптимального срока службы избегать разрядов более80% номинальной емкости; при этом плотность электролита не должна быть ниже 1,13 кг/л (300С).
Во избежание глубоких разрядов необходимо следить за разрядом аккумуляторов транспортных средств.
Рабочая температура должна соответствовать 20 С – 40 С.
Во избежание повреждений батареи нельзя превышать максимально допустимую температуру электролита 55 С.
Перед зарядом и при промежуточных зарядах необходимо обязательно снять или открыть крышку контейнера или закрывающее устройство батареи. Закрыть не ранее чем через 1/2 часа после окончания заряда.
Зарядные устройства должны соответствовать емкости батареи и требуемому времени заряда.
Для долива используется только дистиллированная вода согласно DIN 43530 часть 4, не следует доливать кислоту или применять добавки.
Заряд батареи (ежедневные работы):
Необходимо отключить батарею путем отсоединения штекера от розетки .
 удалить крышку батареи. При этом пробки остаются закрытыми.
удалить крышку батареи. При этом пробки остаются закрытыми.Проверить уровень электролита на отметке «мин».
После этого необходимо измерить температуру электролита. При превышении 45 С — охладить.
Подключить штекер. При необходимости соединить систему перемешивания электролита (для штекеров без интегрированной системы вывода воздуха).
Включить зарядное устройство или проверить, включено ли устройство.
Начать процесс зарядки батареи.
После зарядки отключить зарядное устройство или проверить, отключено ли устройство, затем отсоединить батарею от зарядного устройства. При необходимости проверить конечные результаты.
При недостаточном заряде или после глубокого заряда провести уравнительный заряд.
Очистка (ежедневные работы):
Грязь и пыль, которые скапливаются на поверхности элементов во время работы, необходимо удалять в зависимости от потребностей и от эксплуатации батареи (ветошь, влажный пар от 100 С до 150 С, с помощью шланга с насадкой).

Долив воды (еженедельные работы):
Необходимо также вести контроль уровня электролита. По крайней мере, один раз в неделю. В том случае, если нет автоматического долива, сделать долив очищенной воды согласно DIN 43530 часть 4 в конце заряда.
После заряда необходимо проверить уровень электролита во всех элементах и дополнить его дистиллированной водой.
Необходимо также один раз в неделю проводить уравнительный заряд.
Напряжение, плотность и температура (ежемесячные работы):
Один раз в месяц необходимо провести работу по проверке всех элементов на равномерность выделения газа.
После окончания заряда или уравнительного заряда следует измерить плотность кислоты и температуру и выборочно внести в технологическую карту батареи отклонения от нормативных величин.
Если были установлены существенные различия между элементами, то такие элементы необходимо исследовать отдельно.

Также необходимо измерить напряжение, плотность и температуру элементов.
Работы, выполняемые каждое полугодие и каждый год: .
проверить правильность функционирования зарядного устройства, в первую очередь ток заряда в начале газовыделения (2,4 В/элемент) и в конце заряда.
проверить штекер и штекерное устройство.
исправить небольшие повреждения изоляции контейнера (нанесенный слой) сразу после удаления или нейтрализации следов кислоты (соблюдать рекомендации изготовителя).
следует измерить сопротивление изоляции батарей по отношению к массе в соответствии с DIN 43539 часть 1 при разомкнутой внешней электрической цепи.
измерить сопротивление изоляции: 50 Ом на каждый Вольт номинального напряжения.
почистить батарею при плохом со противлении изоляции.
Хранение
В случае, если в течение длительного периода не планируется эксплуатация батарей, их хранение должно производиться в полностью заряженном состоянии в сухом помещении при температуре выше 0 С.
Для поддержания эксплутационной готовности батареи следует использовать следующие зарядные режимы:
Ежемесячный уравнительный заряд
Поддерживающий заряд при зарядном напряжении 2,23 В х количество элементов (30 С)
Как избежать повреждений и несчастных случаев?
Во избежание повреждений, коротких замыканий, искр, не класть металлические предметы и инструменты на батареи.
Транспортировать батареи только посредством соответствующих подъемных устройствах (согласно VDE 3616).
При работе с батареями следует соблюдать соответствующие правила техники безопасности, а также DIN VDE 0510 и VDE 0105 часть 1.
Срок хранения
Следует учитывать влияние срока хранения на срок службы батареи. Следует помнить, что правильно выбранные подъемные устройства препятствуют деформированию корпуса батареи и защищают таким образом покрытие контейнера. Подъемные устройства должны соответствовать геометрии батареи.
Подъемные устройства должны соответствовать геометрии батареи.
Рекомендации для взрывоопасных батарей
Речь идет о батареях, которые эксплуатируются в зонах повышенной взрывоопасности. Крышки корпуса батареи во время заряда и последующего отвода газов должны быть открыты с тем, чтобы образующаяся взрывоопасная газовая смесь при достаточной вентиляции потеряла свою способность к возгоранию.
Как химический состав батареи определяет производительность
Химические реакции в батарее лежат в основе конструкции батареи Хорошо спроектированные батареи обеспечивают эффективное, надежное и безопасное питание вашего оборудования в течение длительного срока службы. Чтобы достичь этой комбинации идеалов, инженеры оценивают определенные параметры конструкции, включая требуемое напряжение и мощность, продолжительность рабочего цикла, температурные условия, цену и многое другое, чтобы определить свой выбор конструкции.
Химический состав аккумуляторов, возможно, является наиболее фундаментальным выбором при проектировании. По своей сути все батареи представляют собой удобно упакованные электрохимические реакции. Способность батареи накапливать и разряжать электричество напрямую зависит от типа химической реакции.
В этой статье мы подробно рассмотрим, как химия влияет на производительность. Затем мы рассмотрим свойства некоторых распространенных химических веществ.
Для разработка, тестирование и производство индивидуального блока батарей выберите Ave. Мы создадим аккумуляторные блоки, идеально подходящие для вашего конкретного применения. Свяжитесь с нами по телефону для получения дополнительной информации о процессе или запросите предложение сегодня .
Химический состав батарей влияет на напряжение, плотность энергии, способность к перезарядке, саморазряд, срок службы и безопасность.
Блок батарей состоит из одного или нескольких упакованных модулей батарей. Батарейный модуль состоит из гальванических элементов, расположенных параллельно или последовательно. Электрохимический элемент, также называемый гальваническим элементом, состоит из трех основных частей: анода , катода и электролита . Вместе анод, катод и электролит обеспечивают произойдет реакция окисления/восстановления .
Реакции окисления/восстановления связаны с потоком электронов . Когда железо окисляется, атомы железа отдают электроны, а молекулы кислорода приобретают электроны. Разница между ржавым куском металла и батареей заключается в разделении этих двух событий. Это заставляет электроны течь по цепи, чтобы завершить реакцию. При разряде анод теряет электроны, а катод их приобретает. Электролит способствует этим реакциям и позволяет ионам существовать в растворе.
Во время разрядки аккумулятора анод окисляется и отдает электроны. Электроны текут по цепи к катоду, вызывая реакцию восстановления. Электролит обеспечивает обмен ионами. При зарядке аккумулятора процесс обратный. Состав анода, катода и электролита изменяет многие свойства батареи.
Электроны текут по цепи к катоду, вызывая реакцию восстановления. Электролит обеспечивает обмен ионами. При зарядке аккумулятора процесс обратный. Состав анода, катода и электролита изменяет многие свойства батареи.
Вот некоторые электрические свойства, которые зависят от химического состава батареи:
Напряжение элемента
Все гальванические элементы одного химического состава производят одинаковое номинальное напряжение . Это связано с тем, что напряжение напрямую связано с благоприятностью реакции окисления/восстановления. Более благоприятные реакции производят более высокие напряжения. Например, литий-ионные аккумуляторы имеют номинальное напряжение около 3,6 В.
Плотность энергии
Напряжение — не единственный показатель ценности батареи. Вы можете получить любое необходимое вам напряжение и ток при правильном расположении ячеек последовательно и параллельно. В зависимости от ваших потребностей, это может быть тяжелым, громоздким и дорогим.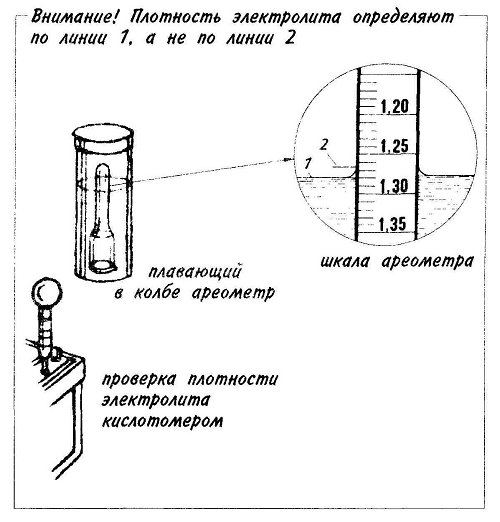 Плотность энергии измеряет энергию, запасенную батареей, по отношению к ее размеру. Гравиметрическая плотность энергии измеряется в ватт-часах на килограмм (Втч/кг).
Плотность энергии измеряет энергию, запасенную батареей, по отношению к ее размеру. Гравиметрическая плотность энергии измеряется в ватт-часах на килограмм (Втч/кг).
Перезаряжаемость
Общеизвестно, что химические реакции протекают в двух направлениях. Вы можете начать с реагентов и получить продукты или использовать продукты для повторного получения реагентов. Если вы примените обратное напряжение и ток, вы можете заставить анод принимать электроны, а катод отдавать их, перезаряжая батарею — по крайней мере, в теории. На практике отменить некоторые реакции может быть чрезвычайно сложно. Первичные элементы — это батареи, химический состав которых делает их перезарядку неэкономичной или небезопасной. Это одноразовые батарейки. Вторичные элементы , также известные как перезаряжаемые батареи, основаны на легко обратимой электрохимии. В этой статье мы сосредоточимся на химии вторичных клеток.
Саморазряд и срок службы
В идеальном мире мы могли бы заряжать и разряжать батареи снова и снова без потери производительности или оставлять их на полке на месяцы без потери заряда. В реальном мире гальванические элементы страдают от нежелательных химических реакций. Пока батарея лежит на полке, происходят спонтанные химические реакции, которые истощают заряд батареи. это называется саморазряд .
Аналогичным образом, когда батарея заряжается и разряжается, происходят нежелательные химические реакции, которые снижают способность батареи накапливать электричество. Количество циклов, которое батарея может использовать до того, как она перестанет работать должным образом, составляет циклов жизни .
Как скорость саморазряда, так и продолжительность срока службы зависят от химического состава батареи. Однако они также зависят от условий использования и хранения.
Экономика, окружающая среда и безопасность
Наконец, примите во внимание экологические и экономические соображения. Некоторые химические вещества для аккумуляторов просто дороже других. Литий-ионные элементы популярны и не зря, но нехватка металлического лития делает их дорогими.
Некоторые химические вещества для аккумуляторов просто дороже других. Литий-ионные элементы популярны и не зря, но нехватка металлического лития делает их дорогими.
В своих экономических расчетах также следует учитывать вопросы охраны окружающей среды и безопасности. Некоторые химические вещества аккумуляторов очень токсичны или вызывают коррозию, что может осложнить утилизацию.
Химикаты на основе никеляБудучи доступными и проверенными, химические вещества на основе никеля имеют множество применений. В этой статье мы сосредоточимся на трех основных химических соединениях никеля: никель-кадмий, никель-металлогидрид и никель-железо. Химия никель-цинк и никель-водород также существуют, хотя они нашли меньшее применение. Никель-водородные батареи особенно широко используются на спутниках из-за их широкого диапазона допустимых температур.
Никель-кадмиевые
Никель-кадмиевые (NiCd) батареи прочные, эластичные и обеспечивают длительный срок службы. Их напряжение также очень стабильно, настолько, что состояние заряда нельзя определить по падению напряжения, как у других аккумуляторов. NiCd элементы можно заряжать очень быстро без ущерба для безопасности. Наконец, никель-кадмиевые аккумуляторы являются одними из самых доступных вторичных аккумуляторов на рынке.
Их напряжение также очень стабильно, настолько, что состояние заряда нельзя определить по падению напряжения, как у других аккумуляторов. NiCd элементы можно заряжать очень быстро без ущерба для безопасности. Наконец, никель-кадмиевые аккумуляторы являются одними из самых доступных вторичных аккумуляторов на рынке.
Однако никель-кадмиевые аккумуляторы имеют некоторые недостатки. Во-первых, хотя они превосходят свинцово-кислотные батареи по плотности энергии, они работают хуже, чем другие современные химические батареи. Во-вторых, они испытывают высокие скорости саморазряда .
В NiCd батареях наблюдается интересное, но неудобное явление: эффект памяти . Эффект памяти заключается в том, что со стороны никель-кадмиевые батареи «вспоминают», насколько глубоко они были разряжены в прошлом, и обеспечивают только такую глубину разряда в будущих циклах. Это вызвано накоплением кристаллов соли, которые блокируют электрод.
Образование кристаллов вызывает эффект памяти. Наросты кристаллов блокируют активную часть анода. Верхнее изображение показывает нормальное образование кристаллов на аноде. На нижнем изображении видны крупные обструктивные кристаллы. Источник: Aero Electric
Наросты кристаллов блокируют активную часть анода. Верхнее изображение показывает нормальное образование кристаллов на аноде. На нижнем изображении видны крупные обструктивные кристаллы. Источник: Aero Electric
Наконец, и это, пожалуй, самое главное, никель-кадмиевые элементы представляют опасность для окружающей среды. Кадмий очень токсичен, а электролитом является гидроксид калия, очень сильное основание. Эти опасности затрудняют правильную утилизацию NiCd элементов. Хотя NiCd-элементы иногда считаются устаревшими, они по-прежнему используются в нишевых приложениях, таких как авиация.
Check out these nickel-cadmium battery specifications:
- Nominal cell voltage : 1.2 V
- Energy density : ~45-80 Wh/kg
- Anode : Nickel hydroxide
- Cathode : Гидроксид кадмия
- Электролит : гидроксид калия
- Самостоятельный разряд : ~ 10%
- Экологические опасности : токсичный, коррозий
 0014
0014 Никель-металлогидридные (NiMH) элементы представляют собой более современную версию NiCd элементов. На первый взгляд, элементы NiMH все еще очень похожи на элементы NiCd — в них по-прежнему используется щелочной электролит, такой как гидроксид калия, а в качестве катода по-прежнему используется гидроксид никеля.
Основное отличие состоит в том, что в ячейках NiMH токсичный кадмий заменен на более эффективные аноды. Точный состав варьируется — отсюда и использование слова «металл», — но все аноды представляют собой сплавы редкоземельных металлов. Такая замена увеличивает стоимость, но делает их более экологичными и обеспечивает большая емкость , уменьшает эффект памяти , снижает чувствительность к температуре .
Check out these nickel-cadmium battery specifications:
- 1.2 V
- ~60-120 Wh/Kg
- 20% in 24 hours, then 10% per month
Nickel-iron
Никель-железные элементы встречаются редко, возможно, из-за их высокой цены, низкой плотности энергии и высокого саморазряда.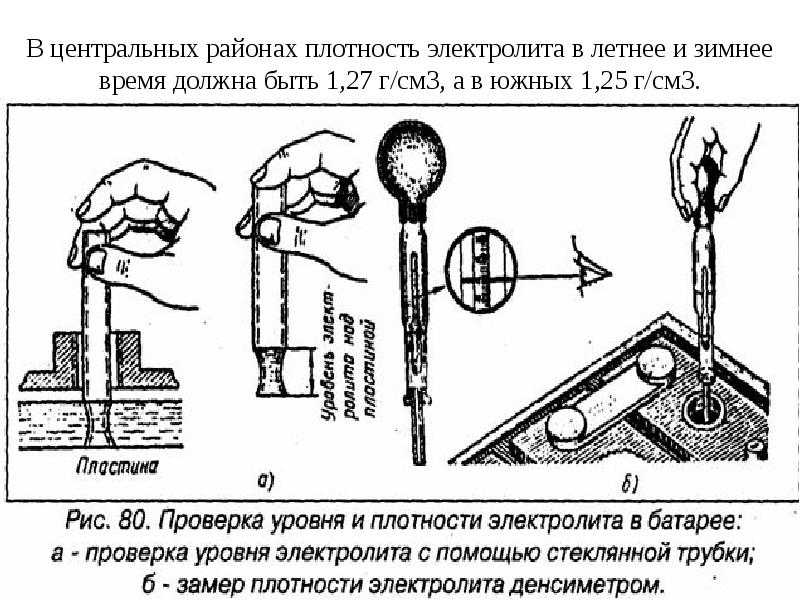 Тем не менее, они эластичны, долговечны и устойчивы к высоким температурам.
Тем не менее, они эластичны, долговечны и устойчивы к высоким температурам.
Check out these nickel-iron battery specifications:
- Nominal cell voltage : ~1.2 V
- Energy density : ~50 Wh/kg
- Anode : Iron
- Cathode : Nickel oxide гидроксид
- Электролит : Гидроксид калия
- Саморазряд : 20-30% в месяц
- Опасность для окружающей среды : Коррозийные
- Nominal cell voltage : ~2 V
- Energy density : 30-50 Wh/kg
- Anode : lead (with others)
- Cathode : lead dioxide
- Electrolyte : sulfuric acid
- Self-discharge : 5% per month
- Environmental hazards : toxic, corrosive
- Номинальное напряжение элемента : 3,6 В
- Плотность энергии : 110-265 Втч/кг
- Анод : углерод, кремний, другие
- Катод : соединения лития
- Электролит : соли лития в органических растворителях0146
- Саморазряд : от 0,35% до 2,5% в месяц
- Опасность для окружающей среды : Горючий органический электролит элементов в систему управления температурным режимом, многие факторы определяют производительность аккумуляторной батареи. Химический состав батареи является фундаментальным выбором при проектировании и выборе батареи.

Свинцово-кислотные батареи дешевые и надежные0004 Свинцово-кислотные аккумуляторы — рабочие лошадки. Эти прочные и надежные батареи обеспечивают питание по низкой цене и имеют низкий уровень саморазряда. Помимо экологических проблем, связанных со свинцовыми и сильнокислотными электролитами, основными недостатками свинцово-кислотных аккумуляторов являются вес и низкая плотность энергии. Это делает их идеальными для ситуаций, когда вес не имеет большого значения, например, автомобили, тележки для гольфа, вилочные погрузчики и источники бесперебойного питания. Химический состав свинцово-кислотных аккумуляторов различается. Свинец составляет большую часть анода в виде сетки. Однако свинец слишком мягок, чтобы выдерживать собственный вес, поэтому для улучшения структурной целостности и электрохимических свойств используются такие металлы, как сурьма, кальций, олово или селен. Check out these lead-acid battery specifications: Сегодня литий-ионные (Li-ion) аккумуляторы являются самой популярной вещью в области хранения энергии. В литий-ионных батареях фактически не используется чистый металлический литий. Как и натрий, литий обладает высокой реакционной способностью, и ранние литий-металлические батареи были склонны к возгоранию и взрыву — знакомая проблема для литиевых батарей. Вместо этого литий-ионные аккумуляторы имеют катоды из ионных соединений лития. Существует несколько химических катодов, включая оксид лития-кобальта (LiCoO2), фосфат лития-железа (LiFePO4), оксид лития-марганца (LiMn2O4) и оксид лития-никель-марганца-кобальта (LiNiMnCoO2). Аноды для литий-ионных аккумуляторов состоят из пористого материала, такого как графит, который связывает ионы лития и высвобождает их в электролит во время разрядки аккумулятора. Силиконовые аноды также являются перспективными анодными материалами. В будущем графен (листы углерода толщиной в один атом) может использоваться в качестве анодов. В качестве электролитов в литий-ионных элементах используются соли лития, растворенные в (воспламеняющихся) органических соединениях. Твердые керамические электролиты могут предложить многообещающую альтернативу. У литий-ионной химии есть два основных недостатка: стоит и хрупкость . Литий может быть дорогостоящим, а добыча лития является интенсивным и вредным для окружающей среды процессом. Однако такие металлы, как кобальт, используемые в литий-ионной химии, повышают цены на аккумуляторы не меньше, а то и больше, чем одноименный литий. Помимо высокой стоимости, литий-ионные аккумуляторы требуют особых условий эксплуатации, поскольку они чувствительны к перезарядке и быстрому разряду. Литий-ионные аккумуляторы заслужили репутацию огневых или взрывоопасных отказов . Благодаря правильному проектированию и тестированию, защите цепи, правильному использованию и предотвращению повреждений этих проблем можно избежать. В этом видео из EE World Online показано, что происходит, когда вы удаляете защитные схемы и игнорируете рекомендации по безопасности для литий-ионных аккумуляторов: Ознакомьтесь со следующими характеристиками литий-ионных аккумуляторов:
Lithium-ion chemistry is at the cutting edge of battery технология 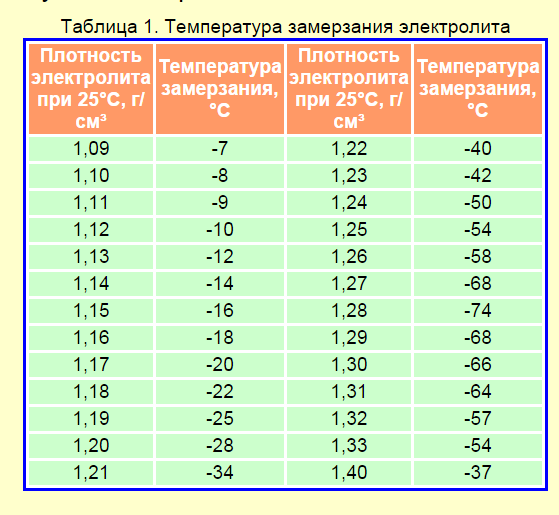 Они обеспечивают высокую плотность энергии и при этом остаются легкими, что делает их востребованными для телефонов, компьютеров, электромобилей и многого другого.
Они обеспечивают высокую плотность энергии и при этом остаются легкими, что делает их востребованными для телефонов, компьютеров, электромобилей и многого другого.
 Но факт остается фактом: литий-ионные аккумуляторы хрупкие.
Но факт остается фактом: литий-ионные аккумуляторы хрупкие.
Состав анода, катода и электролита определяет напряжение батареи, плотность энергии, саморазряд, срок службы и многое другое. Конечно, химический состав батареи сложным образом взаимодействует с другими переменными. Посетите наш блог, чтобы узнать больше о том, как температура влияет на работу батареи.[PD1]
Конструкция аккумуляторной батареи включает в себя множество переменных, одним из которых является химический состав батареи. Наши высококвалифицированные инженеры и техники могут разработать аккумулятор, отвечающий конкретным потребностям вашего предприятия. Свяжитесь с нами по телефону , чтобы обсудить детали проекта, или по телефону , запросите предложение , чтобы начать разработку индивидуального решения для аккумуляторных батарей.
Материал, похожий на зубную пломбу, обеспечивает стабильность литиевой батареи двойной плотности
Энергия
Просмотр 2 изображений
Одним из многих потенциальных путей, которые могут привести нас к накопителям энергии следующего поколения для смартфонов, ноутбуков и электромобилей, является использование твердотельного электролита вместо жидких электролитов, используемых в современных литиевых батареях.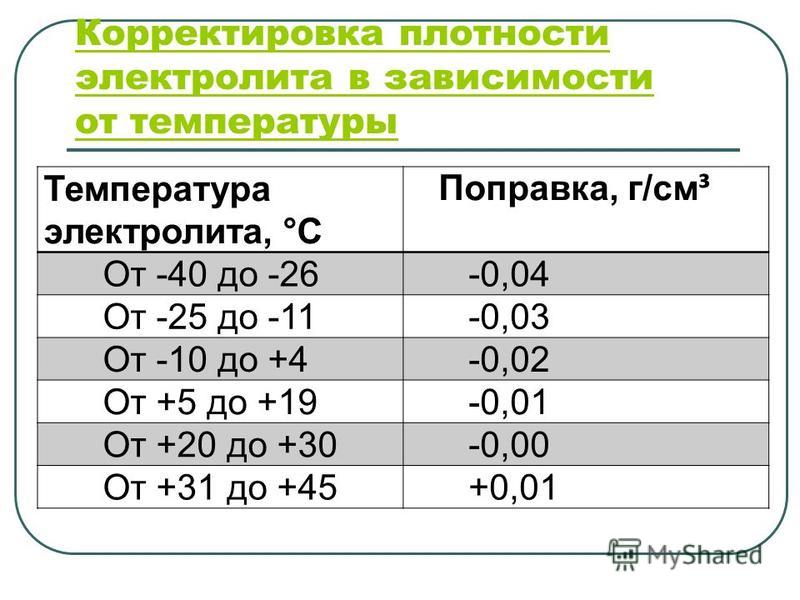 Исследовательская группа в США разработала прототип этих твердотельных батарей, который преодолевает некоторые из ключевых препятствий в этой области, демонстрируя стабильное хранение большой емкости за счет использования нового самовосстанавливающегося материала.
Исследовательская группа в США разработала прототип этих твердотельных батарей, который преодолевает некоторые из ключевых препятствий в этой области, демонстрируя стабильное хранение большой емкости за счет использования нового самовосстанавливающегося материала.
В современных литий-ионных батареях жидкий электролит переносит ионы лития туда и обратно между парой электродов по мере зарядки и разрядки батареи. Если вместо этого электролит может быть изготовлен из твердых материалов, это может сделать батареи более безопасными и обеспечить гораздо большую плотность энергии. Настолько, что было показано, что экспериментальные версии этих элементов способны хранить примерно в два раза больше энергии, чем современные литий-ионные решения.
Проблема в том, что маленькие щупальцеобразные образования, называемые дендритами, имеют тенденцию расти на поверхности одного из электродов по мере разряда батареи. Эти крошечные иголки могут привести к короткому замыканию и выходу из строя батареи или потенциальному возгоранию. Таким образом, разработка твердотельной конструкции, которая позволяет обойти эту проблему, станет большим прорывом.
Таким образом, разработка твердотельной конструкции, которая позволяет обойти эту проблему, станет большим прорывом.
Авторы этого нового исследования из Массачусетского технологического института, Техасского университета A&M, Университета Брауна и Университета Карнеги-Меллона предложили многообещающее решение. Исследователи разработали полутвердый металлический электрод из натрий-калиевых сплавов, который они сравнивают с материалом, который стоматологи используют для пломбирования полостей — прочным, но способным течь и формироваться.
Этот материал обладает достаточной пластичностью, чтобы при контакте с твердым электролитом не образовывались крошечные трещины, которые обычно появляются в полностью твердых, но более хрупких электродных материалах, что обычно приводит к образование дендритов.
«Мотивация заключалась в том, чтобы разработать электроды на основе тщательно отобранных сплавов, чтобы ввести жидкую фазу, которая может служить самовосстанавливающимся компонентом металлического электрода», — говорит Парк.
При циклировании батареи рабочие температуры поддерживают материал в полутвердой фазе, подходящей для выдерживания высоких токов, примерно в 20 раз больших, чем при использовании твердого лития, без образования дендритов. Это устраняет еще один недостаток твердотельных батарей, которые до сих пор не учитывали такую плотность тока, которая позволяла бы перезаряжаться с практической скоростью, по крайней мере, без образования дендритов.
Исследователи, работающие над конструкциями твердотельных аккумуляторов, предложили две конструкции, позволяющие избежать образования дендритов, в одной из которых твердый электролит находится в непосредственном контакте с электродом, а в другой — жидкий металлический сплав, зажатый междуMIT
. В другой конструкции исследователь интегрировал тонкую пленку жидкого натриево-калиевого сплава в батарею, поместив ее между твердым электродом и твердым электролитом. Это также предотвратило образование дендритов, открывая еще один интересный путь для исследований.
Воодушевленные этими многообещающими ранними результатами своих экспериментальных разработок, исследователи в настоящее время изучают способы применения технологии к различным архитектурам твердотельных батарей и с оптимизмом смотрят на возможности.
«Мы думаем, что можем применить этот подход практически к любой твердотельной литий-ионной батарее, — говорит соавтор Венкатасубраманиан Вишванатан, профессор машиностроения Университета Карнеги-Меллона. широкий спектр приложений, от портативных устройств до электромобилей и электроавиации».
Исследование опубликовано в журнале Nature Energy.
Источник: Массачусетский технологический институт
Ник Лаварс
Ник пишет и редактирует в New Atlas уже более шести лет, где он освещал все: от далеких космических зондов до беспилотных автомобилей и странных наук о животных. Ранее он работал в The Conversation, Mashable и The Santiago Times, получив степень магистра в области коммуникаций в Мельбурнском университете RMIT.

 Следует получить как минимум такое количество циклов, которое не приведет к снижению емкости ниже 80% от ее номинальной величины. Соответствующая методика изложена в DIN 43539, часть 3.
Следует получить как минимум такое количество циклов, которое не приведет к снижению емкости ниже 80% от ее номинальной величины. Соответствующая методика изложена в DIN 43539, часть 3.
 удалить крышку батареи. При этом пробки остаются закрытыми.
удалить крышку батареи. При этом пробки остаются закрытыми.

