Сколько электролита должно быть в аккумуляторе?
Как показывает практика далеко не каждый, кто интересуется вопросом, сколько электролита в аккумуляторе, знает, что вообще такое электролит и зачем он нужен, поэтому сейчас вы получите ответы на все озвученные вопросы. Итак, обо всем по порядку.
Что такое электролит и зачем он вообще нужен?
Если вы уже успели прочитать на нашем портале статью: «Какая кислота в аккумуляторе автомобиля», то общее представление об электролите вы уже имеете. Если нет – разъясняем.
Электролит – это раствор серной кислоты и простой дистиллированной воды. Им в нужной концентрации и объеме заполняют свинцово-кислотные аккумуляторные батареи для того, чтобы те благодаря химическим процессам происходящим с этим раствором могли хранить энергию. Отсюда, если концентрация или количество электролита в АКБ уменьшается, она перестает справляться в полной мере со своими обязанности и начинает нуждаться в замене или восстановлении.
Итак, сколько электролита должно быть в АКБ?
То, сколько электролита должна содержать аккумуляторная батарея автомобиля для максимально эффективной своей работы, напрямую определяется ее емкостью. Конечно, в зависимости от производителя возможна некоторая разбежка, но в целом объем электролита для аккумуляторов разной емкости будет следующим:
- 55 А·ч – 2,5 л +/- 100 г;
- 60 А·ч – 2,7-3 л;
- 62 А·ч – около 3 л;
- 65 А·ч – около 3,5 л;
- 75 А·ч – 3,7-4 л;
- 90 А·ч – 4,4-4,8 л;
- 190 А·ч – порядка 10 л.
Но это лишь примерный литраж, он нужен больше для справки перед походом в магазин. В процессе же восстановления аккумулятора нужно ориентироваться не на него, а на особые метки, присутствующие на корпусе последнего. Теперь подробнее.
Какой должен быть уровень электролита в аккумуляторе?
Если в вашем аккумуляторе присутствует шкала с минимумом и максимумом, то вопрос, до какого уровня следует заливать электролит, решается очень просто – по верхнюю черту, то есть до отметки «MAX»,
Если же такой шкалы нет, возможно, в отверстиях вашего аккумулятора есть «язычки», тогда электролита в АКБ нужно заливать столько, чтобы они покрылись 5 мм слоем раствора (полностью в него погрузились).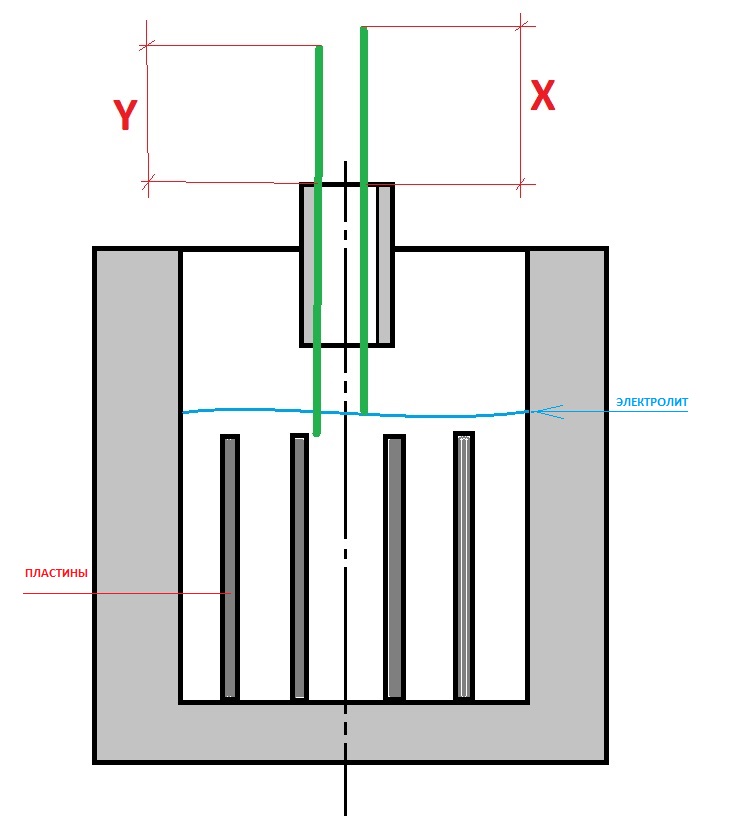
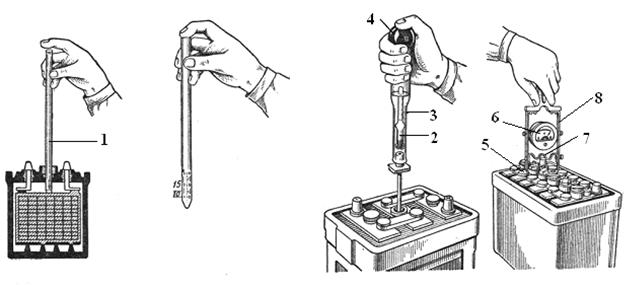
Ну, а если нет ни того, ни другого, залейте в АКБ электролит в рекомендуемом выше объеме (его должно быть не под завязку, а чуть меньше), а затем для самоконтроля возьмите стеклянную трубочку, диаметром до 5 мм и опустите ее внутрь АКБ, пока она не упрется в предохранительный щиток. Закройте верхнее отверстие трубочки пальцем и выньте ее наружу. Если уровень оставшегося в ней электролита находится в пределах 10-15 мм вы все сделали правильно – уровень электролита в АКБ оптимален.
Важно!
Видео.
Рекомендую прочитать:
Часто задаваемые вопросы
Какой минимально допустимый уровень электролита? Что делать если уровень электролита слишком низкий?• Уровень электролита над верхним краем пластин должен быть в пределах от 18 до 45 мм (в зависимости от модели АКБ).
 Минимально допустимый уровень электролита 10мм. Важно помнить, что при понижении уровня электролита в процессе эксплуатации, в батарею следует доливать исключительно дистиллированную воду, а не электролит.
Какова должна быть плотность электролита?
Минимально допустимый уровень электролита 10мм. Важно помнить, что при понижении уровня электролита в процессе эксплуатации, в батарею следует доливать исключительно дистиллированную воду, а не электролит.
Какова должна быть плотность электролита?
• Плотность электролита должна быть в пределах (1,27÷1,30) г/см3 при 25˚С. При плотности электролита ниже 1,26 г/см3 при 25˚С, АКБ необходимо зарядить.
У меня на аккумуляторе маркировка вида 6X71D09UC, что она обозначает? Как определить дату производства АКБ?
• Маркировка вида 6X71D09UC наносится для производственной логистики и не несет информации для владельца аккумулятора. Дата изготовления нанесена на верхнюю часть крышки, состоит из 6 цифр и одной буквы, расшифровывается следующим образом: первые две цифры это месяц, вторая группа цифр это год и третья это день изготовления, буква — шифр смены. Например, маркировка 01 15 02 Т будет читаться как 02 января 2015г. Места нанесения маркировки можно найти у нас на сайте: Маркировка аккумуляторов АКОМ
Места нанесения маркировки можно найти у нас на сайте: Маркировка аккумуляторов АКОМ
У вас на сайте написано, что гарантия на аккумулятор 3 года, а продавец поставил гарантию 1 год? Правильно ли он поступил?
• Гарантийный срок на АКБ производства ЗАО «АКОМ» составляет от 12 до 48 месяцев при пробеге не более 50 000км – 100 000км (в зависимости от модели батареи), данная информация указана как на этикетках самой батареи, так и в инструкции по эксплуатации.
Обращаем Ваше внимание на то, что гарантийный срок всех АКБ производства ЗАО «АКОМ» начинается от даты изготовления. Также обратите внимание на пункт 6.2 инструкции по эксплуатации, где указаны случаи, при которых претензии не удовлетворяются.
В Вашем случае продавец поступил неправильно. В соответствии со ст.5 Закона РФ «О защите прав потребителей» гарантийный срок – период, в течение которого в случае обнаружения в товаре недостатка изготовитель (исполнитель, продавец, уполномоченная организация или уполномоченный индивидуальный предприниматель, импортер) обязаны удовлетворить требования потребителя, установленные статьями 18 и 29 Закона «О защите прав потребителей».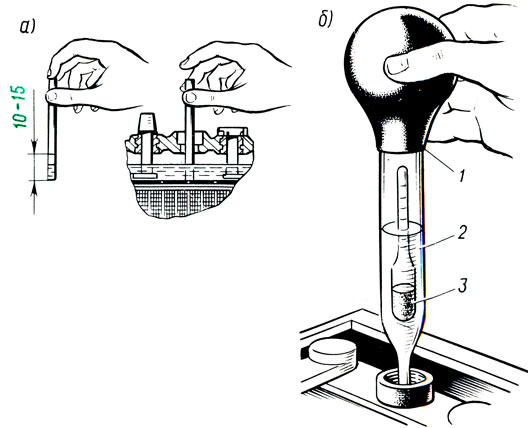
Гарантийные обязательства выполняются в любом регионе РФ, при обращении к официальному представителю. При наличии производственного дефекта в приобретенной Вами батарее, гарантийные обязательства будут исполнены в полном объеме.
У меня вопрос по зарядке аккумулятора
• Инструкция по заряду АКБ находится на нашем сайте: зарядка аккумулятора
Машина всю ночь простояла на морозе, с утра не завелась. Снял аккумулятор и обнаружил, что электролит замерз. Почему это случилось? Что теперь делать с АКБ?
• Если электролит замёрз во всех банках одновременно, батарею необходимо поместить в помещение с температурой 25˚С не менее чем на 24 часа, после чего произвести заряд по инструкции. Данный случай не является гарантийным, т.к. замерзание электролита говорит о понижении его плотности – разряд АКБ не является дефектом завода изготовителя.
• Если электролит замерз в одной из банок АКБ, необходимо также отогреть батарею в течение суток, далее провести контрольный заряд. Если под нагрузкой замерзшая банка начинает кипеть, то вероятнее всего в ней присутствует дефект в виде короткого замыкания. В этом случае батарея подлежит замене по гарантии.
Я купил новый автомобиль, в нем стоит ваш аккумулятор. К кому мне обращаться в случае возникновения проблем с ним?
• В виду того, что аккумуляторная батарея была приобретена в составе автомобиля, все гарантийные обязательства перед Вами несет производитель в лице своего дилера, у которого был приобретен автомобиль.
Инструкции по эксплуатации аккумуляторных батарей
БАТАРЕЯ АККУМУЛЯТОРНАЯ СВИНЦОВАЯ СТАРТЕРНАЯ
ИНСТРУКЦИЯ ПО ЭКСПЛУАТАЦИИ
1. МЕРЫ БЕЗОПАСНОСТИ
МЕРЫ БЕЗОПАСНОСТИ
1.1. Не допускается замыкание полюсов батареи.
1.2. Не допускается эксплуатация батареи с плохими: контактами между выводами батареи и клеммами проводов.
1.3. В помещениях, где ведется заряд батареи, запрещается курить и пользоваться открытым пламенем.
1.4. При работе с электролитом, осмотре заряжающейся батареи глаза должны быть защищены очками.
1.5. После любой работы с батареей и электролитом необходимо вымыть руки с мылом.
1.6. При попадании электролита на кожу или одежду необходимо немедленно промыть это место проточной водой, затем раствором соды.
1.8. Присоединение и отсоединение батареи от бортовой сети автомобиля производить при выключенных потребителях. Сначала присоединить положительный вывод, а затем отрицательный, соединенный с массой автомобиля. Отсоединение производить в обратном порядке.
1.9. Батарея должна быть надежно закреплена в штатном установочном месте автомобиля, соединительные клеммы плотно зажаты на полюсных выводах, а сами провода прослаблены.

2. ПОДГОТОВКА БАТАРЕИ К ЭКСПЛУАТАЦИИ
2.1. Перед началом эксплуатации батареи необходимо полностью удалить с нее упаковочный материал, изучить руководство по эксплуатации.
2.2. Ориентировочная степень заряженности батареи может быть определена по напряжению без нагрузки (см. Таблицу далее) и плотности электролита в батареях с пробками.
3. ЭКСПЛУАТАЦИЯ АККУМУЛЯТОРНОЙ БАТАРЕИ
3.1. Эксплуатация батареи на транспортных средствах допускается только при исправной зарядной системе (при напряжении реле-регулятора в пределах от 13,8В до 14,4В для 12-вольтовых систем электропитания, а для 24-вольтовых систем электропитания- от 26,8В до 28,0В летом и от 28,0В до 29,6В зимой), токе утечки не более 30 мА, плотности электролита согласно Таблице и уровне электролита не ниже 10 мм над пластинами.
3.2. При запуске двигателя длительность работы стартера не должна превышать для карбюраторных автомобилей 10 секунд, для дизельных — 15 секунд. Если попытка запуска не удалась, необходимо сделать перерыв в течение 1 минуты. После этого вновь можно повторить запуск. После пяти неудавшихся запусков рекомендуется проверить систему зажигания и подачу топлива на автомобиле.
— проверяйте и, при необходимости, очищайте батарею от пыли и грязи. Если на поверхности батареи оказался электролит, удаляйте его с помощью ветоши, смоченной в десятипроцентном растворе соды;
— проверяйте и, при необходимости, прочищайте вентиляционные отверстия в пробках;
— проверяйте уровень электролита и, при необходимости, доливайте дистиллированную воду до нормального уровня (при наличии пробок). Доливать электролит в батарею с пробками можно только в тех случаях, когда точно известно, что понижение уровня электролита произошло за счет его выплескивания;
— проверяйте надежность крепления батареи в месте установки и контакты наконечников проводов, установленных на полюсные выводы;
— не реже одного раза в месяц проверяйте степень заряженности батареи.
 При необходимости зарядите батарею в соответствии с п.4.
При необходимости зарядите батарею в соответствии с п.4.3.4. Зимой требования предыдущего пункта следует выполнять обязательно (не реже одного раза в месяц).
3.5. Глубокий разряд батареи недопустим! При отрицательных температурах это приводит к замерзанию электролита и разрушению корпуса батареи.
4. ЗАРЯДКА БАТАРЕИ
4.1. Зарядка аккумуляторной батареи должна производиться в специально оборудованном для этих целей, хорошо вентилируемом нежилом помещении с соблюдением правил противопожарной безопасности.
4.2. Перед началом зарядки аккумуляторной батареи следует вывернуть все пробки (при их наличии).
4.3. Зарядка аккумуляторной батареи должна осуществляться зарядным устройством заводского изготовления в соответствии с инструкцией к этому зарядному устройству и руководством по эксплуатации на батарею.
Таблица: Степень заряженности, напряжение без нагрузки и плотность электролита.
| Напряжение без нагрузки, В | Степень заряженности,% | Плотность электролита при +25°С, г/см |
12. 75-12.60 75-12.60 | 100-80 | 1.27-1.26 |
| 12.55-12.40 | 75-65 | 1.25-1.24 |
| 12.35-12.30 | 50-40 | 1.23-1.21* |
*- эксплуатировать батарею нельзя, требуется зарядить.
4.4. Аккумуляторные батареи без пробок необходимо заряжать автоматическим зарядным устройством, чтобы не допустить интенсивного перезаряда и, как следствие, выкипания электролита.
4.5. Температура электролита в батарее перед зарядкой должна быть в пределах от +15°С до +25°С. Если измерить температуру невозможно по причине отсутствия доступа к электролиту, а батарея находилась при более низкой температуре, то перед зарядкой необходимо выдержать батарею при комнатной температуре не менее 10 часов.
4.6. Не допускается зарядка батареи при температуре электролита выше 50°С.
4.7. Для зарядки положительную клемму батареи присоединить к положительному полюсу зарядного устройства, а отрицательную — к отрицательному.
4.8. При зарядке батарей, имеющих пробки, необходимо откорректировать уровень электролита, добавив дистиллированную воду в случае, если уровень ниже отметки MIN или ниже 10 мм от верхних кромок пластин и сепараторов.
5. ЭЛЕКТРОЛИТ
5.1. Плотность заливаемого в сухозаряженную батарею электролита, приведенная к +25°С, должна быть 1,27-1,28 г/см3.
6. ХРАНЕНИЕ АККУМУЛЯТОРНОЙ БАТАРЕИ
6.1. Батарея устанавливается на хранение полностью заряженной. Рекомендуется ежемесячно проверять напряжение на выводах батареи и, при наличии пробок, плотность электролита. При снижении степени заряженности до 50% (см. Таблицу), батарею необходимо зарядить, эксплуатировать такую батарею нельзя.
6.2. При длительном (сезонном) хранении залитые и заряженные батареи рекомендуется хранить в сухом холодном помещении при температуре до минус 30°С.
7. УТИЛИЗАЦИЯ АККУМУЛЯТОРНОЙ БАТАРЕИ
7.1. Вышедшая из строя батарея подлежит обязательной сдаче в пункт приема отработанных аккумуляторов для последующей надлежащей утилизации.
Берегите окружающую среду! Не выбрасывайте отработанные батареи, сдавайте их в специализированные пункты приема.
Как восстановить гелевый аккумулятор самостоятельно в домашних условиях
Время прочтения: 5 мин
Дата публикации: 12-08-2020
Аккумуляторная батарея – это важный расходник в системах резервного электроснабжения, мотоциклах, скутерах, автомобилях и в прочих видах транспорта. Несмотря на то, что цена аккумулятора не является заоблачной, часто менять батареи никто не хочет. Чтобы АКБ прослужила долго и безотказно, следует придерживаться требований по эксплуатации. Тем не менее, из-за халатного отношения или невнимательности аккумуляторы часто значительно теряют свои первоначальные характеристики или, иными словами, выходят из строя.
Сперва определимся, что такое гелевая аккумуляторная батарея. Гелевым называют свинцово-кислотный аккумулятор с электролитом, свойства которого близки к сухому. Речь идет об АКБ класса GEL. В ней жидкий электролит абсорбирован гелевым наполнителем. Это наделяет батарею массой полезных свойств и преимуществ по сравнению с традиционными АКБ. Из-за схожести реализации и «маркетинговых трюков» гелевыми также называют аккумуляторы класса AGM. И действительно: принцип тот же, только вместо геля свободное пространство заполнено пористым стекловолоконным наполнителем.
Это наделяет батарею массой полезных свойств и преимуществ по сравнению с традиционными АКБ. Из-за схожести реализации и «маркетинговых трюков» гелевыми также называют аккумуляторы класса AGM. И действительно: принцип тот же, только вместо геля свободное пространство заполнено пористым стекловолоконным наполнителем.
Как GEL, так и AGM аккумуляторы являются необслуживаемыми. Речь идет об отсутствии необходимости доливать дистиллированную воду в связи с протеканием процесса рекомбинации. Многие трактуют это иначе и, например, не поддерживают высокий уровень заряда, хотя это необходимо для любой свинцово-кислотной АКБ. Гелевые аккумуляторы часто эксплуатируются в режимах с длительными периодами хранения. В таких условиях можно запросто упустить недопустимо низкий заряд батареи. Поэтому рекомендуется завести мультиметр и периодически проверять напряжение между клеммами. Только оно опустится ниже 10,5-11В – требуется осуществить обслуживание в виде заряда. Если же ситуацию запустить, возможно придется выполнить восстановление гелевого аккумулятора после глубокого разряда.
Что надо знать о сульфатации и десульфатации
В процессе разряда положительные пластины покрываются слоем сульфата свинца. Когда начинается заряд – образовавшийся слой мелкокристаллического сульфата растворяется и аккумулятор возвращается в первоначальное состояние. Условие необратимого образования крупнокристаллического сульфата свинца – это глубокий разряд. Такой налет не снимется полностью в процессе заряда, снижая активность протекающей между электролитом и электродами реакцию. Существуют различные способы очистки пластин:
- Способ №1. Самый простой и безопасный способ частично избавиться от налета в домашних условиях – это использование режима восстановления, который доступен во многих современных зарядных устройствах. Данный режим заключается в чередовании лавинообразных импульсов тока с периодами разряда, что позволяет добиться некоторого восстановления емкости. От крупнокристаллического сульфата, конечно же, такой способ не поможет.
- Способ №2.
 Существуют растворы, позволяющие растворить образовавшийся на пластинах сульфат свинца. Если первый способ можно назвать электрическим, то этот – химическим. Химическая очистка сульфата более эффективна и позволяет добиться очищения более крупного налета сульфата.
Существуют растворы, позволяющие растворить образовавшийся на пластинах сульфат свинца. Если первый способ можно назвать электрическим, то этот – химическим. Химическая очистка сульфата более эффективна и позволяет добиться очищения более крупного налета сульфата. - Способ №3. Никуда не делся старый добрый механический способ удаления сульфата свинца. Это наиболее опасный способ, который ни в коем случае не рекомендуется использовать. Для этого придется необратимо повредить корпус и, возможно, сами пластины.
Осуществлять какие-либо физические и химические манипуляции над электродами с целью их очистки крайне не рекомендуются. Поэтому важно следить за уровнем заряда и не допускать глубокого разряда, способствующего сульфатации. Только так Вы можете обеспечить длительный срок службы аккумуляторной батареи.
Восстановления электролита
И все же, как восстановить гелевый аккумулятор, если манипуляции с электродами совершать не рекомендуется? Единственное, что Вы можете сделать, не навредив – это долить дистиллированной воды, если та все-таки испарилась. В гелевых аккумуляторах испарения возможны лишь при неправильной эксплуатации. Если ток заряда превышает допустимые значения, электролит может закипать, а образовавшиеся испарения – выходить через предохранительные клапаны.
В гелевых аккумуляторах испарения возможны лишь при неправильной эксплуатации. Если ток заряда превышает допустимые значения, электролит может закипать, а образовавшиеся испарения – выходить через предохранительные клапаны.
Если требуется долив воды, необходимо снять крышку и колпачки с банок, после чего заливать дистиллированную воду мелкими порциями. Каждой порции воды следует дать впитаться в наполнитель. Испарение воды – это, повторимся, единственный случай, когда можно довольно безопасно восстановить характеристики гелевого аккумулятора. Во многих остальных случаях батарея не подлежит восстановлению.
Определить, можно ли что-то сделать с аккумулятором, можно визуально. Если аккумулятор потерял емкость, то первое, на что надо обратить внимание – это форма аккумулятора. Если различимо даже малейшее вздутие – эксплуатировать АКБ нельзя. В таком случае только замена. Если же аккумулятор не изменил свою форму, следует убедиться, что с пластинами все в порядке – вполне возможно они попросту начали рассыпаться. Для этого можно потрясти АКБ и постараться расслышать шум от движения трухи, которая отслоилась от электродов. Следующий шаг – это визуальный осмотр через отверстия банок. Снимите колпачки и посветите внутрь, стараясь рассмотреть очертания пластин. Если они рассыпались – пора покупать новый аккумулятор.
Для этого можно потрясти АКБ и постараться расслышать шум от движения трухи, которая отслоилась от электродов. Следующий шаг – это визуальный осмотр через отверстия банок. Снимите колпачки и посветите внутрь, стараясь рассмотреть очертания пластин. Если они рассыпались – пора покупать новый аккумулятор.
Проверяем емкость
Прежде чем делать выводы о состоянии свинцово-кислотной аккумуляторной батареи, надо узнать текущие показатели емкости. А как проверить емкость гелевого аккумулятора, когда вменяемых технических приспособлений для этого попросту нет? Здесь на помощь приходит классический контрольный разряд. Для «эксперимента» потребуется лишь потребитель с известной мощностью (в идеале лампочка) и мультиметр.
Зарядите гелевый аккумулятор до 100% и повесьте на него нагрузку. Следует засечь время, за которое аккумулятор потеряет половину заряда. Сколько осталось заряда, можно определить при помощи мультиметра, измеряя напряжение. Для гелевых аккумуляторов при 50% емкости напряжение будет составлять 12В. Проверять емкость аккумуляторной батареи путем разряда до нуля не рекомендуется по понятным причинам: Вы не только проверите емкость аккумулятора, но и сократите его срок службы глубоким разрядом.
Проверять емкость аккумуляторной батареи путем разряда до нуля не рекомендуется по понятным причинам: Вы не только проверите емкость аккумулятора, но и сократите его срок службы глубоким разрядом.
Таким образом, мы приходим к одному важному выводу: практически любые проблемы, связанные с гелевым аккумулятором, вызваны нарушением требований по эксплуатации. Закипание электролита связано с неправильным зарядом, сульфатация пластин — с глубоким разрядом, а их осыпание – с эксплуатацией под высокой температурой.
Следовательно, единственный способ добиться максимально длительного срока службы – это вовремя заряжать аккумуляторную батарею качественным зарядным устройством, а также эксплуатировать АКБ в прохладном помещении. Банальным бережным обслуживанием батареи Вы добьетесь таких показателей длительности работы и срока службы АКБ, каких не добьетесь ни одним существующим способом восстановления.
Что подливать в современные АКБ: воду или электролит?
Большинство автомобилистов предпочитает покупать именно необслуживаемые аккумуляторы, они хороши тем, что не требуют к себе никакого внимания весь срок своей службы. Но кроме таких АКБ, в продаже доступны и классические – обслуживаемые батареи. За ними требуется регулярный уход, вот только не все водители умеют правильно это делать. Сегодня разберём, что нужно доливать в аккумулятор – электролит или дистиллированную воду.
Но кроме таких АКБ, в продаже доступны и классические – обслуживаемые батареи. За ними требуется регулярный уход, вот только не все водители умеют правильно это делать. Сегодня разберём, что нужно доливать в аккумулятор – электролит или дистиллированную воду.
Куда делся электролит?
В процессе работы аккумулятора из него постепенно испаряется электролит, что приводит к снижению его ёмкости, она начинает быстро разряжаться и не набирает полную зарядку. Стоит отметить, что электролит выкипает из всех типов аккумуляторов, даже из тех, которые не нуждаются в обслуживании. Практически во всех батареях производители предусматривают смотровое окошко, через которое можно контролировать уровень электролита — после испарения достаточного объёма происходит оголение свинцовых пластин. На обслуживаемых АКБ предусмотрены специальные крышки, открутив которые, вы можете посмотреть уровень жидкости и при необходимости долить.
Что долить в аккумулятор?
В большинстве случаев при уменьшении объёма электролита в аккумулятор добавляют дистиллированную воду. На дне батареи остаётся серная кислота, и, чтобы получить электролит, её необходимо разбавить водой. Процедура довольно простоя: покупаете в автомобильном магазине воду и доливаете её до уровня в аккумулятор. Но иногда это не помогает, и в этом случае в батарею нужно заливать уже готовый электролит. Такое бывает в случаях перезаряда АКБ из-за сломавшегося генератора. Это приводит к тому, что электролит начинает активно выкипать, и батарея остаётся буквально сухой. Тогда дистиллированная вода не поможет, и придётся доливать готовый электролит, его можно также купить в автомагазине.
На дне батареи остаётся серная кислота, и, чтобы получить электролит, её необходимо разбавить водой. Процедура довольно простоя: покупаете в автомобильном магазине воду и доливаете её до уровня в аккумулятор. Но иногда это не помогает, и в этом случае в батарею нужно заливать уже готовый электролит. Такое бывает в случаях перезаряда АКБ из-за сломавшегося генератора. Это приводит к тому, что электролит начинает активно выкипать, и батарея остаётся буквально сухой. Тогда дистиллированная вода не поможет, и придётся доливать готовый электролит, его можно также купить в автомагазине.
После заливки дистиллированной воды или электролита обязательно нужно проверить его плотность при помощи ареометра. Нормальной плотностью для электролита считается 1,27 грамм/см3.
Фото: интернет-ресурсы
Особенности эксплуатации щелочных аккумуляторных батарей
Характеристики щелочных аккумуляторов
| Типы аккумуляторов | Номинальная емкость, А-ч | Номинальное напряжение, В |
| НК-28 | 28 | 1,25 |
| НЖ-22 | 22 | 1,25 |
| НК-55 | 55 | 1,25 |
| НЖ-45 | 45 | 1,25 |
| НК-80 | 80 | 1,25 |
| НЖ-60 | 60 | 1,25 |
- «НК» — никель-кадмиевая;
- «НЖ» — никель-железная;
- Цифры после букв — номинальную емкость аккумулятора в ампер-часах.

Характеристики щелочных аккумуляторных батарей
| Типы батарей | Количество аккумуляторов в батарее | Номинальная емкость, А-ч | Номинальное напряжение, В |
| 10НК-28КТ | 10 | 28 | 12,50 |
| 10НЖ-22КТ | 10 | 22 | 12,50 |
| 17НК-28К | 17 | 28 | 21,25 |
| 17НЖ-22К | 17 | 22 | 21,25 |
| 4НК-55КТ, 4НК-55К | 4 | 55 | 5,00 |
| 4НЖ-45КТ, 4НЖ-45К | 4 | 45 | 5,00 |
| 5НК-55К | 5 | 55 | 6,25 |
| 5НЖ-45К | 5 | 45 | 6,25 |
| 10НК-55К | 10 | 55 | 12,50 | 10НЖ-45К | 10 | 45 | 12,50 |
| 4НК-80КТ | 4 | 80 | 5,00 |
| 4НЖ-60КТ | 4 | 60 | 5,00 |
| 5НК-80КТ | 5 | 80 | 6,25 |
| 5НЖ-60КТ | 5 | 60 | 6,25 |
| 10НК-80К | 10 | 80 | 12,50 |
| 10НЖ-60К | 10 | 60 | 12,50 |
Введение в эксплуатацию аккумуляторов и батарей, не бывших в эксплуатации или хранившихся в разряженном состоянии без электролита:
- Перед пуском в эксплуатацию аккумуляторы, как единично работающие, так и комплектуемые в батареи, подвергнуть растренировке с целью получения номинальной емкости;
- С поверхности аккумуляторов и батарей удалите чистой ветошью пыль и соль, проверьте правильность последовательного соединения аккумуляторов в батарее и плотно затяните гайки межэлементных соединений.
 Следы ржавчины на деталях, не покрытых лаком, снимите ветошью, смоченной в керосине;
Следы ржавчины на деталях, не покрытых лаком, снимите ветошью, смоченной в керосине; - Аккумуляторы залейте электролитом, дайте постоять не менее 2 ч (для пропитки пластин) и проверьте вольтметром напряжение на каждом из них. В случае отсутствия напряжения на аккумуляторе оставьте его еще на 10 ч, после чего вновь проверьте напряжение. В случае отсутствия его — аккумулятор замените;
- После 2-часовой пропитки проверьте уровень электролита над пластинами аккумуляторов, который должен быть не менее 5 и не более 12 мм над краем пластин.
Строгое соблюдение уровня электролита (не более 12 мм) требуется для предупреждения выплескивания электролита из аккумулятора во время заряда.
Примечание. Для уменьшения уровня электролита в аккумуляторе пользуйтесь резиновой грушей.
После установления уровня электролита аккумуляторам сообщите три тренировочных цикла токами согласно таблице.
| Типы аккумуляторов | Заряд | Разряд | ||
| Время, ч | Ток, А | Ток, А | Конечное напряжение, В | |
| НЖ-22 | 6 | 5,5 | 2,8 | 1,0 |
| НК-28 | 7,0 | 2,8 | ||
| НЖ-45 | 11,2 | 5,5 | ||
| НК-55 | 14,0 | 5,5 | ||
| НЖ-60 | 15,0 | 8,0 | ||
| НК-80 | 20,0 | 8,0 | ||
Напряжение в конце разряда должно быть не менее одного вольта на худшем аккумуляторе. Если отданная емкость будет не ниже номинальной, аккумуляторы могут быть пущены в эксплуатацию.
Если отданная емкость будет не ниже номинальной, аккумуляторы могут быть пущены в эксплуатацию.
Примечание. Рекомендуется для улучшения качества аккумуляторов перед пуском в эксплуатацию сменить электролит на свежий.
Иногда аккумуляторы после длительного бездействия имеют временное снижение емкости. В этих случаях после контрольного цикла дайте заряд нормальным режимом, а разряд производите в течение восьми часов при постоянной силе тока, не обращая внимания на напряжение аккумуляторов.
В конце разряда нормальную силу тока поддерживайте с помощью внешнего источника тока.
Для этого аккумуляторы подключите к зарядному агрегату так, чтобы положительный полюс аккумулятора был соединен с минусом зарядного устройства,
а отрицательный — с плюсом. После такого глубокого разряда дайте заряд током нормального режима в течение 16 ч и аккумуляторы направьте в эксплуатацию.
Последующие заряды производите в течение 6 ч нормальным током в каждой батарее.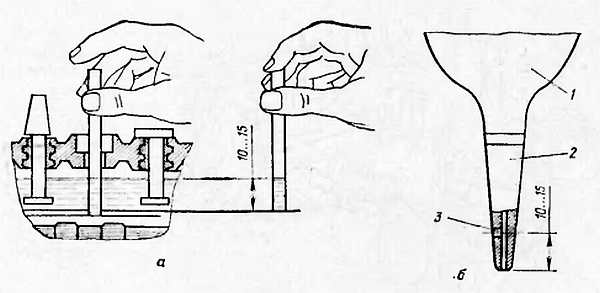
Введение в эксплуатацию аккумуляторов и батарей, хранившихся залитыми электролитом
Аккумуляторы, хранившиеся с электролитом не больше одного года, вводите в эксплуатацию без смены электролита (при условии его соответствия требованиям настоящей инструкции).
При более длительном хранении электролит смените. Введение в эксплуатацию производите как аккумуляторы, не бывшие в эксплуатации.Заряд щелочных аккумуляторов и батарей
Заряд производите от любого источника постоянного тока. Автоматический заряд без постоянного контроля параметров обеспечивают автоматические зарядные устройства серии УЗПС.
Для включения на заряд однотипные аккумуляторы или батареи соедините последовательно.
Количество соединенных аккумуляторов определяется напряжением источника тока и напряжением аккумулятора в конце заряда.
У исправного и правильно включенного аккумулятора напряжение при нормальном зарядном токе должно быть:
- в начале заряда 1,40 В.
 ..1.45 В;
..1.45 В;
- в конце заряда 1,75 В — 1,85 В.
При эксплуатации аккумуляторов и батарей применяйте следующие режимы заряда:
- Нормальный — 6ч нормальным током;
- Усиленный — 12 ч нормальным током, он сообщается:
- при вводе в действие;
- через каждые 10 циклов, а при нерегулярной работе один раз в месяц;
- после смены электролита;
- после глубоких разрядов ниже допустимых конечных напряжений, а также после разрядов слабыми токами, чередующимися с перерывами в течение 16 и более часов.
- Ускоренный — 2,5 ч силой тока вдвое больше нормальной и 2 ч — нормальной силой тока.
Никель — кадмиевые и никель-железные аккумуляторы можно заряжать более слабым током, соответственно увеличивая время заряда,
однако снижать ток более чем на половину не рекомендуется.
ВНИМАНИЕ! Заряды слабыми токами ухудшают работу щелочных аккумуляторов, а поэтому применяйте их в случае крайней необходимости.
Не допускайте повышение температуры электролита при заряде выше 45° С для составных электролитов, и выше 35° С для электролитов без добавки лития едкого.
В случае повышения температуры выше указанной прервите заряд и дайте аккумуляторам остыть.
Заряд аккумуляторов зимой на открытом воздухе при температуре ниже минус 10° С (до минус 30° С) производите нормальной силой тока в течение 7 ч. В случае необходимости заряжать аккумуляторы ниже минус 30° С их утеплите, закрыв войлоком, брезентом или другим материалом.
Примечание. Никель — железные аккумуляторы заряжать при температуре ниже минус 10° С не рекомендуется.
Во время заряда не допускайте выплёскивания электролита. Перед зарядом через каждые 10 циклов проверьте и доведите уровень электролита до норм.Проверьте отсутствие замыкания между стенками соседних аккумуляторов в результате возможного раздутия корпусов. При наличии замыкания напряжение батарей будет значительно ниже номинального.Для обнаружения замкнутых аккумуляторов производите замер зазоров между ними и замер их напряжений. У соприкасающихся аккумуляторов немедленно отверните пробки. Если после устранения замыкания зазор между аккумуляторами меньше 3 мм, изолируйте их листом тонкого эбонита, винипласта или резины.После устранения замыкания аккумуляторов сообщите им усиленный заряд.
При наличии замыкания напряжение батарей будет значительно ниже номинального.Для обнаружения замкнутых аккумуляторов производите замер зазоров между ними и замер их напряжений. У соприкасающихся аккумуляторов немедленно отверните пробки. Если после устранения замыкания зазор между аккумуляторами меньше 3 мм, изолируйте их листом тонкого эбонита, винипласта или резины.После устранения замыкания аккумуляторов сообщите им усиленный заряд.
Разряд щелочных аккумуляторов и батарей
Разряд щелочных аккумуляторов можно производить до конечного напряжения:- при 5-часовом и более длительном режиме разряда не ниже 1,0 В;
- при 3-часовом режиме разряда не ниже 0,8 В;
- при 1-часовом режиме разряда не ниже 0,5 В;
Конечное напряжение разряда аккумуляторных батарей определяйте как произведение числа аккумуляторов в батарее на конечное напряжение отдельного аккумулятора, соответственно режиму разряда.Автоматический разряд с заданными параметрами разряда обеспечивают устройства тестирования аккумуляторных батарей.
При эксплуатации аккумуляторов и батарей через каждые 100 — 150 циклов производите контрольные электрические испытания.Аккумуляторам или батареям сообщите два прогоночных цикла. Заряд производите током нормального режима в течение 12ч, разряд нормальным режимом до конечного напряжения 1,0 В у одного из аккумуляторов.
Контрольный цикл проводите в нормальным режимом.
На контрольном цикле производите замеры напряжения каждого аккумулятора:- при заряде — в начале и конце заряда;
- при разряде — в начале разряда, через 6 ч, 7 ч и через 8 ч разряда.
Аккумуляторы, имеющие через 6 ч разряда напряжение 1.0В и ниже, замените.
Примечание. Контрольные испытания производите после смены электролита.Никель-железные аккумуляторы могут эксплуатироваться при температуре не ниже минус 20° С, при этом они отдают не менее 70% номинальной емкости.
Никель-кадмиевые аккумуляторы — не ниже минус 40° С, при этом они отдают 20% номинальной емкости.
Факторы, сокращающие срок службы аккумуляторов и батарей
- систематические недозаряды;
- глубокие разряды ниже конечных напряжений;
- снижение уровня электролита ниже верхнего края пластин;
- повышенная плотность электролита при температуре выше 0° С;
- повышение температуры.
С рекомендациями по выбору зарядного устройства можно ознакомиться здесь.
Купить щелочные аккумуляторные батареи
По вопросу приобретения щелочных аккумуляторных батарей рекомендуем обращаться по адресу:
Общество с ограниченной ответственностью «АИТ-СПб»
Адрес: 197374, г. Санкт-Петербург, ул. Оптиков, 4
Телефон: 8 (812) 324-18-02; 8 (921) 847-12-11
Факс: 8 (812) 324-18-01
http://www.valgen.ru
Обслуживание аккумулятора на скутере — Статьи о скутерах и мопедах
Свинцово-кислотные аккумуляторы для мототехники существуют 2-х типов:
- обслуживаемые;
- необслуживаемые.

АКБ продаются в заряженном и сухозаряженном состоянии. Еще появились гелевые виды, которым обслуживание аккумулятора не требуется.
Реклама: аккумулятор в рассрочку
Подготовка необслуживаемого аккумулятора к первому пускуПервое что нужно сделать, необходимо заправить электролитом сухозаряженный аккумулятор. Летом достаточно довести плотность электролита до 1,25г/см куб, а зимой довести плотность до 1,28 г/см куб.
Далее нужно открутить пробки банок аккумулятора и очень аккуратно залить в них электролит (лучше это делать в перчатках и рабочей одежде), залить нужно так, чтобы электролит покрывал свинцовые пластины на 1-1,5см, но не под самое горлышко.
Вот и закончена не сложная процедура заправки аккумулятора и уже через два часа можно пользоваться. Обратите внимание, аккумулятор сначала будет заряжен только на 60-70%, но этого достаточно чтобы завести скутер.
Обслуживание аккумуляторов- За сухозаряженным и уже заправленным электролитом аккумулятором требуются одинаковый уход в процессе эксплуатации.
 Важно чтобы аккумулятор содержался в чистоте. Эстетически это конечно приятно, но главная причина не в этом, дело в том, что пыль и грязь которые собираются между клеммами, постепенно пропитывается парами электролита и становится проводником электричества. И даже если по счастливому случаю это не приведет к короткому замыканию, то привести к преждевременному разряду точно сможет, а что снижает срок службы аккумулятора скутера.
Важно чтобы аккумулятор содержался в чистоте. Эстетически это конечно приятно, но главная причина не в этом, дело в том, что пыль и грязь которые собираются между клеммами, постепенно пропитывается парами электролита и становится проводником электричества. И даже если по счастливому случаю это не приведет к короткому замыканию, то привести к преждевременному разряду точно сможет, а что снижает срок службы аккумулятора скутера. - Не забывайте проверять уровень электролита. Если у корпуса аккумулятор непрозрачный, то уровень электролита проверяется щупом.
- Так как идет реакция электролиза, то вода понемногу испаряется, нужно проверять количество воды и с случае необходимости доливать в банки аккумулятора, ориентируясь на метки или показания щупа.
- Если по какой-то причине аккумулятор опрокинулся с открытыми пробками, то тогда нужно повторить процедуру описанную выше для.
Когда скутер исправен (запчасти для скутера), аккумулятор отлично держит заряд, то не требуется дополнительной зарядки.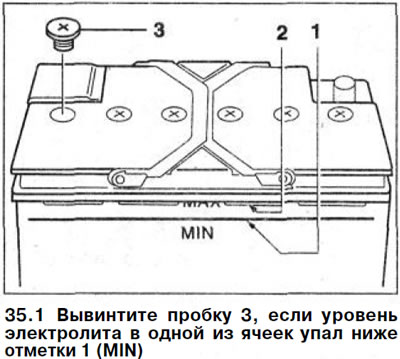 Но к началу зимнего периода обычно владельцы скутеров уже отгоняют их в гараж. Никогда не оставляйте подключенный аккумулятор к скутеру на длительный период и особенно на неотапливаемую зимовку. В последствии зарядить его уже навряд ли удастся.
Но к началу зимнего периода обычно владельцы скутеров уже отгоняют их в гараж. Никогда не оставляйте подключенный аккумулятор к скутеру на длительный период и особенно на неотапливаемую зимовку. В последствии зарядить его уже навряд ли удастся.
Для всех свинцово-кислотных аккумуляторов существует правило: ток заряда не должен превышать 1/10 его емкости.
Периодически нужно проверять состояние заряда вашего аккумулятора. Заряд можно определить с помощью специального индикатора на нем, а если индикатора нет, то обычным вольтметром. Через 20-30 мин. после эксплуатации скутера, напряжение на клеммах рабочего аккумулятора составляет около 12,8 вольт, а если 12,3 вольта или даже ниже, то аккумулятор либо не заряжается и есть проблема в электрооборудовании скутера, либо аккумулятор изношен и требует замены.
Если на вашем скутере гелевый аккумулятор, то самое главное в уходе такого аккумулятора – содержать его в чистоте. Следует помнить, что даже короткое кратковременное замыкание, выведет гелевый аккумулятор из строя раз и навсегда.
Как активировать обычную батарею
Как обычные батареи покидают завод
Обычные батареи Yuasa покидают завод в виде бутылки, поставляемой (BS):
- Бутылка в комплекте (BS) — сухая Обычные батареи поставляются с сохраненным электролитом в пластиковом контейнере. Аккумулятор заполняется электролитом из контейнера, когда он готов к активации. Обычные батареи имеют срок годности 2 года, указанный производителем, при условии, что они остаются закрытыми.Надлежащая герметизация обычных батарей означает, что крышки заливных горловин и красные вентиляционные крышки устанавливаются и хранятся при комнатной температуре. После того, как аккумулятор распечатан, его следует активировать, зарядить и установить. Пластины ячеек незапечатанной незаряженной батареи начнут окисляться, что затруднит дальнейшую зарядку.
Процесс активации обычной батареи
- Батарея должна быть вне автомобиля и размещена на ровной поверхности.
 Снимите крышки заливного отверстия (красные, желтые или зеленые крышки батарейного отсека).
Снимите крышки заливного отверстия (красные, желтые или зеленые крышки батарейного отсека). - Снимите красную заглушку с вентиляционного колена . Если на вентиляционном патрубке аккумулятора есть красный колпачок, снимите его и выбросьте. Никогда не надевайте этот колпачок обратно на аккумулятор после того, как он наполнен кислотой, так как повышение внутреннего давления газа может привести к разрыву корпуса аккумулятора.
- Используя бутылку с кислотой, поставляемую с аккумулятором, поместите емкость вертикально на плоскую поверхность. Осторожно отрежьте кончик носика бутылки и прикрепите прилагаемую короткую трубку. Осторожно: Не сжимайте бутылку при разрезании наконечника наполнения . Не курите при включении аккумулятора или работе с аккумуляторной кислотой. Всегда надевайте пластиковые перчатки и защитные очки.
- Залейте в аккумулятор электролит, поставляемый с аккумулятором.
 Не используйте воду или другие жидкости для активации батареи. Температура электролита перед заливкой должна быть от 60 до 86 градусов по Фаренгейту. Если электролит хранится в холодном помещении, перед заливкой его следует нагреть до комнатной температуры.Залейте до ВЕРХНЕГО УРОВНЯ, как указано на батарее. Примечание. Никогда не заправляйте и не активируйте аккумулятор, установленный в автомобиле, так как пролив электролита может вызвать повреждение. .
Не используйте воду или другие жидкости для активации батареи. Температура электролита перед заливкой должна быть от 60 до 86 градусов по Фаренгейту. Если электролит хранится в холодном помещении, перед заливкой его следует нагреть до комнатной температуры.Залейте до ВЕРХНЕГО УРОВНЯ, как указано на батарее. Примечание. Никогда не заправляйте и не активируйте аккумулятор, установленный в автомобиле, так как пролив электролита может вызвать повреждение. . - Медленно и осторожно заполняйте каждую ячейку батареи до линии наивысшего уровня.
- После заполнения дайте аккумулятору постоять не менее 30 минут. Переместите батарею или осторожно постучите по ней, чтобы удалить пузырьки воздуха между пластинами. Если уровень кислоты упал, долейте кислоту до верхнего уровня.
- Заправка обычной батареи электролитом доведет ее до 75-80% заряда. Аккумулятор необходимо зарядить до 100% перед вводом в эксплуатацию . Чтобы найти рекомендуемые требования к току зарядки в амперах для конкретной батареи, разделите номинальную емкость батареи в ампер-часах на 10.
 Например, батарею емкостью 14 Ач следует заряжать с током 1,4 ампера (14 Ач ÷ 10 = 1,4 ампера). Удельный вес электролита должен вырасти как минимум до 1,260 на батареях серии 12N. На всех высокопроизводительных батареях (серия YB) должно соблюдаться минимальное показание 1,280.
Например, батарею емкостью 14 Ач следует заряжать с током 1,4 ампера (14 Ач ÷ 10 = 1,4 ампера). Удельный вес электролита должен вырасти как минимум до 1,260 на батареях серии 12N. На всех высокопроизводительных батареях (серия YB) должно соблюдаться минимальное показание 1,280. - Во время начальной зарядки проверьте, не упал ли уровень электролита, и если да, залейте кислоту до ВЕРХНЕГО УРОВНЯ. После добавления кислоты заряжайте еще час с той же скоростью, что и выше, чтобы смешать воду и кислоту. Примечание. Это последний раз, когда нужно добавлять электролит в аккумулятор. Если во время использования уровень низкий, следует добавить дистиллированную воду по мере необходимости. .
- По окончании зарядки установите на место пробки крышки заливной горловины и затяните их вручную — не используйте отвертку или плоскогубцы .Смойте пролитую кислоту водой с раствором пищевой соды, обращая особое внимание на то, чтобы кислота смывалась с клемм.
 Высушите аккумуляторный отсек и установите аккумулятор.
Высушите аккумуляторный отсек и установите аккумулятор.
Активация обычной батареи — это простой процесс, который может успешно выполнить почти любой гонщик или механик. Не забывайте всегда проявлять осторожность при обращении с батареями и активационным оборудованием.
DOE объясняет … Батареи | Министерство энергетики
Батареи и аналогичные устройства принимают, хранят и отпускают электроэнергию по запросу.В батареях используется химия в форме химического потенциала для хранения энергии, как и во многих других повседневных источниках энергии. Например, бревна хранят энергию в своих химических связях, пока при горении энергия не преобразуется в тепло. Бензин — это запасенная химическая потенциальная энергия, пока она не преобразуется в механическую энергию в двигателе автомобиля. Точно так же, чтобы батареи работали, электричество должно быть преобразовано в форму химического потенциала, прежде чем оно может быть легко сохранено. Батареи состоят из двух электрических клемм, называемых катодом и анодом, разделенных химическим материалом, называемым электролитом. Чтобы принимать и высвобождать энергию, батарея подключается к внешней цепи. Электроны движутся по цепи, в то время как ионы (атомы или молекулы с электрическим зарядом) одновременно движутся через электролит. В перезаряжаемой батарее электроны и ионы могут двигаться в любом направлении через цепь и электролит. Когда электроны движутся от катода к аноду, они увеличивают химическую потенциальную энергию, заряжая таким образом аккумулятор; когда они движутся в другом направлении, они преобразуют эту химическую потенциальную энергию в электрическую цепь и разряжают батарею.Во время зарядки или разрядки противоположно заряженные ионы перемещаются внутри батареи через электролит, чтобы уравновесить заряд электронов, проходящих через внешнюю цепь, и создать устойчивую перезаряжаемую систему. После зарядки аккумулятор может быть отключен от цепи для хранения химической потенциальной энергии для последующего использования в качестве электричества.
Чтобы принимать и высвобождать энергию, батарея подключается к внешней цепи. Электроны движутся по цепи, в то время как ионы (атомы или молекулы с электрическим зарядом) одновременно движутся через электролит. В перезаряжаемой батарее электроны и ионы могут двигаться в любом направлении через цепь и электролит. Когда электроны движутся от катода к аноду, они увеличивают химическую потенциальную энергию, заряжая таким образом аккумулятор; когда они движутся в другом направлении, они преобразуют эту химическую потенциальную энергию в электрическую цепь и разряжают батарею.Во время зарядки или разрядки противоположно заряженные ионы перемещаются внутри батареи через электролит, чтобы уравновесить заряд электронов, проходящих через внешнюю цепь, и создать устойчивую перезаряжаемую систему. После зарядки аккумулятор может быть отключен от цепи для хранения химической потенциальной энергии для последующего использования в качестве электричества.
Батареи были изобретены в 1800 году, но их химические процессы сложны. Ученые используют новые инструменты, чтобы лучше понять электрические и химические процессы в батареях, чтобы создать новое поколение высокоэффективных аккумуляторов электроэнергии.Например, они разрабатывают улучшенные материалы для анодов, катодов и электролитов в батареях. Ученые изучают процессы в аккумуляторных батареях, потому что они не полностью меняются, когда батарея заряжается и разряжается. Со временем отсутствие полной замены может изменить химический состав и структуру материалов батареи, что может снизить производительность и безопасность батареи.
Ученые используют новые инструменты, чтобы лучше понять электрические и химические процессы в батареях, чтобы создать новое поколение высокоэффективных аккумуляторов электроэнергии.Например, они разрабатывают улучшенные материалы для анодов, катодов и электролитов в батареях. Ученые изучают процессы в аккумуляторных батареях, потому что они не полностью меняются, когда батарея заряжается и разряжается. Со временем отсутствие полной замены может изменить химический состав и структуру материалов батареи, что может снизить производительность и безопасность батареи.
Департамент науки и хранения электроэнергии Министерства энергетики
Исследования, проведенные при поддержке Департамента науки Министерства энергетики, Управления фундаментальных энергетических наук (BES), привели к значительным улучшениям в хранении электроэнергии.Но мы все еще далеки от комплексных решений для хранения энергии следующего поколения с использованием совершенно новых материалов, которые могут значительно увеличить количество энергии, которое может хранить батарея. Это хранилище имеет решающее значение для интеграции возобновляемых источников энергии в нашу систему электроснабжения. Поскольку усовершенствование аккумуляторных технологий имеет важное значение для повсеместного использования подключаемых к электросети электромобилей, хранение также является ключом к уменьшению нашей зависимости от нефти при транспортировке.
Это хранилище имеет решающее значение для интеграции возобновляемых источников энергии в нашу систему электроснабжения. Поскольку усовершенствование аккумуляторных технологий имеет важное значение для повсеместного использования подключаемых к электросети электромобилей, хранение также является ключом к уменьшению нашей зависимости от нефти при транспортировке.
BES поддерживает исследования отдельных ученых и в многопрофильных центрах.Самый крупный центр — Объединенный центр исследований в области накопления энергии (JCESR), центр энергетических инноваций Министерства энергетики США. Этот центр изучает электрохимические материалы и явления на атомном и молекулярном уровне и использует компьютеры для разработки новых материалов. Эти новые знания позволят ученым разработать более безопасные накопители энергии, которые служат дольше, заряжаются быстрее и обладают большей емкостью. По мере того как ученые, поддерживаемые программой BES, достигают новых успехов в науке об аккумуляторах, эти достижения используются прикладными исследователями и промышленностью для продвижения приложений в области транспорта, электросетей, связи и безопасности.
Факты о накоплении электроэнергии
- Нобелевская премия по химии 2019 года была присуждена совместно Джону Б. Гуденафу, М. Стэнли Уиттингему и Акире Йошино «за разработку литий-ионных батарей».
- Компания Electrolyte Genome в JCESR создала вычислительную базу данных, содержащую более 26 000 молекул, которую можно использовать для расчета основных свойств электролита для новых, усовершенствованных аккумуляторов.
Ресурсы и связанные с ними термины
Научные термины могут сбивать с толку.DOE Explains предлагает простые объяснения ключевых слов и концепций фундаментальной науки. В нем также описывается, как эти концепции применяются к работе, которую проводит Управление науки Министерства энергетики США, поскольку это помогает Соединенным Штатам преуспевать в исследованиях в научном спектре.
Новый аккумуляторный электролит может расширить ассортимент электромобилей
Марк Шварц
Новый электролит на основе лития, изобретенный учеными Стэнфордского университета, может проложить путь для следующего поколения электромобилей с батарейным питанием.
В исследовании, опубликованном 22 июня в журнале Nature Energy , исследователи из Стэнфорда демонстрируют, как их новая конструкция электролита повышает производительность литий-металлических батарей — многообещающей технологии для питания электромобилей, ноутбуков и других устройств.
Обычный (прозрачный) электролит слева и новый электролит Стэнфордского стандарта
справа. (Изображение предоставлено: Чжиао Юй)
«Большинство электромобилей работают на литий-ионных батареях, которые быстро приближаются к своему теоретическому пределу по плотности энергии», — сказал соавтор исследования И Цуй, профессор материаловедения, инженерии и фотоники из Национальной ускорительной лаборатории SLAC.«Наше исследование было сосредоточено на литий-металлических батареях, которые легче, чем литий-ионные, и потенциально могут обеспечивать больше энергии на единицу веса и объема».
Литий-ионный против металлического лития
Литий-ионные батареи, используемые во всем, от смартфонов до электромобилей, имеют два электрода — положительно заряженный катод, содержащий литий, и отрицательно заряженный анод, обычно сделанный из графита.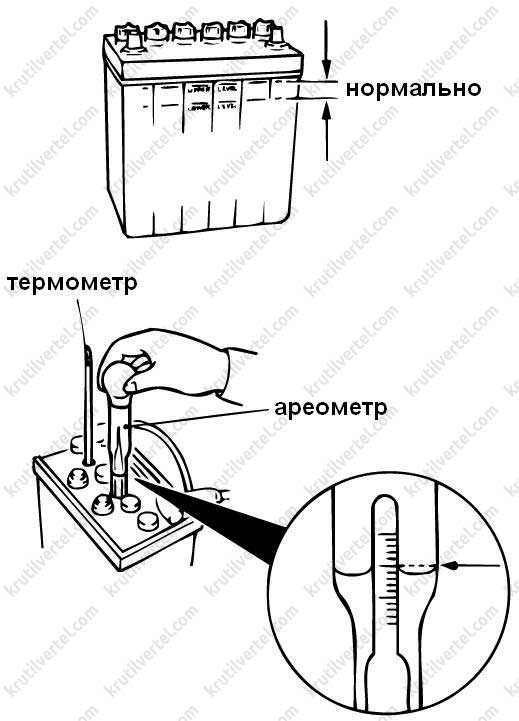 Раствор электролита позволяет ионам лития перемещаться между анодом и катодом, когда батарея используется и когда она заряжается.
Раствор электролита позволяет ионам лития перемещаться между анодом и катодом, когда батарея используется и когда она заряжается.
Литий-металлический аккумулятор может содержать примерно в два раза больше электроэнергии на килограмм, чем современные литий-ионные аккумуляторы. Литий-металлические батареи делают это путем замены графитового анода металлическим литием, который может хранить значительно больше энергии.
«Литий-металлические батареи очень перспективны для электромобилей, где вес и объем имеют большое значение», — сказал соавтор исследования Женан Бао, K.K. Ли Профессор инженерной школы. «Но во время работы анод из металлического лития вступает в реакцию с жидким электролитом.Это вызывает рост микроструктур лития, называемых дендритами, на поверхности анода, что может привести к возгоранию батареи и ее выходу из строя ».
Исследователи потратили десятилетия, пытаясь решить проблему дендритов.
«Электролит был ахиллесовой пятой литий-металлических батарей», — сказал соавтор исследования Чжао Юй, аспирант по химии. «В нашем исследовании мы используем органическую химию для рационального проектирования и создания новых стабильных электролитов для этих батарей.”
«В нашем исследовании мы используем органическую химию для рационального проектирования и создания новых стабильных электролитов для этих батарей.”
Электролит новый
Для исследования Ю и его коллеги выяснили, могут ли они решить проблемы стабильности с помощью обычного, коммерчески доступного жидкого электролита.
«Мы предположили, что добавление атомов фтора к молекуле электролита сделает жидкость более стабильной», — сказал Ю. «Фтор — широко используемый элемент в электролитах литиевых батарей. Мы использовали его способность притягивать электроны, чтобы создать новую молекулу, которая позволяет аноду из металлического лития хорошо работать в электролите.”
В результате получилось новое синтетическое соединение, сокращенно FDMB, которое можно легко производить в больших объемах.
«Конструкции электролитов становятся очень экзотичными, — сказал Бао. «Некоторые из них оказались многообещающими, но их производство очень дорогое. Молекула FDMB, которую придумал Чжиао, легко производить в больших количествах и довольно дешево ».
«Невероятная производительность»
Команда Стэнфорда провела испытания нового электролита в литий-металлической батарее.
Результаты были впечатляющими.Экспериментальная батарея сохранила 90 процентов своего первоначального заряда после 420 циклов зарядки и разрядки. В лабораториях типичные литий-металлические батареи перестают работать примерно через 30 циклов.
Докторанты и ведущие авторы Хансен Ван (слева) и Чжиао Ю (справа) тестируют
экспериментальную ячейку в своей лаборатории. (Изображение предоставлено Hongxia Wang.)
Исследователи также измерили, насколько эффективно ионы лития переносятся между анодом и катодом во время зарядки и разрядки, это свойство известно как «кулоновская эффективность».”
«Если вы зарядите 1000 ионов лития, сколько вы получите обратно после разрядки?» — сказал Цуй. «В идеале вы хотите 1000 из 1000 для 100-процентного кулоновского КПД. Чтобы быть коммерчески жизнеспособным, элемент батареи должен иметь кулоновскую эффективность не менее 99,9%. В нашем исследовании мы получили 99,52 процента в половинных ячейках и 99,98 процентов в полных ячейках; невероятная производительность ».
В нашем исследовании мы получили 99,52 процента в половинных ячейках и 99,98 процентов в полных ячейках; невероятная производительность ».
Батарея безанодная
Для потенциального использования в бытовой электронике команда Стэнфордского университета также провела испытания электролита FDMB в безанодных литий-металлических ячейках — коммерчески доступных батареях с катодами, которые поставляют литий на анод.
«Идея состоит в том, чтобы использовать литий только на катодной стороне, чтобы уменьшить вес», — сказал соавтор исследования Хансен Ван, аспирант в области материаловедения и инженерии. «Безанодная батарея проработала 100 циклов, прежде чем ее емкость упала до 80 процентов — не так хорошо, как эквивалентная литий-ионная батарея, которая может выдерживать от 500 до 1000 циклов, но все же одна из самых эффективных безанодных ячеек».
«Эти результаты показывают многообещающие результаты для широкого диапазона устройств», — добавил Бао. «Легкие безанодные батареи станут привлекательным элементом для дронов и многих других видов бытовой электроники. ”
”
Аккумулятор 500
Министерство энергетики США (DOE) финансирует большой исследовательский консорциум под названием Battery500, чтобы сделать литий-металлические батареи жизнеспособными, что позволит производителям автомобилей создавать более легкие электромобили, которые могут преодолевать гораздо большие расстояния между зарядками. Это исследование было частично поддержано грантом консорциума, в который входят Стэнфорд и SLAC.
За счет улучшения анодов, электролитов и других компонентов Battery500 стремится почти в три раза увеличить количество электроэнергии, которое может выдать литий-металлический аккумулятор, с примерно 180 ватт-часов на килограмм, когда программа стартовала в 2016 году, до 500 ватт-часов на килограмм.Более высокое отношение энергии к весу, или «удельная энергия», является ключом к решению проблемы запаса хода, которую часто испытывают потенциальные покупатели электромобилей.
«Безанодная батарея в нашей лаборатории обеспечивает мощность около 325 ватт-часов на килограмм удельной энергии, приличное число», — сказал Цуй. «Нашим следующим шагом могла бы стать совместная работа с другими исследователями Battery500 над созданием ячеек, которые приблизятся к цели консорциума — 500 ватт-часов на килограмм».
Испытание на воспламеняемость обычного карбонатного электролита (слева) и нового электролита FDMB (справа) разработано
в Стэнфорде.Обычный карбонатный электролит воспламеняется сразу после прикосновения к пламени, но электролит
FDMB может выдерживать прямое пламя в течение как минимум трех секунд. (Кредит Чжиао Ю)
Помимо более длительного срока службы и лучшей стабильности, электролит FDMB также гораздо менее воспламеняем, чем обычные электролиты, как исследователи продемонстрировали во встроенном видео.
«Наше исследование в основном обеспечивает принцип конструкции, который люди могут применять для создания более качественных электролитов», — добавил Бао.«Мы только что показали один пример, но есть много других возможностей».
Другие соавторы Стэнфордского университета: Цзянь Цинь , доцент кафедры химического машиностроения; докторанты Сянь Конг, Кеченг Ван, Вэньсяо Хуанг, Снехашис Чоудхури и Чибуезе Аманчукву; аспиранты Уильям Хуанг, Ючи Цао, Дэвид Маканич, Ю Чжэн и Саманта Хунг; и студенты Ютинг Ма и Эдер Ломели. Синьчан Ван из Университета Сямэнь также является соавтором.Чжэнань Бао и И Цуй — старшие научные сотрудники Стэнфордского энергетического института Precourt Institute for Energy . Цуй также является ведущим исследователем в Стэнфордского института материаловедения и энергетики , совместной исследовательской программе SLAC / Стэнфорд.
Эта работа также была поддержана программой исследования материалов для аккумуляторов Департамента автомобильных технологий Министерства энергетики США. Двое из соавторов поддерживаются Программой стипендий для аспирантов Национального научного фонда и стипендией Центра TomKat в области устойчивой энергетики в Стэнфорде.Средство, используемое в Стэнфорде, поддерживается Национальным научным фондом.
Как работает аккумулятор — Любопытно
Представьте себе мир без батарей. Все портативные устройства, от которых мы так зависим, были бы настолько ограничены! Мы сможем доставить наши ноутбуки и телефоны так, чтобы их кабели были доступны только для того, чтобы сделать это новое работающее приложение, которое вы только что загрузили на свой телефон, практически бесполезным.
К счастью, у нас есть батарейки. Еще в 150 г. до н.э. в Месопотамии парфянская культура использовала устройство, известное как багдадская батарея, сделанное из медных и железных электродов с уксусом или лимонной кислотой.Археологи считают, что на самом деле это не батареи, а в основном они использовались для религиозных церемоний.
Изобретение батареи в том виде, в котором мы ее знаем, приписывают итальянскому ученому Алессандро Вольта, который собрал первую батарею, чтобы доказать свою точку зрения другому итальянскому ученому Луиджи Гальвани. В 1780 году Гальвани показал, что лапки лягушек, подвешенных на железных или латунных крючках, подергиваются при прикосновении к зонду из другого металла. Он считал, что это было вызвано электричеством из тканей лягушек, и называл это «животным электричеством».
Луиджи Гальвани обнаружил, что лапы лягушек, подвешенных на латунных крючках, дергались, когда их ткнули зондом из другого металла. Он думал, что эта реакция была вызвана «животным электричеством» внутри лягушки. Источник изображения: Луиджи Гальвани / Wikimedia Commons.Вольта, первоначально впечатленный открытиями Гальвани, пришел к выводу, что электрический ток исходит от двух разных типов металла (крючки, на которых висели лягушки, и другой металл зонда) и просто передается через них, а не через них. из тканей лягушек.Он экспериментировал со стопками слоев серебра и цинка, перемежаемых слоями ткани или бумаги, пропитанной соленой водой, и обнаружил, что электрический ток действительно течет через провод, приложенный к обоим концам стопки.
Батарея Алессандро Вольта: куча цинковых и серебряных листов, перемежаемых тканью или бумагой, пропитанной соленой водой. Представьте, что вы используете это для питания вашего телефона. Источник изображения: Луиджи Кьеза / Wikimedia Commons.Volta также обнаружил, что, используя различные металлы в свае, можно увеличить количество напряжения.Он описал свои открытия в письме Джозефу Бэнксу, тогдашнему президенту Лондонского королевского общества, в 1800 году. Это было довольно большое дело (Наполеон был весьма впечатлен!), И его изобретение принесло ему устойчивое признание в честь «вольта». ‘(мера электрического потенциала), названная в его честь.
Я сам, шутя в сторону, поражен тем, как мои старые и новые открытия … чистого и простого электричества, вызванного контактом металлов, могли вызвать такое волнение.Алессандро Вольта
Так что же именно происходило с этими слоями цинка и серебра и действительно с подергивающимися лягушачьими лапами?
Химия батареи
Батарея — это устройство, которое накапливает химическую энергию и преобразует ее в электричество.Это известно как электрохимия, а система, лежащая в основе батареи, называется электрохимическим элементом. Батарея может состоять из одного или нескольких (как в оригинальной кучке Вольты) электрохимических ячеек. Каждая электрохимическая ячейка состоит из двух электродов, разделенных электролитом.
Итак, откуда электрохимический элемент получает электричество? Чтобы ответить на этот вопрос, нам нужно знать, что такое электричество. Проще говоря, электричество — это тип энергии, производимый потоком электронов.В электрохимической ячейке электроны образуются в результате химической реакции, которая происходит на одном электроде (подробнее об электродах ниже!), А затем они перетекают на другой электрод, где расходуются. Чтобы понять это должным образом, нам нужно внимательнее изучить компоненты клетки и то, как они устроены вместе.
Электроды
Чтобы создать поток электронов, вам нужно где-то, чтобы электроны текли из , а где-то электроны текли с на .Это электроды ячейки. Электроны текут от одного электрода, называемого анодом (или отрицательным электродом), к другому электроду, называемому катодом (положительный электрод). Как правило, это разные типы металлов или другие химические соединения.
В котле Вольта анодом служил цинк, от которого электроны текли по проволоке (при подключении) к серебру, которое было катодом батареи. Он сложил много этих ячеек вместе, чтобы получилась общая куча, и поднял напряжение.
Но откуда анод вообще берет все эти электроны? И почему они так счастливы, что их отправили в веселый путь к катоду? Все сводится к химии, происходящей внутри клетки.
Здесь происходит пара химических реакций, которые нам необходимо понять. На аноде электрод вступает в реакцию с электролитом, в результате чего образуются электроны. Эти электроны накапливаются на аноде. Между тем, на катоде одновременно происходит другая химическая реакция, которая позволяет этому электроду принимать электроны.
Технический химический термин, обозначающий реакцию, которая включает обмен электронами, — это реакция окисления-восстановления, обычно называемая окислительно-восстановительной реакцией. Вся реакция может быть разделена на две половинные реакции, и в случае электрохимической ячейки одна полуреакция происходит на аноде, а другая — на катоде. Уменьшение — это усиление электронов, и это то, что происходит на катоде; мы говорим, что катод восстанавливается во время реакции. Окисление — это потеря электронов, поэтому мы говорим, что анод окисляется.
Каждая из этих реакций имеет определенный стандартный потенциал. Думайте об этой характеристике как о способности / эффективности реакции либо производить, либо поглощать электроны — ее силу в электронном перетягивании каната.
- Стандартные потенциалы полуреакций
Ниже приведен список половинных реакций, которые включают высвобождение электронов из чистого элемента или химического соединения. Рядом с реакцией указано число (E 0 ), которое сравнивает силу электрохимического потенциала реакции с силой готовности водорода расстаться со своим электроном (если вы посмотрите вниз по списку, вы увидите, что водородный полуреактион имеет нулевое значение E 0 ).E 0 измеряется в вольтах.
Причина, по которой этот список настолько интересен, заключается в том, что если вы выберете две реакции из списка и объедините их в электрохимическую ячейку, значения E 0 скажут вам, в каком направлении будет протекать общая реакция: реакция с более отрицательной реакцией. Значение E 0 отдает свои электроны другой реакции, и это определяет анод и катод вашей ячейки. Разница между двумя значениями E 0 говорит вам об электрохимическом потенциале вашей ячейки, который в основном представляет собой напряжение ячейки.
Итак, если вы возьмете литий и фторид и сумеете объединить их, чтобы сделать элемент батареи, у вас будет самое высокое напряжение, теоретически достижимое для электрохимического элемента. Этот список также объясняет, почему в котле Вольта цинк был анодом, а серебро — катодом: полуреакция цинка имеет более низкое (более отрицательное) значение E 0 (-0,7618), чем полуреакция серебра (0,7996). .
Источник: UC Davis ChemWiki
Любые два проводящих материала, которые вступают в реакцию с разными стандартными потенциалами, могут образовывать электрохимическую ячейку, потому что более сильный из них сможет забирать электроны у более слабого.Но идеальным выбором для анода был бы материал, который вызывает реакцию со значительно более низким (более отрицательным) стандартным потенциалом, чем материал, который вы выбираете для своего катода. В итоге мы получаем электроны, притягивающиеся к катоду от анода (и анод не очень сильно пытается бороться), и, когда у нас есть легкий путь, чтобы добраться туда — проводящий провод, мы можем использовать их энергию для обеспечения электрического питание нашего фонарика, телефона или чего-то еще.
Разница в стандартном потенциале между электродами как бы равна силе, с которой электроны перемещаются между двумя электродами.Это известно как общий электрохимический потенциал ячейки, и он определяет напряжение ячейки. Чем больше разница, тем больше электрохимический потенциал и выше напряжение.
У нас есть два варианта увеличения напряжения батареи. Мы могли бы выбрать для наших электродов другие материалы, которые придадут ячейке больший электрохимический потенциал. Или мы можем сложить несколько ячеек вместе. Когда элементы объединяются определенным образом (последовательно), это оказывает аддитивное влияние на напряжение батареи.По сути, силу, с которой электроны движутся через батарею, можно рассматривать как общую силу, когда они движутся от анода первого элемента на всем пути, сколько бы ячеек ни содержала батарея, к катоду последнего элемента.
Когда элементы объединяются другим способом (параллельно), это увеличивает возможный ток батареи, который можно рассматривать как общее количество электронов, протекающих через элементы, но не ее напряжение.
Электролит
Но электроды — это всего лишь часть батареи.Помните обрывки бумаги Вольты, пропитанные соленой водой? Соленая вода была электролитом, еще одной важной частью картины. Электролит может быть жидкостью, гелем или твердым веществом, но он должен обеспечивать движение заряженных ионов.
Электроны имеют отрицательный заряд, и поскольку мы посылаем поток отрицательных электронов по нашей цепи, нам нужен способ уравновесить это движение заряда. Электролит обеспечивает среду, через которую могут протекать положительные ионы, уравновешивающие заряд.
Поскольку химическая реакция на аноде производит электроны, для поддержания баланса нейтрального заряда на электроде также производится соответствующее количество положительно заряженных ионов. Они не проходят по внешнему проводу (только для электронов!), А попадают в электролит.
В то же время катод должен также уравновешивать отрицательный заряд электронов, которые он получает, поэтому реакция, которая здесь происходит, должна притягивать положительно заряженные ионы из электролита (альтернативно, он также может высвобождать отрицательно заряженные ионы из электрода в электролит. электролит).
Итак, в то время как внешний провод обеспечивает путь для потока отрицательно заряженных электронов, электролит обеспечивает путь для переноса положительно заряженных ионов, чтобы уравновесить отрицательный поток. Этот поток положительно заряженных ионов так же важен, как и электроны, обеспечивающие электрический ток во внешней цепи, которую мы используем для питания наших устройств. Роль балансировки заряда, которую они выполняют, необходима для поддержания протекания всей реакции.
Так вот, если бы все ионы, высвобожденные в электролит, могли полностью свободно перемещаться через электролит, они в конечном итоге покрыли бы поверхности электродов и забили бы всю систему.Таким образом, в клетке обычно есть какой-то барьер, чтобы этого не произошло.
При использовании аккумулятора возникает ситуация, когда происходит непрерывный поток электронов (через внешнюю цепь) и положительно заряженных ионов (через электролит). Если этот непрерывный поток остановлен — если цепь разомкнута, например, когда ваш фонарик выключен — поток электронов остановлен. Заряды будут накапливаться, и химические реакции, приводящие в движение аккумулятор, прекратятся.
По мере использования батареи и протекания реакций на обоих электродах возникают новые химические продукты.Эти продукты реакции могут создавать своего рода сопротивление, которое может помешать продолжению реакции с такой же эффективностью. Когда это сопротивление становится слишком большим, реакция замедляется. Электронное перетягивание каната между катодом и анодом также теряет свою силу, и электроны перестают течь. Аккумулятор медленно разряжается.
Зарядка аккумулятора
Некоторые распространенные батареи предназначены только для одноразового использования (так называемые первичные или одноразовые батареи).Электроны перемещаются от анода к катоду в одну сторону. Либо их электроды истощаются по мере того, как они выделяют свои положительные или отрицательные ионы в электролит, либо накопление продуктов реакции на электродах препятствует продолжению реакции, и это делается и вытирается пыль. Батарея оказывается в мусорном ведре (или, надеюсь, на переработку, но это уже другая тема Nova).
Но. Изящная вещь в этом потоке ионов и электронов, который имеет место в некоторых типах батарей с соответствующими материалами электродов, заключается в том, что он также может двигаться в обратном направлении, возвращая нашу батарею в исходную точку и давая ей совершенно новую жизнь. .Подобно тому, как батареи изменили способ использования различных электрических устройств, аккумуляторные батареи еще больше изменили полезность этих устройств и их продолжительность жизни.
Когда мы подключаем почти разряженную батарею к внешнему источнику электричества и отправляем энергию обратно в батарею, происходит обратная химическая реакция, которая произошла во время разряда. Это отправляет положительные ионы, выпущенные из анода, в электролит, обратно к аноду, а электроны, которые катод принимает, также обратно к аноду.Возврат как положительных ионов, так и электронов обратно в анод подготавливает систему, так что она снова готова к работе: ваша батарея заряжена.
Однако процесс не идеален. Замена отрицательных и положительных ионов электролита обратно на соответствующий электрод при перезарядке аккумулятора не такая аккуратная и не такая хорошо структурированная, как электрод вначале. Каждый цикл зарядки приводит к еще большему ухудшению состояния электродов, а это означает, что аккумулятор со временем теряет производительность, поэтому даже аккумуляторные батареи не работают вечно.
В течение нескольких циклов зарядки и разрядки форма кристаллов аккумулятора становится менее упорядоченной. Это усугубляется, когда аккумулятор разряжается / заряжается с высокой скоростью — например, если вы едете на электромобиле с большой скоростью, а не с постоянной скоростью. Высокоскоростное переключение приводит к тому, что кристаллическая структура становится более неупорядоченной, что приводит к менее эффективной батарее.
Эффект памяти и саморазряд
Почти, но не полностью обратимые реакции разряда и перезарядки также способствуют так называемому «эффекту памяти».Когда вы перезаряжаете некоторые типы аккумуляторных батарей, не разрядив их сначала, они «запоминают», где находились в предыдущих циклах разрядки, и не перезаряжаются должным образом.
В некоторых элементах это вызвано тем, как металл и электролит реагируют с образованием соли (и тем, как эта соль затем снова растворяется и металл заменяется на электродах при перезарядке). Мы хотим, чтобы наши клетки имели красивые, однородные, маленькие кристаллы соли, покрывающие идеальную металлическую поверхность, но это не то, что мы получаем в реальном мире! Некоторые кристаллы образуются очень сложно, а некоторые металлы откладываются во время перезарядки, поэтому некоторые типы батарей имеют больший эффект памяти, чем другие.Дефекты в основном зависят от первоначального состояния заряда батареи, температуры, напряжения заряда и тока зарядки. Со временем недостатки в одном цикле зарядки могут вызвать то же самое в следующем цикле зарядки и так далее, и наша батарея накапливает некоторые плохие воспоминания. Эффект памяти силен для некоторых типов элементов, таких как батареи на никелевой основе. Другие типы, такие как литий-ионные, не страдают этой проблемой.
Другой аспект аккумуляторных батарей заключается в том, что химический состав, который делает их перезаряжаемыми, также означает, что они имеют более высокую тенденцию к саморазряду.Это когда внутренние реакции происходят внутри аккумуляторного элемента, даже когда электроды не подключены через внешнюю цепь. Это приводит к тому, что клетка со временем теряет часть своей химической энергии. Высокая скорость саморазряда серьезно ограничивает срок службы аккумуляторов — и приводит к их разрядке во время хранения.
Литий-ионные аккумуляторы в наших мобильных телефонах имеют довольно хорошую скорость саморазряда около 2–3 процентов в месяц, и наши свинцово-кислотные автомобильные аккумуляторы также довольно разумны — они, как правило, теряют 4–6 процентов. месяц.Никелевые батареи теряют около 10–15 процентов своего заряда в месяц, что не очень хорошо, если вы планируете хранить фонарик в течение всего сезона, когда он вам не нужен! Неперезаряжаемая щелочная батарея теряет около 2–3% своего заряда в год.
Напряжение, сила тока, мощность, емкость… в чем разница?
Все эти слова в основном описывают мощность батареи, не так ли? Ну вроде как.Но все они немного разные.
Напряжение = сила, при которой реакция, приводящая в движение аккумулятор, проталкивает электроны через элемент. Это также известно как электрический потенциал и зависит от разницы потенциалов между реакциями, которые происходят на каждом из электродов, то есть от того, насколько сильно катод оттянет электроны (через цепь) от анода. Чем выше напряжение, тем больше работы может совершить то же количество электронов.
Ток = количество электронов, которые проходят через любую точку цепи в данный момент времени.Чем выше ток, тем больше работы он может выполнять при том же напряжении. Внутри ячейки ток можно также рассматривать как количество ионов, проходящих через электролит, умноженное на заряд этих ионов.
Мощность = напряжение x ток. Чем выше мощность, тем быстрее батарея может работать — это соотношение показывает, как напряжение и ток важны для определения того, для чего подходит батарея.
Емкость = мощность батареи как функция времени, которая используется для описания продолжительности времени, в течение которого батарея может обеспечивать питание устройства.Аккумулятор большой емкости сможет проработать более длительный период, прежде чем разрядится / разрядится. У некоторых батарей есть небольшая печальная особенность — если вы слишком быстро попытаетесь извлечь из них слишком много энергии, химические реакции не успеют поспеть, и емкость станет меньше! Итак, мы всегда должны быть осторожны, когда говорим о емкости батареи, и помнить, для чего она будет использоваться.
Еще один популярный термин — «плотность энергии». Это количество энергии, которое устройство может удерживать на единицу объема, другими словами, сколько энергии вы получите за свои деньги с точки зрения мощности по сравнению сразмер. С батареей, как правило, чем выше плотность энергии, тем лучше, так как это означает, что батарея может быть меньше и компактнее, что всегда является плюсом, когда вам нужно заряжать то, что вы хотите держать в кармане. Для электромобилей это даже плюс — аккумулятор должен как-то влезать в машину!
Для некоторых приложений, таких как хранение электроэнергии на возобновляемых электростанциях, таких как ветряная или солнечная ферма, высокая плотность энергии не является большой проблемой, поскольку в них, скорее всего, будет достаточно места для хранения батарей.Основная цель такого использования — просто хранить как можно больше электроэнергии, как можно безопаснее и дешевле.
Почему так много типов?
Ряд материалов (раньше это были просто металлы) могут использоваться в качестве электродов в батарее. За прошедшие годы было опробовано много-много различных комбинаций, но лишь немногие из них действительно прошли дистанцию.Но зачем вообще использовать разные комбинации металлов? Если у вас есть пара металлов, которые хорошо работают вместе в качестве электродов, зачем возиться с другими?
Различные материалы имеют разные электрохимические свойства, поэтому они дают разные результаты, когда вы соединяете их в батарейном элементе. Например, некоторые комбинации будут производить высокое напряжение очень быстро, но затем быстро падают, не в состоянии поддерживать это напряжение в течение длительного времени. Это хорошо, если вам нужно произвести, скажем, внезапную вспышку света, такую как вспышка фотоаппарата.
Другие комбинации будут производить только тонкую струйку тока, но они будут поддерживать эту струю вечно. Например, нам не нужен большой ток для питания детектора дыма, но мы хотим, чтобы наши детекторы дыма работали долгое время.
Еще одна причина для использования различных комбинаций металлов заключается в том, что часто для получения требуемого напряжения необходимо уложить два или более элемента батареи друг на друга, и оказывается, что некоторые комбинации электродов складываются вместе намного удобнее, чем другие комбинации.Например, литий-железо-фосфатные батареи (тип литий-ионных аккумуляторов), используемые в электромобилях, складываются вместе для создания систем высокого напряжения (100 или даже более вольт), но вы никогда не сделаете этого с теми батареями NiCad Walkman, которые имеют горячий!
Наши различные потребности с течением времени привели к разработке огромного количества типов батарей. Чтобы узнать больше о них и о том, что ждет аккумулятор в будущем, ознакомьтесь с другими нашими темами о Nova.
Эта тема является частью нашей серии из четырех статей об аккумуляторах.Для дальнейшего чтения ознакомьтесь с типами аккумуляторов, литий-ионных аккумуляторов и аккумуляторов будущего. Уход за солнечной батареей, техническое обслуживание и безопасность: не прикасайтесь к клеммам!
Если вы новичок в использовании возобновляемых источников энергии и не знаете, что означают такие термины, как удельный вес и сульфатация, вы попали в нужное место. В нашей недавней статье о солнечных батареях мы познакомили вас с различными типами батарей, которые могут вам потребоваться для вашей солнечной энергетической системы .
Связанная статья : Системы хранения на солнечных батареях: если вы не можете отличить AGM от своего геля
Теперь, когда вы выбрали батарейки, вы определенно захотите позаботиться о них, чтобы продлить срок их службы. Забота о ваших солнечных батареях — один из лучших способов продлить срок службы ваших батарей и снизить эксплуатационные расходы вашей автономной солнечной системы электроснабжения. При неправильном обращении аккумуляторы могут выйти из строя в течение нескольких недель, оставив вас сломанным и в темноте.Эта статья будет разбита на два раздела. Во-первых, мы рассмотрим основную теорию свинцово-кислотных аккумуляторов, чтобы вы могли понять, что происходит, и, что более важно, что может пойти не так внутри вашей системы. Далее мы расскажем, как безопасно обращаться со своими батареями, независимо от того, залиты ли они (FLA) или регулируются клапаном (VRLA). Батареи с регулируемым клапаном включают как гелевые, так и AGM-аккумуляторы.
Знакомство с солнечной батареей — немного электрохимии
Если ваши глаза закатываются, когда вы начинаете думать о химии в средней школе, вы можете перейти к следующему разделу, но для тех, кому нужен учебник по батареям, читайте здесь.Батарея состоит из трех основных частей: электродов , электролита и сепаратора . В батарее всегда есть как минимум два электрода, одна положительная клемма и одна отрицательная клемма. Положительный вывод называется катодом (вы можете запомнить это, написав как ca + hode). Отрицательный вывод называется анодом. Электролит — это жидкость, в которую помещены электроды. Он позволяет заряду течь между катодом и анодом. Сепаратор предотвращает прямое соединение анода и катода.Это означает, что электроны должны пройти через провод, чтобы завершить электрохимическую реакцию.
Свинцово-кислотные батареи состоят из ряда свинцовых пластин (электродов) в разбавленном растворе серной кислоты (электролите). При разряде атомы кислорода из оксида свинца (PbO 2 ) в положительной пластине реагируют с атомами водорода из серной кислоты (H 2 SO 4 ) в электролите. Как вы, наверное, догадались, они будут производить воду (H 2 O).Между тем сульфат свинца (PbSO 4 ) также образуется на катоде и аноде. Итак, в целом можно сказать, что во время разряда сульфат-ионы покидают электролит и образуется вода. Во время зарядки реакция идет в обратном направлении, образуя оксид свинца на катоде. При перезарядке может выделяться водород, что создает риск взрыва, поскольку водород легко воспламеняется. Поэтому правильное обращение с батареями и уход за ними имеют решающее значение.
Понимание различных стандартов и терминов, используемых для описания аккумуляторов, будет иметь решающее значение при уходе за аккумулятором.В таблице ниже представлены те, с которыми вы, скорее всего, столкнетесь.
Общий уход и обслуживание: как максимально эффективно использовать солнечные батареи
Целью ухода за аккумулятором и технического обслуживания является повышение производительности и срока службы аккумулятора. Срок службы батареи — это очень изменчивое свойство, которое зависит от всех видов факторов, таких как температура хранения и глубина разряда (DOD).
Около 80% отказов вызвано сульфатом , процессом, при котором кристаллы серы образуются на свинцовых пластинах батареи и предотвращают химические реакции.Сульфатирование происходит, когда аккумулятор имеет низкий заряд или уровень электролита. Из-за опасности сульфатирования очень важно отслеживать, поддерживать и контролировать эти два фактора в затопленных аккумуляторах . Для этого вам понадобится дистиллированная вода, цифровой вольтметр, термокомпенсирующий ареометр и соответствующие средства защиты.
Помните, вы не можете и не должны проверять уровень жидкости и удельный вес в AGM и гелевых батареях. Таким образом, первые два шага применимы только к залитым батареям.
Как проверить уровень жидкости
Вы делаете это только для негерметичных аккумуляторов (FLA) — это свинцово-кислотные аккумуляторы с жидким электролитом. Откройте крышку батарейного отсека и загляните внутрь. В ячейки следует доливать дистиллированную воду так, чтобы не было видно металлических поверхностей свинца. У большинства батарей есть «линия заполнения», указывающая, где должен быть уровень электролита. Максимальный уровень жидкости примерно на 1/2 дюйма ниже крышки. Не переполняйте батареи, вы не хотите, чтобы они пролились!
Как проверить уровень заряда
Определите степень заряда или глубину разряда (DOD), проверив удельный вес и напряжение аккумулятора.Приведенная ниже таблица удельного веса поможет вам определить уровень заряда аккумулятора. Если ваши батареи на 6 В вместо 12 В, просто разделите напряжение на два. Аналогичным образом удвойте значения напряжения для системы 24 В.
Если вы не отслеживаете эти два фактора должным образом, ваша батарея подвергнется значительной сульфатации. Если это произойдет, вы можете перезарядить аккумулятор, как показано в этом видео на YouTube, чтобы минимизировать потери эффективности. Но это не могло полностью изменить ущерб.
Как заряжать аккумуляторы
Все домовладельцы, не использующие солнечную энергию, должны иметь общее представление о цикле зарядки аккумулятора. Есть три фазы зарядки: поплавок, насыпь и абсорбция. Вам нужно знать только основы этих фаз:
- Плавающая зарядка, также называемая непрерывной зарядкой, заключается в зарядке аккумулятора с той же скоростью, с которой он разряжается. Это просто держит батареи полностью заряженными.
- Массовая зарядка происходит, когда вы начинаете заряжать разряженный аккумулятор.Напряжение повышается до максимально допустимого уровня.
- Абсорбционная зарядка следует за групповым этапом. Напряжение поддерживается постоянным на максимальном уровне, а ток начинает уменьшаться до тех пор, пока аккумулятор не будет полностью заряжен.
Если вы устанавливаете регулируемый контроллер заряда, вам нужно будет установить плавающее, объемное и абсорбционное напряжение заряда. Убедитесь, что они такие же, как рекомендованные производителем батареи. Для систем солнечного электричества время, в течение которого происходит зарядка от солнечных панелей, может быть слишком коротким для прохождения полной фазы накопления и поглощения.В этом случае можно обойтись установкой одинакового напряжения для обеих фаз. Для получения информации о конкретных значениях зарядного напряжения обратитесь к производителю или обратитесь к паспорту аккумулятора.
Как чистить батареи
Клеммы аккумулятора необходимо регулярно очищать смесью пищевой соды и дистиллированной воды с помощью щетки для очистки клемм аккумулятора. Затем промойте клеммы водой, убедитесь, что все соединения герметичны, и нанесите на металлические компоненты коммерческий герметик или высокотемпературную смазку.Конечно, перед чисткой обязательно снимите зажимы (сначала отрицательные).
Как заменить батареи
При замене старых батарей имейте в виду, что их работа может быть снижена из-за «смешивания». Когда старые и новые батареи используются вместе, новые батареи быстро ухудшаются до качества старых. По этой причине смешивание старых и новых батарей — огромная трата ваших денег. Избегайте этого, правильно ухаживая за батареями, чтобы у всех был хороший срок службы.
Как безопасно использовать батареи
Как упоминалось ранее, свинцово-кислотные батареи выделяют водород, который воспламеняется в присутствии кислорода. Фактически, ракеты «Сатурн-5» использовали водород и кислород в качестве топлива на своих верхних ступенях. Чтобы предотвратить накопление ракетного топлива в вашем аккумуляторном блоке, подключите коробку к улице с помощью вентиляционных труб и убедитесь, что система хорошо вентилируется. В некоторых системах также используются вентиляторы, которые помогают отводить газы.
Если у вас есть система резервного питания от батарей, которая срабатывает при отключении электроэнергии, она должна работать после нескольких месяцев или даже лет простоя.Чтобы убедиться, что он будет работать, батареи должны оставаться полностью заряженными. Если вы позволите батарее просто сидеть там, она постепенно разряжается. Режим зарядки, при котором аккумуляторы остаются заряженными, называется непрерывной зарядкой. Поэтому, чтобы позаботиться о резервном банке аккумуляторных батарей, лучше всего использовать аккумуляторы AGM, которые мы обсудим ниже, потому что они практически не требуют обслуживания, и подзарядить их от небольшой солнечной панели или другого источника электроэнергии. Если вы используете хорошую настройку, ваши солнечные батареи могут прослужить 8 лет.
Батареи опасны
Необходимо соблюдать надлежащие меры предосторожности, когда вы находитесь рядом с аккумуляторным блоком. Используйте толстые перчатки и защитные очки и снимите все металлические предметы. Меньше всего вам нужно обжечься кислотой или ударить током. На случай утечки кислоты убедитесь, что рядом с батареями есть пищевая сода и вода. Их можно использовать для нейтрализации кислоты.
Солнечные батареи VRLA и FLA: разные требования к обслуживанию и уходу
Солнечные батареи следует обслуживать, как мы описали выше, но также существуют некоторые другие требования в зависимости от того, какой у вас аккумулятор: гелевый, AGM или залитый.В этом разделе мы укажем на некоторые из этих различий.
Батареи FLA (залитые)
Большую часть того, что вам нужно знать о негерметичных свинцово-кислотных аккумуляторах, можно найти выше. Наиболее важное различие между FLA и VRLA заключается в том, что залитые батареи необходимо повторно заправлять. Давайте перейдем к конкретным рекомендациям по уходу за залитыми свинцово-кислотными батареями.
- Зарядка аккумуляторов FLA — Залитые аккумуляторы имеют самый большой допуск по напряжению зарядки среди аккумуляторов, которые мы обсуждаем в этой статье.Чтобы правильно зарядить батареи FLA, купите соответствующий контроллер заряда и используйте соответствующую программу зарядки.
- Заправка батарей FLA — Не прикасайтесь к электролиту и не используйте морскую воду для заправки батарей. Используйте только дистиллированную воду. Когда в ячейку добавляется морская вода, происходит химическая реакция, в результате которой образуется газообразный хлор. Этот газ очень опасен и использовался в химической войне Первой мировой войны. Что касается электролита, то свинцово-кислотные аккумуляторы содержат концентрированный кислотный электролит, который обожжет вас при прикосновении.
- Ориентация батарей FLA — Залитые свинцово-кислотные батареи никогда не должны храниться на боку. В отличие от батарей VRLA, они предназначены только для работы в вертикальном положении.
- Вентиляционные батареи FLA — Эти батареи необходимо хранить в хорошо вентилируемых помещениях. Если у вас есть какие-либо проблемы с вентиляцией аккумуляторной батареи, не рекомендуется использовать залитые элементы. См. Предыдущий раздел для получения полной информации о вентиляции.
VRLA (гель и AGM)
После установки батареи VRLA не требуют такого ухода, как батареи FLA, поскольку их не нужно повторно заряжать. Также нельзя измерить степень заряда с помощью ареометра. Поэтому первые две темы в разделе выше не относятся к этим батареям. Однако есть и другие важные различия между залитыми батареями и гелевыми / AGM батареями.
- Зарядка аккумуляторов VRLA — Зарядное напряжение для аккумуляторов AGM очень точное и должно поддерживаться, чтобы они имели приличный срок службы.Слишком высокое напряжение приведет к нагреву батарей, выделению газообразного водорода и необратимому повреждению (утечки газообразного водорода необратимы в негерметичных элементах). Это особенно верно для гелевых аккумуляторов, где чувствительность к зарядному напряжению является очень частым источником сбоев. Вы также должны быть осторожны при зарядке аккумуляторов AGM, хотя они имеют больший допуск. В обоих случаях купите контроллер заряда, предназначенный для вашего типа аккумулятора.
- Заправка батарей VRLA — Это невозможно.Батареи VRLA герметичны, поэтому их нельзя заправлять водой или контролировать удельный вес. Но не волнуйтесь, батареи сконструированы таким образом, что в этих этапах обслуживания нет необходимости.
- Ориентация батарей VRLA — VRLA сконструирована таким образом, что они могут работать на своих сторонах. Это дает вам больше гибкости при хранении батарей.
- Вентиляционные батареи VRLA — Батареи VRLA очень универсальны.Им требуется меньше вентиляции, чем залитым батареям, потому что они разряжают газ только при перезарядке. Если вы устанавливаете батареи в зоне с несовершенной вентиляцией, AGM или гелевые батареи могут быть более безопасным способом. Это не означает, что не следует предпринимать никаких мер предосторожности.
Пять способов продлить срок службы свинцово-кислотной батареи. Часть I [Victron Energy]
Хотя высококачественные батареи изначально дороже, они также более надежны, а их более длительный срок службы позволяет окупить вложения в долгосрочной перспективе.
Их продолжительность напрямую зависит от того, как их используют… или злоупотребляют. Простое знание того, что вы должны и чего не должны делать с батареей, сэкономит вам тысячи — если ваш аккумулятор большой. Давайте подробнее рассмотрим батареи и пять простых способов продлить их жизнь …
В этой статье мы рассмотрим основные причины преждевременного выхода батареи из строя, а именно:
Разрядился аккумулятор… затем не удалось подзарядить
Постоянная недозарядка
Перезарядка
Слишком быстрая зарядка
Игнорирование температурных соображений
Эта статья посвящена свинцовым батареям.Есть также много других типов батарей, таких как литиевые, но эта информация касается конкретно свинца.
Чтобы понять, что происходит внутри батареи, нам нужно знать, как она устроена, и что происходит, когда мы ее разряжаем и перезаряжаем.
Ячейка свинцово-кислотной батареи составляет примерно 2 В. Таким образом, батарея 12 В состоит из шести ячеек, каждая из которых состоит из двух свинцовых пластин, погруженных в разбавленную серную кислоту (электролит), которая может быть либо жидкостью, либо гелем.Оксид свинца не твердая, а губчатая и должна поддерживаться сеткой. Пористость свинца в этом состоянии делает его полностью доступным для электролита, позволяя относительно легко протекать химической реакции по всей толщине пластины, поскольку батарея выполняет свою задачу по хранению и высвобождению энергии.
Эта химическая реакция довольно сложна, но мы должны отметить только пару вещей о ней: когда энергия потребляется от батареи, серная кислота теряется из электролита и соединяется с пластинами свинца с образованием сульфата свинца.И наоборот — перезарядка батареи заставляет сульфат покинуть свинцовые пластины и снова вернуться к электролиту, образуя разбавленную серную кислоту. Второе, что нам нужно заметить, это то, что если зарядное напряжение слишком высокое или поддерживается слишком долго, начинается серьезная другая химическая реакция: вода в электролите разлагается на кислород и водород.
Разложение воды в электролите на кислород и газообразный водород (электролиз) является нормальным явлением на заключительных этапах зарядки аккумулятора, но обычно весьма ограничено.Батареи с влажными элементами требуют периодического доливания (деионизированной) воды для замены жидкости, которая была потеряна с течением времени. Батареи, не требующие особого обслуживания, не нуждаются в дозаправке — фактически, их нельзя дозаправить, потому что они герметичны. Герметизация батареи предотвращает утечку газов водорода и кислорода; вместо этого они рекомбинируют под давлением, газы улавливаются и повторно абсорбируются во время цикла разряда. Однако такие батареи снабжены клапаном сброса давления на случай переизбытка газа, вызванного зарядкой при слишком высоком напряжении.Позже мы посмотрим на напряжение заряда.
Циклическое движение сульфата между свинцовыми пластинами и электролитом, вызванное движением электронов, звучит довольно просто — так что же может пойти не так? В основном три вещи:
Губчатые свинцовые пластины могут быть покрыты твердым слоем кристаллов сульфата свинца, который препятствует доступу к пластинам. Это состояние называется сульфатацией — в конечном итоге оно закрывает доступ к емкости аккумулятора.Связная структура свинца разрушается, и часть свинца отваливается — такое разрушение пластин известно как «осыпание». Электролит — жидкость или гель — разлагается и теряется в виде газа. Электролит является агентом химической реакции — когда он сильно снижен или отсутствует, батарея не может работать.
Это основные болезни, которые вызывают либо неприемлемую потерю емкости батареи, либо вообще неспособность сохранять или высвобождать энергию. Есть и другие.
Что еще хуже, функциональные ограничения, вызванные любым из этих разрушительных событий, часто вызывают второй или третий режим отказа.
Есть несколько способов уничтожить даже совершенно новую батарею за неделю или меньше — и это те, которые мы рассмотрим в первую очередь … но прежде чем мы это сделаем, давайте установим несколько общих правил использования нашей батареи, не вызывая ее ущерб, сокращающий жизнь.
При выборе размера (емкости) аккумулятора для нашей работы помните, что он прослужит дольше всего, если он никогда не будет разряжен более чем на половину своей емкости… другими словами, он никогда не разряжается ниже 50% уровня заряда (SOC).
Частично разряженные батареи необходимо как можно скорее зарядить. Повреждение вызвано оставлением их в частично заряженном состоянии… чем ниже заряд; и чем дольше аккумулятор остается в разряженном состоянии, тем больше повреждения.
Безопасно переключать батарею между 50% SOC и 80% SOC — это тоже довольно эффективно. Но такая езда на велосипеде не может продолжаться длительное время. Перезарядка разряженного аккумулятора до уровня заряда примерно 80% может быть достигнута быстро, но возврат аккумулятора к 100% SOC занимает гораздо больше времени, потому что скорость, с которой он может принимать заряд, очень сильно снижается по мере приближения к полной зарядке.Важно обеспечить необходимое время для зарядки, чтобы вернуть батарею к 100% SOC не реже одного раза в 30 циклов — это ежемесячно для батареи, которая используется каждый день. Для этого есть несколько причин, о которых мы поговорим чуть позже.
Изображение батареи в разрезе принадлежит Sun.solanki и использовалось без изменений.
На следующей неделе мы посмотрим, что происходит, когда аккумулятор слишком сильно разряжается… и затем остается в разряженном состоянии.
Пожалуйста, подпишитесь на эту страницу, чтобы получать уведомление, когда она будет опубликована.
Джастин Тайерс
&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&&
Слишком глубокая разрядка и оставление аккумулятора «разряженным»
Худшее обращение с аккумулятором (кроме получения опасно высокого зарядного напряжения) — это полностью разряжать аккумулятор и хранить его без подзарядки.
Что происходит, когда батарея глубоко разряжена — особенно ниже 20% SOC — пластина механически повреждается из-за обширного образования кристаллов серы, которые подрывают сцепление материала. Часть материала рассыпается и начинает отпадать. Этот процесс деградации будет происходить в любом случае по мере старения батареи, но глубокая разрядка батареи значительно ускоряет этот процесс.
Вот и все, что касается слишком глубокой разрядки: если затем оставить аккумулятор в разряженном состоянии, то образовавшиеся крошечные кристаллы сульфата начинают расти.Сульфат на поверхности пластин начинает затвердевать — в конечном итоге образуя непроницаемое твердое белое покрытие вокруг свинцовой пластины, которое закупоривает пористость материала — и значительно препятствует диффузии ионов, которые управляют химическим процессом. На этом этапе емкость батареи и ее способность принимать или отдавать энергию будут настолько медленными, что она не сможет выполнять ту работу, для которой была выбрана.
Такое повреждение аккумулятора происходит, например, когда фары автомобиля оставлены включенными, и автомобиль не используется в течение нескольких дней или недель … или если аккумулятор оставлен на полке в мастерской в течение нескольких месяцев, и он саморазрядился, пока не станет плоским.Почти несомненно, что в обоих случаях аккумулятор придется утилизировать.
Если какое-либо повреждение является обратимым, его можно устранить, перезарядив аккумулятор обычным способом (это может быть медленным, если он будет заряжаться), а затем применяя выравнивающий заряд, пока напряжение аккумулятора не достигнет 16 В или 17 В (для аккумулятора 12 В ) в течение, скажем, трех часов. Это заставит сульфатированные участки пластины высвободить сульфат обратно в электролит. Успех не гарантируется, и почти во всех случаях будет некоторая необратимая потеря мощности.
Будьте очень осторожны, внимательно следите за аккумулятором при этих высоких напряжениях заряда, так как это также приведет к разделению электролита на газ.
Слишком быстрая зарядка аккумулятора
Батарею следует заряжать током не более 20% от ее емкости. Например, если батарея рассчитана на 100 ампер / час, ее максимальный зарядный ток не должен превышать 20 ампер. Разряженный аккумулятор способен выдерживать гораздо более высокие уровни заряда — в течение короткого времени, — но этого типа зарядки следует избегать.Например, генераторы с высокой выходной мощностью обещают очень эффективную и быструю перезарядку аккумуляторов, но высокие токи заряда нарушают сцепление свинцовых пластин, что приводит к отслаиванию материала пластин и ускорению старения.
Сначала это «только» снижает емкость батареи — позже, когда потерянный материал накапливается в нижней части батареи, он в конечном итоге коснется и положительной, и отрицательной пластины, создавая короткое замыкание, и элемент перестанет работать. Батарея потеряет напряжение от этой ячейки (отказ других ячеек не будет далеко позади).
Слишком быстрая зарядка аккумулятора усугубляет то, что быстрая зарядка увеличивает температуру аккумулятора. Контролируемый цикл зарядки для конкретной батареи — напряжения, при которых она заряжается во время каждой из трех фаз зарядки — были рассчитаны с предположением, что температура батареи составляет 20ºC (обычно), при более высоких температурах напряжения заряда должны быть уменьшены. Неспособность снизить зарядные напряжения приводит к большему повреждению когезии свинцовой пластины и выделению электролита (электролиз), что быстро снижает количество электролита в батарее с влажными элементами.В герметичных батареях проблема еще хуже: клапаны давления будут выпускать газ, чтобы избежать разрушения корпуса батареи, и потерянный электролит не может быть заменен.
Стоит отметить, что не все батареи одинаковы, и что некоторые из них, например, спиральные батареи, могут противостоять эффекту быстрой зарядки лучше, чем другие.
Повторяющаяся неспособность полностью зарядить аккумулятор
Большинство из нас следят за состоянием заряда батареи с помощью грубого и готового метода «наблюдения за напряжением батареи».Например, в представленной выше установке с быстрой зарядкой напряжение нарастает так быстро, что создается иллюзия, что наша батарея полностью заряжена, и поэтому мы можем завершить цикл зарядки, полагая, что работа почти завершена. Хотя батареи, заряжаемые и разряженные таким образом, на самом деле более «эффективны» (в том смысле, что большая часть энергии, передаваемой батарее, поглощается батареей), короткие резкие циклы зарядки приводят к постоянной недозарядке. Повторяющаяся недозарядка вызывает три проблемы:
Недозаряженная пластина батареи не вернула все сульфаты в электролит.Как было замечено ранее, кристаллы сульфата, оставленные на некоторое время, начинают формировать твердое покрытие — сульфатирование. Мы уже упоминали, что это покрытие снижает емкость аккумулятора, но оно также приводит к более высокому сопротивлению зарядке, требуя гораздо более длительного времени зарядки … что, в свою очередь, увеличивает вероятность недозарядки, что приводит к дальнейшей сульфатации. Мы должны разорвать этот круг ухудшения.
Расслоение электролита — это состояние, о котором мы еще не упомянули — оно возникает, когда электролит остается статическим и «несмешанным» в течение длительного периода.Кислота, будучи более плотной, чем вода, падает на дно электролита и остается там, если электролит каким-либо образом не перемешивается. Это волнение может быть, когда транспортное средство или лодка, в которых установлена батарея, начинает двигаться или катиться. В статической установке электролит перемешивается только тогда, когда во время перезарядки достигается напряжение выделения газа, и пузырьки газа, поднимающиеся через электролит, тщательно перемешивают его. Стратифицированный электролит слабее вверху и сильнее внизу, в результате чего большая часть химической реакции происходит внизу на свинцовых пластинах.В этом случае нижняя часть пластин выполняет всю работу, в то время как верхняя часть пластин находится в отпуске, так что пластина будет стареть быстрее, чем если бы работа распределялась более равномерно.
Наконец, мы упомянули, что батарея на 12 В состоит из шести ячеек. Эти элементы никогда не бывают полностью идентичными — некоторые будут иметь меньшую емкость, некоторые будут заряжаться медленнее. Важно убедиться, что все ячейки периодически достигают полной перезарядки, чтобы они находились в гармонии друг с другом — в противном случае ячейки, которые были немного хуже по производительности, постепенно ухудшаются: их емкость снижается, а скорость снижается. которые они могут перезаряжаться, становится медленнее, и они начинают все больше и больше отставать в производительности по сравнению с другими ячейками.Этот процесс приведения клеток в гармонию называется выравниванием.
Перезарядка:
Перезарядка часто происходит, когда аккумулятор «хранится», но все еще подключен к зарядному устройству. Невозможно принять больше энергии, вода в электролите разлагается на водород и кислород. Уровень электролита упадет ниже уровня пластин, что приведет к непоправимому повреждению этой части пластины — и в конечном итоге батарея полностью высохнет.
Вместо того, чтобы оставлять аккумулятор на постоянной подзарядке во время хранения, лучше оставить его разомкнутым и заряжать каждую неделю или две, чтобы восполнить потерю энергии из-за саморазряда.
Температура
Каждый тип батареи — глубокий цикл / стартер / мокрый элемент / гелевый / спиральный элемент / AGM / регулируемый с помощью клапана — имеет немного разные требования к зарядке или «алгоритм заряда». Эти алгоритмы заряда определяют напряжение, которое должно быть достигнуто перед переходом в новую фазу заряда. Отклонение от этих предустановленных пределов — даже на несколько процентов — оказывает драматическое влияние на то, завершит ли аккумулятор цикл зарядки чрезмерно или недостаточно. И, как мы обсуждали выше, как недостаточная, так и чрезмерная зарядка ускоряют процесс старения или сокращают срок службы батареи.
Чтобы установить алгоритм зарядки батареи, необходимо предположить, что батарея будет иметь стандартную температуру окружающей среды, а стандарт обычно составляет 20 ° C. Но, конечно, такая температура часто неуместна — батареи, используемые в тропиках или полярных регионах, будут храниться при температурах, сильно отличающихся от предполагаемых стандартов; батареи, установленные в горячих машинных отделениях, часто имеют температуру 50 ° C; и температура быстро заряжаемых аккумуляторов также резко возрастет по сравнению с температурой окружающей среды.
Важно, чтобы устройство зарядки аккумулятора имело способность определять температуру аккумулятора и применяло температурную компенсацию к его зарядному напряжению. Например, батарея, температура которой составляет 30 ° C в начале цикла зарядки, может повыситься еще на 10 ° C во время зарядки. Напряжение заряда для этой батареи следует уменьшить на 0,5 В, чтобы избежать повреждения батареи, особенно батарей, которые особенно уязвимы для высоких зарядных напряжений, таких как гель или абсорбирующий стеклянный мат.
Еще одна вещь — при более высоких температурах батареи испытывают ускоренное химическое разложение — каждые 10 ° C повышения температуры выше предполагаемой рабочей температуры вдвое сокращают ожидаемый срок службы батареи.
Итого:
Выбирая аккумулятор, убедитесь, что он подходит для работы, которую он должен выполнять… запуск двигателя или глубокий цикл; резервное питание или скачок напряжения. Убедитесь, что аккумуляторная батарея имеет достаточную емкость, чтобы легко выполнять свою задачу.На практике для долгого срока службы это означает, что емкость должна быть примерно в четыре раза больше требуемой. Убедитесь, что рабочие циклы батареи включают период, когда батареи могут быть медленно доведены до состояния 100% заряда и допустимое время сверх этого времени, чтобы элементы могли выровняться. Это должно быть не реже одного раза в 30 циклов. Установка устройства автоматического отключения нагрузки, чтобы предотвратить разряд батареи ниже уровня, скажем, 20% SOC, может быть лучшим вложением, которое вы можете сделать. Сульфатирование: Свинец и диоксид свинца реагируют с серной кислотой с образованием сульфата свинца — небольших кристаллов, которые легко превращаются обратно в свинец, диоксид свинца и серную кислоту.Со временем часть сульфата свинца не восстанавливается, а образует стабильное кристаллическое покрытие, которое больше не растворяется при перезарядке. Сульфатирование можно уменьшить, если аккумулятор полностью зарядить после цикла разрядки. Сульфатированные батареи содержат меньше свинца, меньше серной кислоты, блокируют поглощение электронов, что приводит к снижению емкости батареи, и могут обеспечивать только часть своего нормального тока разряда. Лучший способ предотвратить это — периодически полностью заряжать аккумулятор.
Изображение раздутой батареи принадлежит Деннису ван Зуйлекому и воспроизведено без изменений.
Джастин Тайерс
Руководство по техническому обслуживанию аккумулятора вилочного погрузчика| BHS
Чем дольше срок службы аккумуляторов погрузчика, тем ниже ваши расходы. Большинство свинцово-кислотных аккумуляторных батарей для вилочных погрузчиков обеспечивают около 2000 циклов зарядки, что обычно составляет около пяти лет службы. Но даже такой срок службы может быть достигнут только при правильном уходе.
Чтобы получить максимальную отдачу от инвестиций, следует установить регулярные интервалы технического обслуживания для всех батарей.При правильном уходе многие свинцово-кислотные батареи могут прослужить намного дольше, чем срок их гарантии, обеспечивая работу вилочных погрузчиков на годы, превышающие типичный срок службы промышленных аккумуляторов.
Существует три основных задачи по техническому обслуживанию, которые обеспечивают надежное обслуживание аккумуляторных батарей вилочного погрузчика: полив элементов, мытье корпуса аккумуляторной батареи и проведение регулярных выравнивающих зарядов. Далее следует подробное объяснение каждой задачи, а также советы по безопасному выполнению каждой работы.
Полив аккумуляторной батареи для вилочного погрузчика
Рисунок 1.Система деионизации воды (WDS-1) очищает воду прямо из-под крана, чтобы максимизировать производительность батареи, а также включает в себя индикатор чистоты, который контролирует состояние системы.
Электролит аккумулятора представляет собой смесь серной кислоты и деионизированной воды (не обязательно дистиллированной воды). Когда уровень воды становится низким, пластины аккумулятора могут находиться на открытом воздухе. Это вызывает окисление, которое необратимо снижает емкость и сокращает общий срок службы батареи.
Помимо потерь воды от простого испарения, в процессе зарядки вода разбивается на составные молекулы.По мере того, как водород и кислород выливаются из вентиляционных отверстий батареи, уровень воды в элементах снижается. Чрезмерная потеря воды может быть признаком того, что батарея выделяет больше газа, чем следовало бы. Если вы заметили, что во время зарядки аккумулятор теряет больше воды, чем обычно, попросите техника проверить аккумулятор и зарядное устройство.
Помните эти советы при поливе аккумуляторов вилочного погрузчика:
- Аккумуляторы только для водных погрузчиков после зарядки, но не до нее. Электролит расширяется во время процесса зарядки, и добавление воды до полной зарядки может привести к чрезмерному поливу, что является основной причиной выкипания.
- Используйте чистую неионизированную воду. Многие муниципалитеты содержат добавки или минералы в водопроводной воде. Эти загрязнители накапливаются на элементах при испарении воды, оставляя слои осадка, уменьшающие емкость аккумулятора. Если вы живете в районе с жесткой водой, используйте систему деионизации воды для очистки воды перед добавлением ее в клетки. (Примечание: некоторые ресурсы рекомендуют дистиллированную воду. Дистиллированная вода часто более чистая, чем деионизированная, но также намного дороже. Правильно деионизированная вода идеально подходит для аккумуляторных батарей вилочных погрузчиков).
- Заполните элементы батареи примерно на 1/4 дюйма над защитным элементом элемента. Это одна из лучших практик в области промышленных аккумуляторов, которую рабочие часто игнорируют. К сожалению, переполнение или недостаточное заполнение элемента батареи может иметь серьезные последствия, о чем мы поговорим чуть позже.
- Для достижения наилучших результатов установите интегрированную систему полива. Эта система устанавливается на шкаф зарядного устройства со шлангами, ведущими к аккумуляторным элементам. Его можно настроить на автоматический полив нескольких батарей, который активируется сразу после завершения цикла зарядки.Сокращение времени зарядки имеет очевидные последствия для вашего предприятия в целом.
- Производители аккумуляторов рекомендуют поливать аккумуляторы для вилочных погрузчиков один раз в неделю. Старые батареи могут потребовать более частого полива, и их следует проверять чаще.
Однако постоянная потребность в поливе может быть признаком того, что с аккумулятором или зарядным устройством что-то не так. Если в одном из блоков постоянно наблюдается низкий уровень воды, проведите тщательный осмотр аккумулятора и его зарядного оборудования.
Узнайте больше в нашем полном руководстве по поливу аккумуляторов для вилочных погрузчиков.
Рекомендации по использованию промышленных аккумуляторов: выравнивающие заряды
Со временем разные ячейки в погрузчиках могут развивать немного разную мощность. Когда это происходит, пользователи не могут заряжать батареи до полной мощности; одна ячейка может быть полностью заряжена, а другая — только наполовину.
Уравнительные заряды предотвращают эту неэффективность. По сути, выравнивающий заряд — это целенаправленная завышенная плата.Типичный цикл зарядки длится около восьми часов, в то время как выравнивающий заряд требует дополнительных трех часов или около того. Зарядные устройства продолжают обеспечивать низкий поток энергии в последние часы.
Эта практика также предотвращает расслоение, потенциально опасное состояние, при котором кислота и вода разделяются внутри клеток. На заключительных этапах выравнивающей зарядки аккумуляторы вилочных погрузчиков выделяют водород и кислород. Эти выходящие газы образуют пузырьки, которые перемешивают электролит, предотвращая расслоение.
Обратите внимание, что для выравнивающих зарядов требуется более длительное время охлаждения, чем при обычном цикле зарядки. Поскольку большинство производителей аккумуляторов рекомендуют еженедельный выравнивающий заряд, многие операторы выполняют эту задачу в выходные дни, оставляя достаточно времени для зарядки и охлаждения перед следующей сменой.
Мойка аккумуляторов для вилочного погрузчика
Существует несколько способов утечки электролита из аккумулятора погрузчика и его накопления на корпусах аккумулятора:
- Поскольку батареи выделяют газ во время зарядки, мелкодисперсный кислотный пар может подниматься к верху ящиков батареи.
- Взбалтываемый электролит может вылиться из вентиляционных отверстий батареи во время процесса зарядки, что обычно называется «выкипанием». Чрезмерный полив клеток увеличивает риск выкипания.
- Из батарей может протекать электролит. Если они хранятся в многоярусных стеллажах, а поддоны не устанавливаются или не меняются регулярно, батареи на верхних уровнях могут капать электролит на расположенные ниже.
Остатки кислоты, скапливающиеся на корпусах аккумуляторных батарей вилочного погрузчика, могут вызвать самые разные проблемы.Во-первых, это может создать токопроводящую цепь между выводами и стальным корпусом. Это вызывает низкоуровневый, но постоянный саморазряд, сжигание циклов зарядки и ограничение срока службы аккумулятора.
Во-вторых, накопление кислоты может вызвать коррозию клемм. Поврежденные клеммы могут вызвать проблемы с электричеством в погрузчиках, а также ограничить емкость аккумулятора. Они могут даже сделать батарею непригодной для использования.
Регулярно протирайте верхнюю часть ящиков батарей с помощью обезжиривающего средства, нейтрализующего кислоту, например, AcidSafe Liquid.Просто убедитесь, что вентиляционные колпачки плотно закрыты перед любой операцией стирки. Случайное введение нейтрализаторов в электролит приведет к разрушению аккумулятора.
В дополнение к регулярной чистке верхней части аккумулятора, а также после выкипания или проливания, тщательно мойте аккумуляторы вилочного погрузчика два-четыре раза в год, в зависимости от использования. Продавец аккумуляторов с комплектом шкафа для мойки аккумуляторов может просто предоставить эту услугу на месте с минимальным временем простоя аккумуляторов для вилочных погрузчиков.
Технические специалисты прибывают с портативным шкафом для мытья батарей с карманами для вилок для облегчения доставки.Два резервуара емкостью 330 галлонов позволяют им забирать пресную воду, собирать весь сток с мытья и уносить использованную воду для повторного использования и / или утилизации в соответствии с федеральными и местными экологическими нормативами.
Советы по безопасности при мытье и поливе аккумуляторов вилочного погрузчика
Рис. 2. Работа с аккумуляторами промышленных вилочных погрузчиков может быть опасной задачей. Важно, чтобы руководство предлагало средства индивидуальной защиты, а персонал принимал меры предосторожности, используя средства индивидуальной защиты.
При техническом обслуживании аккумуляторной батареи вилочного погрузчикасотрудники часто оказываются в непосредственной близости от кислотного электролита, что может вызвать серьезные химические ожоги или даже слепоту.
Управление по охране труда требует, чтобы работодатели предоставляли средства индивидуальной защиты и станции для промывки глаз всем сотрудникам, которые поливают и моют аккумуляторы вилочных погрузчиков. Средства индивидуальной защиты для мытья и полива батарей должны включать:
- Очки для защиты от химикатов
- Брызгозащитный экран
- Кислотостойкая куртка или фартук
- Перчатки кислотостойкие
- Ботинки HAZ-MAT
Помимо защиты от брызг кислоты, персонал аккумуляторной комнаты должен соблюдать все меры безопасности, рекомендованные OSHA.К ним относятся следующие:
- Батарейные помещения являются зоной, свободной от табачного дыма, и должны иметь соответствующие знаки.
- На других вывесках для аккумуляторных батарей должны быть указаны опасности поражения электрическим током, станции для промывки глаз, комплекты для сбора утечек и зоны движения погрузчиков.
- Никогда не носите металлические украшения при работе с аккумуляторными батареями для вилочного погрузчика.
- Избегайте контакта с клеммами или элементами аккумуляторной батареи, чтобы предотвратить электрические ожоги.
- Не используйте металлические инструменты рядом с батареями. Только неискрящие инструменты безопасны для обслуживания аккумуляторной батареи.
- Выбирайте искробезопасное оборудование, чтобы свести к минимуму опасность взрыва.
- Храните батареи только в помещениях с механической вентиляцией и детекторами газообразного водорода.
Контрольный список для обслуживания аккумуляторной батареи вилочного погрузчика
В зависимости от использования и области применения некоторым пользователям вилочных погрузчиков может потребоваться увеличить или уменьшить интервалы технического обслуживания. Однако в качестве общего руководства следуйте этому контрольному списку:
Рис. 3. В качестве общего правила поливайте батареи
еженедельно с помощью водяного пистолета (WGX), ежемесячно очищайте верхнюю часть ящиков батарей с помощью AcidSafe Liquid (ASL) и мойте батареи каждые несколько месяцев в шкафу для мытья батарей (BWC).
Еженедельные задачи обслуживания
- Проверить уровни электролита.
- Водяные элементы при необходимости (после зарядки).
- Проверьте, нет ли остатков на аккумуляторных отсеках; при необходимости очистите с помощью AcidSafe.
- После зарядки измерьте удельный вес с помощью ареометра. Стандартные аккумуляторные батареи для вилочных погрузчиков, полностью заряженные, обычно должны иметь идеальный удельный вес 1,285 (уточните у производителей). Если удельный вес отличается от одной ячейки к другой, попробуйте выравнивающий заряд.
- Обеспечивает выравнивающий заряд с достаточным временем охлаждения.
Ежемесячные задачи обслуживания
- Тщательно осмотрите аккумуляторные батареи. Обратите внимание на признаки коррозии на клеммах. Проверить разъемы и кабели на предмет повреждений.
- Очистите верхнюю часть ящиков батарей с помощью AcidSafe или аналогичного нейтрализующего средства.
- После зарядки измерьте удельный вес с помощью ареометра. Стандартные аккумуляторные батареи для вилочных погрузчиков, полностью заряженные, обычно должны иметь идеальный удельный вес 1.285 (уточняйте у производителей). Если удельный вес отличается от одной ячейки к другой, попробуйте выравнивающий заряд.
Каждые три-шесть месяцев
- Тщательно вымойте батареи. Батарейные моечные шкафы автоматизируют процесс, включая дополнительные нейтрализующие вещества и сушку на воздухе по завершении стирки.
- Отправьте использованные батареи в службы утилизации.
Продавцы аккумуляторов для вилочных погрузчиков могут предлагать пакеты услуг, которые включают все эти услуги по техническому обслуживанию; спросите своего провайдера.В качестве альтернативы, операторы аккумуляторной комнаты могут обеспечить собственное обслуживание, чтобы продлить срок службы всей коллекции аккумуляторов. Тем не менее, независимо от того, кто предоставляет услуги, обслуживание аккумуляторов является важной частью прибыльного парка вилочных электропогрузчиков.
Артикул:
Фауст, Брайан. «Правильный уход, безопасность и обслуживание аккумуляторов вилочного погрузчика». MHLNews. Пентон, 21 ноября 2014 г. Web. 13 декабря 2016 г.
«Инструкции по уходу за аккумулятором вилочного погрузчика». ФлитманКонсалтинг .Fleetman Consulting, n.d. Интернет. 13 декабря 2016 г.
«Механические промышленные грузовики (вилочные погрузчики)». OSHA . Управление по охране труда и технике безопасности, Министерство труда США, n.d. Интернет. 13 декабря 2016 г.
Редель, Кевин. «Зарядка, полив и очистка аккумулятора вилочного погрузчика». Вилочный погрузчик, Америка. Forklift America, 6 марта 2016 г. Интернет. 13 декабря 2016 г.
Скьяво, Брайан. «Это продолжается и продолжается…» FoodLogistics . AC Business Media, 16 декабря.2008. Интернет. 13 декабря 2016 г.
.
 Существуют растворы, позволяющие растворить образовавшийся на пластинах сульфат свинца. Если первый способ можно назвать электрическим, то этот – химическим. Химическая очистка сульфата более эффективна и позволяет добиться очищения более крупного налета сульфата.
Существуют растворы, позволяющие растворить образовавшийся на пластинах сульфат свинца. Если первый способ можно назвать электрическим, то этот – химическим. Химическая очистка сульфата более эффективна и позволяет добиться очищения более крупного налета сульфата.
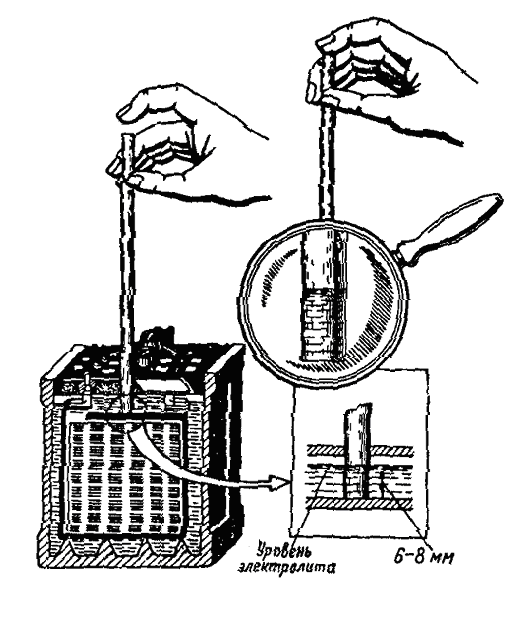 Следы ржавчины на деталях, не покрытых лаком, снимите ветошью, смоченной в керосине;
Следы ржавчины на деталях, не покрытых лаком, снимите ветошью, смоченной в керосине; ..1.45 В;
..1.45 В;

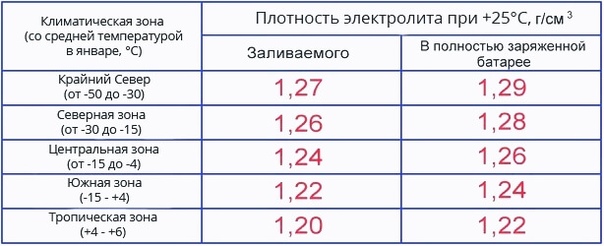 Важно чтобы аккумулятор содержался в чистоте. Эстетически это конечно приятно, но главная причина не в этом, дело в том, что пыль и грязь которые собираются между клеммами, постепенно пропитывается парами электролита и становится проводником электричества. И даже если по счастливому случаю это не приведет к короткому замыканию, то привести к преждевременному разряду точно сможет, а что снижает срок службы аккумулятора скутера.
Важно чтобы аккумулятор содержался в чистоте. Эстетически это конечно приятно, но главная причина не в этом, дело в том, что пыль и грязь которые собираются между клеммами, постепенно пропитывается парами электролита и становится проводником электричества. И даже если по счастливому случаю это не приведет к короткому замыканию, то привести к преждевременному разряду точно сможет, а что снижает срок службы аккумулятора скутера. Снимите крышки заливного отверстия (красные, желтые или зеленые крышки батарейного отсека).
Снимите крышки заливного отверстия (красные, желтые или зеленые крышки батарейного отсека).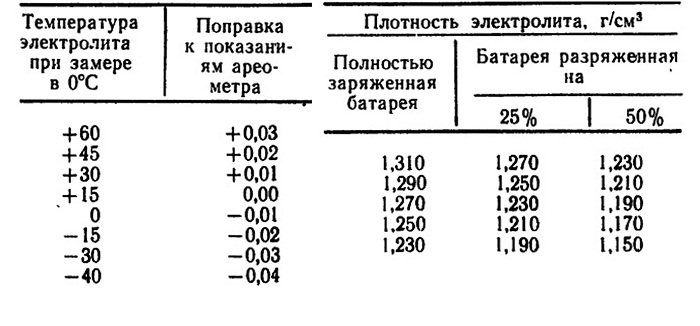 Не используйте воду или другие жидкости для активации батареи. Температура электролита перед заливкой должна быть от 60 до 86 градусов по Фаренгейту. Если электролит хранится в холодном помещении, перед заливкой его следует нагреть до комнатной температуры.Залейте до ВЕРХНЕГО УРОВНЯ, как указано на батарее. Примечание. Никогда не заправляйте и не активируйте аккумулятор, установленный в автомобиле, так как пролив электролита может вызвать повреждение. .
Не используйте воду или другие жидкости для активации батареи. Температура электролита перед заливкой должна быть от 60 до 86 градусов по Фаренгейту. Если электролит хранится в холодном помещении, перед заливкой его следует нагреть до комнатной температуры.Залейте до ВЕРХНЕГО УРОВНЯ, как указано на батарее. Примечание. Никогда не заправляйте и не активируйте аккумулятор, установленный в автомобиле, так как пролив электролита может вызвать повреждение. .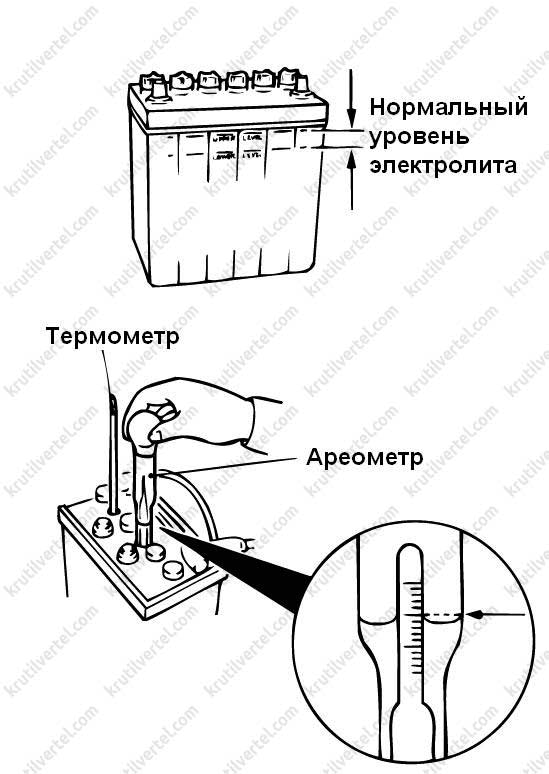 Например, батарею емкостью 14 Ач следует заряжать с током 1,4 ампера (14 Ач ÷ 10 = 1,4 ампера). Удельный вес электролита должен вырасти как минимум до 1,260 на батареях серии 12N. На всех высокопроизводительных батареях (серия YB) должно соблюдаться минимальное показание 1,280.
Например, батарею емкостью 14 Ач следует заряжать с током 1,4 ампера (14 Ач ÷ 10 = 1,4 ампера). Удельный вес электролита должен вырасти как минимум до 1,260 на батареях серии 12N. На всех высокопроизводительных батареях (серия YB) должно соблюдаться минимальное показание 1,280.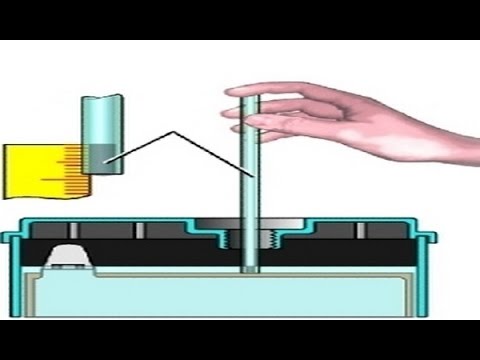 Высушите аккумуляторный отсек и установите аккумулятор.
Высушите аккумуляторный отсек и установите аккумулятор.