Единица измерения плотности электролита — Вместе мастерим
Измерение плотности электролита в сочетании с измерением напряжения под нагрузкой и без позволяет быстро установить причину неисправности в аккумуляторной батарее. При низкой плотности — это может быть дефект в какой-либо ячейке, глубокий разряд или обрыв цепи внутри АКБ. Плотность измеряется специальным прибором — ареометром (денсиметром).
В качестве электролита в аккумуляторных батареях применяют раствор серной кислоты, плотность которого измеряется в г/см3. В основном плотность зависит от концентрации раствора серной кислоты — чем больше концентрация раствора, тем больше плотность. Однако, она также зависит и от температуры раствора и от степени заряженности аккумулятора — при разрядке часть серной кислоты «уходит» в пластины, плотность снижается.
Поэтому измерение плотности принято проводить при 25 °С и полностью заряженном аккумуляторе.
Линейно снижаясь, по мере разряда АКБ, она составляет 1.20±0.01 г/см3 у батарей, степень заряженности которых снизилась до 50%. У полностью разряженной батареи плотность электролита составляет 1.10±0.01 г/см3.
Если значение плотности во всех банках аккумулятора одинаково (±0.01 г/см3), это говорит о степени заряженности батареи и отсутствии внутренних замыканий. При наличии внутреннего короткого замыкания плотность электролита в дефектной ячейке будет значительно ниже (на 0.10-0.15 г/см3), чем в остальных.
Низкая плотность в одной из ячеек указывает на наличие дефекта в ней (короткое замыкание между пластинами в блоке). Одинаково низкая плотность во всех ячейках связана с глубоким разрядом всей батареи, ее сульфатацией или устареванием.
Все заливаемые аккумуляторные батареи во время заряда и работы теряют часть воды.
Существует три основных вида аккумуляторных батарей:
Малосурьмянистые (Sb/Sb) — это обычная «классическая» свинцовая батарея с добавками в пластины сурьмы, они подвержены наибольшему саморазряду и выкипанию воды из раствора электролита, но не боятся глубоких разрядов, их легко зарядить даже при низкой плотности электролита.
Кальциевые (Ca/Ca) — пластины легированы кальцием, они практически не требуют слежения за уровнем и плотностью электролита, виброустойчивы, застрахованы от длительного перезаряда до 14.8 В, терпят перепады напряжения в бортовой сети, обладают коррозионной стойкостью, имеют низкий саморазряд, больший срок службы.
Такие батареи хорошо подходят тем, кто ездит много на большие расстояния, кому нужны виброустойчивые аккумуляторы, хорошо переносящие постоянные перезаряды в пути.

Гибридные (Sb/Ca) — являются золотой серединой. Они довольно стойки к глубоким разрядам, при этом значительно меньше подвержены выкипанию и саморазряду по сравнению с малосурьмянистыми.
На примере кальциевой батареи емкостью 60 А·ч, попробуем выяснить плотность электролита и ее исправность. Для начала, проверим напряжение на клеммах аккумулятора мультиметром, чтобы выяснить степень ее заряженности. Такая проверка проводится через 6-8 часов после выключения двигателя или отключения зарядного устройства. В нашем случае машина простояла около 4-х дней под сигнализацией — напряжение составляет 12 В, что говорит нам о том, что батарея почти полностью разряжена.
Теперь проверим выборочно плотность электролита в двух банках — она составляет 1.23 г/см3 при температуре окружающего воздуха 0°С, поэтому внесем поправку в показания ареометра, приведя их к 25°С: 1.23-0.02=1.21 г/см3 — это также говорит нам о том, что аккумулятор требует срочной подзарядки.
Снимаем аккумулятор и переносим в теплое помещение для подзарядки.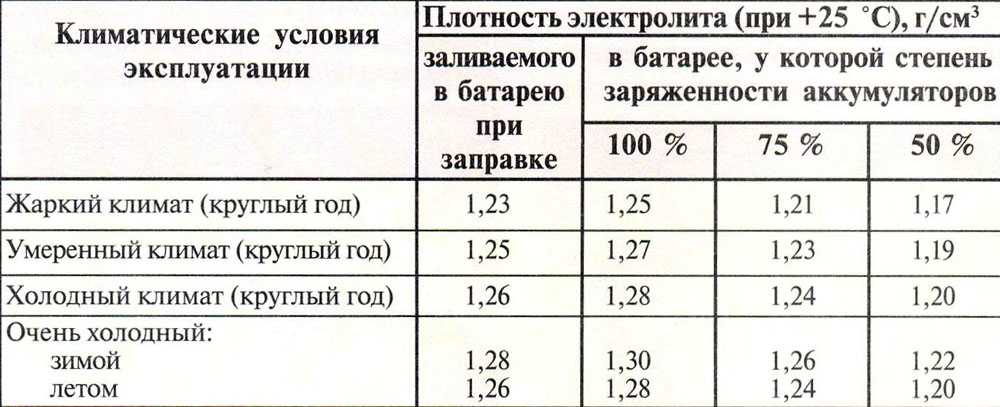
Для кальциевых батарей губительны старые «дедовские» методы зарядки, используемые для малосурмянистых АКБ с контрольно-тренировочным циклом заряда/разряда и «кипячением», а также малоэффективны некоторые автоматические зарядные устройства.
В наши дни в большинстве таких устройств используется комбинированный метод зарядки, когда в процессе зарядки сила тока снижается со временем, а напряжение, наоборот, повышается. Это объясняется тем, что ЭДС аккумуляторной батареи направлена именно на напряжение, соответственно при его повышении нужно повышать и напряжение. А вот сила тока уменьшается из-за все увеличивающегося сопротивления батареи.
Батарея считается полностью заряженной, когда ток и напряжение при заряде сохраняются без изменения в течение 1-2 часов.
 Ток должен упасть практически до нуля, а входящее напряжение может повысится до 16,5 В, в зависимости от устройства.
Ток должен упасть практически до нуля, а входящее напряжение может повысится до 16,5 В, в зависимости от устройства.Если вы часто заводите двигатель, двигаетесь на небольшие расстояния, и автомобиль долго простаивает без движения, то для такой батареи необходима ежемесячная плановая зарядка аккумулятора специализированным зарядным устройством, подходящим именно для кальциевых батарей.
После того, как электролит прогрелся до 20-25°С еще раз замерим напряжение и плотность. Теперь мультиметр показывает напряжение 12.45 В, а плотность в банках от 1.22 до 1.24 г/см3, что все равно указывает на недозаряд батареи.
Плотность электролита в аккумуляторе очень важный параметр у всех кислотных АКБ, и каждый автовладелец должен знать: какая плотность должна быть, как её проверить, а самое главное, как правильно поднять плотность аккумулятора (удельный вес кислоты) в каждой из банок со свинцовыми пластинами заполненных раствором h3SO4.
Проверка плотности – это один из пунктов процесса обслуживания аккумуляторной батареи, включающий так же проверку уровня электролита и замер напряжения АКБ.
По плотности электролита можно определить состояние батареи. Так что если батарея не держит заряд, то следует проверить состояние её жидкости в каждой его банке.
Плотность электролита влияет на емкость аккумулятора, и срок его службы.
Проверяется денсиметром (ареометр) при температуре +25°С. В случае, если температура отличается от требуемой, в показания вносятся поправки, как показано в таблице.
Итак, немного разобрались, что это такое, и что нужно регулярно делать проверку. А на какие цифры ориентироваться, сколько хорошо, а сколько плохо, какой должна быть плотность электролита аккумулятора?
Какая плотность должна быть в аккумуляторе
Выдерживать оптимальный показатель плотности электролита очень важно для аккумулятора и стоит знать, что необходимые значения зависят от климатической зоны.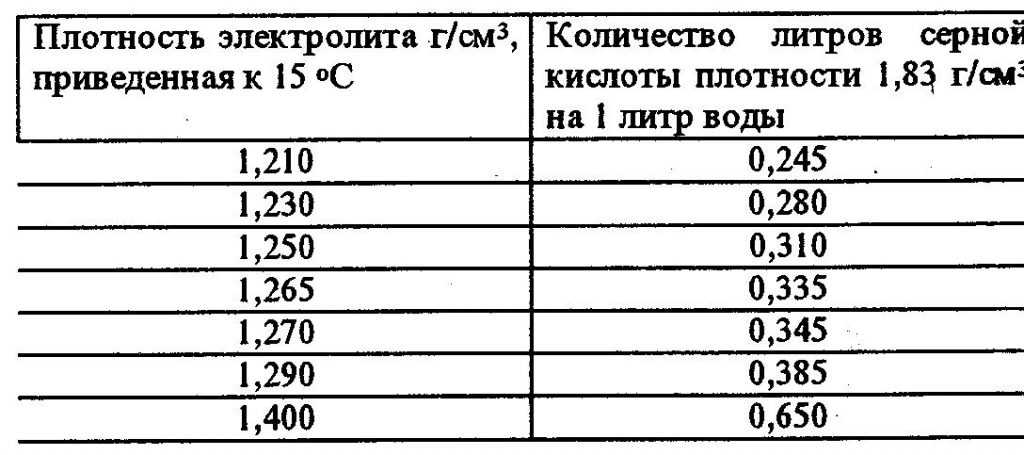 Поэтому плотность аккумулятора должна быть установлена исходя из совокупности требований и условий эксплуатации. К примеру, при умеренном климате плотность электролита должна находиться на уровне 1,25-1,27 г/см3 ±0,01 г/см3. В холодной зоне, с зимами до -30 градусов на 0,01 г/см3 больше, а в жаркой субтропической — на 0,01 г/см3 меньше. В тех регионах, где зима особо сурова (до -50 °С), дабы аккумулятор не замерз, приходится повышать плотность от 1,27 до 1,29 г/см3.
Поэтому плотность аккумулятора должна быть установлена исходя из совокупности требований и условий эксплуатации. К примеру, при умеренном климате плотность электролита должна находиться на уровне 1,25-1,27 г/см3 ±0,01 г/см3. В холодной зоне, с зимами до -30 градусов на 0,01 г/см3 больше, а в жаркой субтропической — на 0,01 г/см3 меньше. В тех регионах, где зима особо сурова (до -50 °С), дабы аккумулятор не замерз, приходится повышать плотность от 1,27 до 1,29 г/см3.
Много автовладельцев задаются вопросом: «Какой должна быть плотность электролита в аккумуляторе зимой, а какой летом, или же нет разницы, и круглый год показатели нужно держать на одном уровне?» Поэтому, разберемся с вопросом более подробно, а поможет это сделать, таблица плотности электролита в аккумуляторе с разделением на климатические зоны.
Также нужно помнить, что, как правило, аккумуляторная батарея, находясь на автомобиле, заряжена не более чем на 80-90 % её номинальной ёмкости, поэтому плотность электролита будет немного ниже, чем при полном заряде.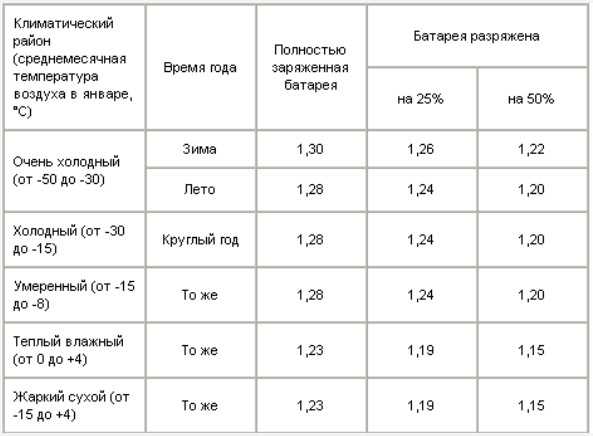 Так что, требуемое значение, выбирается чуть-чуть повыше, от того, которое указано в таблице плотности, дабы при снижении температуры воздуха до максимального уровня, АКБ гарантированно оставался работоспособным и не замерз в зимний период. Но, касаясь летнего сезона, повышенная плотность может и грозить закипанием.
Так что, требуемое значение, выбирается чуть-чуть повыше, от того, которое указано в таблице плотности, дабы при снижении температуры воздуха до максимального уровня, АКБ гарантированно оставался работоспособным и не замерз в зимний период. Но, касаясь летнего сезона, повышенная плотность может и грозить закипанием.
Таблица плотности электролита в аккумуляторе
Таблица плотности составляется относительно среднемесячной температуры в январе-месяце, так что климатические зоны с холодным воздухом до -30 °C и умеренные с температурой не ниже -15 не требуют понижения или повышения концентрации кислоты. Круглый год (зимой и летом) плотность электролита в аккумуляторе не стоит изменять, а лишь проверять и следить, чтобы она не отклонялась от номинального значения, а вот в очень холодных зонах, где столбик термометра часто на отметке ниже -30 градусов (в плоть до -50), корректировка допускается.
Плотность электролита в аккумуляторе зимой
Плотность электролита в аккумуляторе зимой должна составлять 1,27 (для регионов с зимней температурой ниже -35 не менее 1. 28 г/см3). Если будет значение ниже, то это приводит к снижению электродвижущей силы и трудного запуска двигателя в морозы, вплоть до замерзания электролита.
28 г/см3). Если будет значение ниже, то это приводит к снижению электродвижущей силы и трудного запуска двигателя в морозы, вплоть до замерзания электролита.
Когда в зимнее время плотность в аккумуляторной батареи понижена, то не стоит сразу бежать за корректирующим раствором дабы её поднять, гораздо лучше позаботится о другом – качественном заряде АКБ при помощи зарядного устройства.
Получасовые поездки от дому к работе и обратно не позволяют электролиту прогрется, и, следовательно, хорошо зарядится, ведь аккумулятор принимает заряд лишь после прогрева. Так что разряженность изо дня в день увеличивается, и в результате падает и плотность.
Для новой и исправной АКБ нормальный интервал изменения плотности электролита (полный разряд – полный заряд) составляет 0,15-0,16 г/см3.
Помните, что эксплуатация разряженного аккумулятора при минусовой температуре приводит к замерзанию электролита и разрушению свинцовых пластин!
По таблице зависимости температуры замерзания электролита от его плотности, можно узнать минусовой порог столбика термометра, при котором образовывается лед в вашем аккумуляторе.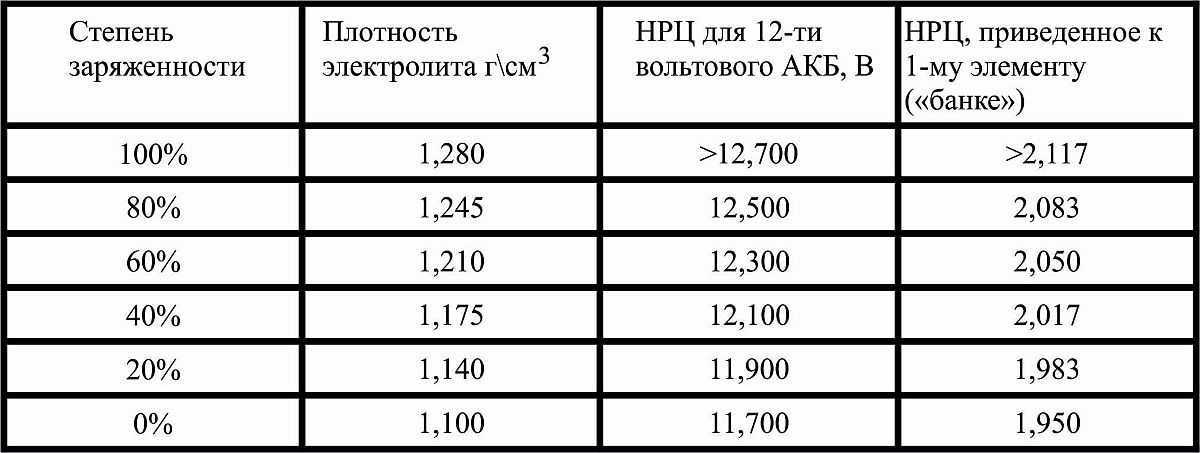
Как видите, при заряженности на 100% аккумуляторная батарея замерзнет при -70 °С. При 40% заряде замерзает уже при -25 °С. 10% не только не дадут возможности запустить двигатель в морозный день, но и напрочь замерзнет в 10 градусный мороз.
Когда плотность электролита не известна, то степень разряженности батареи проверяют нагрузочной вилкой. Разность напряжения в элементах одной батареи не должна превышать 0,2В.
Показания вольтметра нагрузочной вилки, B
Степень разряженности батареи, %
Если АКБ разрядилась более чем на 50% зимой и более чем на 25% летом, её необходимо подзарядить.
Плотность электролита в аккумуляторе летом
Летом аккумулятор страдает от обезвоживания, поэтому учитывая то, что повышенная плотность плохо влияет на свинцовые пластины, лучше если она будет на 0,02 г/см3 ниже требуемого значения (особенно касается южных регионов).
В летнее время температура под капотом, где зачастую находится аккумулятор, значительно повышена. Такие условия способствуют испарению воды из кислоты и активности протекания электрохимических процессов в АКБ, обеспечивая высокую токоотдачу даже при минимально допустимом значении плотности электролита (1,22 г/см3 для теплой влажной климатической зоны). Так что, когда уровень электролита постепенно падает, то повышается его плотность, что ускоряет процессы коррозионного разрушения электродов. Именно поэтому так важно контролировать уровень жидкости в аккумуляторной батарее и при его понижении добавить дистиллированной воды, а если этого не сделать, то грозит перезаряд и сульфация.
Такие условия способствуют испарению воды из кислоты и активности протекания электрохимических процессов в АКБ, обеспечивая высокую токоотдачу даже при минимально допустимом значении плотности электролита (1,22 г/см3 для теплой влажной климатической зоны). Так что, когда уровень электролита постепенно падает, то повышается его плотность, что ускоряет процессы коррозионного разрушения электродов. Именно поэтому так важно контролировать уровень жидкости в аккумуляторной батарее и при его понижении добавить дистиллированной воды, а если этого не сделать, то грозит перезаряд и сульфация.
Если аккумулятор разрядился по невнимательности водителя или другим причинам, следует попробовать вернуть ему его рабочее состояние при помощи зарядного устройства. Но перед тем как заряжать АКБ, смотрят на уровень и по надобности доливают дистиллированную воду, которая могла испариться в процессе работы.
Через некоторое время плотность электролита в аккумуляторе, из-за постоянного разбавления его дистиллятом, снижается, и опускается ниже требуемого значения. Тогда эксплуатация батареи становится невозможной, так что возникает необходимость повысить плотность электролита в аккумуляторе. Но для того, чтобы узнать насколько повышать, нужно знать как проверять эту самую плотность.
Тогда эксплуатация батареи становится невозможной, так что возникает необходимость повысить плотность электролита в аккумуляторе. Но для того, чтобы узнать насколько повышать, нужно знать как проверять эту самую плотность.
Как проверить плотность аккумулятора
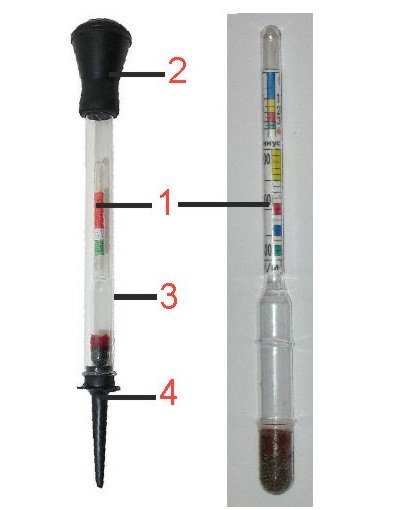
Дабы обеспечить правильную работу аккумуляторной батареи, плотность электролита следует проверять каждые 15-20 тыс. км пробега. Измерение плотности в аккумуляторе осуществляется при помощи такого прибора как денсиметр. Устройство этого прибора состоит из стеклянной трубки, внутри которой ареометр, а на концах — резиновый наконечник с одной стороны и груша с другой. Чтобы произвести проверку, нужно будет: открыть пробку банки аккумулятора, погрузить его в раствор, и грушей втянуть небольшое количество электролита. Плавающий ареометр со шкалой покажет всю необходимую информацию. Более детально как правильно проверить плотность аккумулятора рассмотрим чуть ниже, поскольку есть еще такой вид АКБ, как необслуживаемые, и в них процедура несколько отличается — вам не понадобится абсолютно никаких приборов.
Индикатор плотности на необслуживаемой АКБ
Плотность необслуживаемого аккумулятора отображается цветовым индикатором в специальном окошке. Зеленый индикатор свидетельствует, что все в норме (степень заряженности в пределах 65 — 100%), если плотность упала и требуется подзарядка, то индикатор будет черный. Когда в окошке отображается белая или красная лампочка, то нужен срочный долив дистиллированной воды. Но, впрочем, точная информация о значении того или иного цвета в окошке, находится на наклейке аккумуляторной батареи.
Теперь продолжаем далее разбираться, как проверять плотность электролита обычного кислотного аккумулятора в домашних условия.
Проверка плотности электролита в аккумуляторе
Итак, чтобы можно было правильно проверить плотность электролита в аккумуляторной батарее, первым делом проверяем уровень и при необходимости его корректируем. Затем заряжаем аккум и только тогда приступаем к проверке, но не сразу, а после пары часов покоя, поскольку сразу после зарядки или долива воды будут недостоверные данные.
Следует помнить, что плотность напрямую зависит от температуры воздуха, поэтому сверяйтесь с таблицей поправок, рассматриваемой выше. Сделав забор жидкости из банки аккумулятора, держите прибор на уровне глаз – ареометр должен находиться в состоянии покоя, плавать в жидкости, не касаясь стенок. Замер производится в каждом отсеке, а все показатели записываются.
Таблица определения заряженности аккумулятора по плотности электролита.
Аккумуляторная батарея – один из основных элементов автомобиля, отвечающих за пуск двигателя. Значение аккумулятора сложно переоценить, ведь без него невозможно завести мотор, а, значит, машина своим ходом передвигаться не сможет. Именно поэтому АКБ требует к себе особого внимания, исключающего возникновение неприятных ситуаций в виде невозможности совершить запланированную поездку. При этом стоит отметить, что для поддержания работоспособности это важного источника питания не требуется предпринимать каких-то сверхусилий, а достаточно выполнять лишь небольшой комплекс профилактических мер.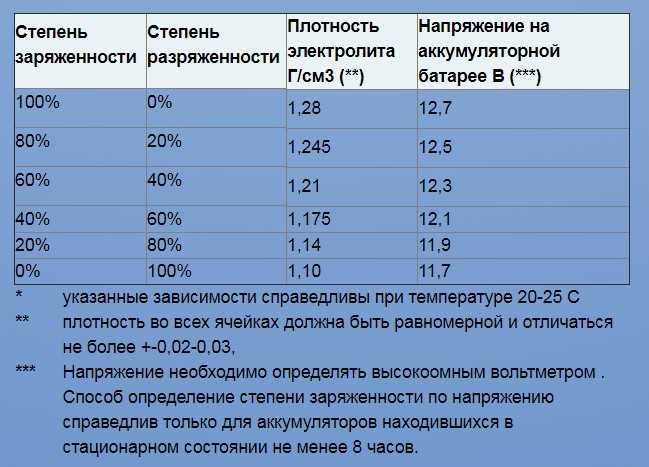
Свинцовая аккумуляторная батарея представляет собой гальванический элемент, внутри которого химическая энергия в результате протекающих реакций преобразуется в электрическую. Этот процесс невозможен без электролита – раствора кислоты, обеспечивающего движение заряженных частиц между погруженными в него электродами. Как правило, электролит представляет собой водный раствор серной кислоты определенной плотности. Именно такой параметр как плотность электролита оказывает значительное влияние на работоспособность аккумулятора, поэтому периодически его нужно контролировать.
Измерение плотности электролита в аккумуляторе
Измерить плотность залитого в свинцовый аккумулятор электролита не так уж сложно, однако есть определенные нюансы, связанные с особенностями устройства и принципом работы АКБ. Перечислим некоторые важные моменты, которые надо учесть:
- Осуществить процедуру измерения плотности получится только в случае с так называемым обслуживаемым аккумулятором, который предоставляет доступ к банкам (секциям) с электролитом посредством закрытых крышками заливных отверстий.
 Как раз через эти отверстия (обычно их число равно шести, как и количество секций) и осуществляется забор состава для замера плотности.
Как раз через эти отверстия (обычно их число равно шести, как и количество секций) и осуществляется забор состава для замера плотности. - В процессе своей работы автомобильная аккумуляторная батарея постоянно заряжается и разряжается. Разряд происходит при прокручивании стартера, а заряд – при уже заведенном двигателе от генератора. В зависимости от степени заряженности меняется и плотность электролита. Значения могут колебаться в пределах 0.15-0.16 г/см 3 . Важно отметить, что автомобильный генератор не способен полностью зарядить аккумуляторную батарею. При штатной работе на машине потенциал АКБ используется только на 80-90%. Полный заряд может обеспечить только внешнее зарядное устройство, к которому обязательно придется прибегнуть перед осуществлением замера плотности электролита.
- Плотность электролита зависит от его температуры. Обычно замер производится при температуре +25 °С, в противном случае делаются поправки.
Допустим, все вышеперечисленные условия приняты во внимание, и есть возможность приступить непосредственно к замеру плотности. Для этого понадобится специальный прибор – денсиметр, который состоит из ареометра, резиновой груши и стеклянной трубки с наконечником. Прибор вводится в банку аккумулятора через заливное отверстие, а затем осуществляется засасывание электролита с помощью резиновой груши. Оно происходит до тех пор, пока ареометр не всплывет. Показания считываются после того, как прекратятся колебания ареометра и появится возможность определения точного значения. Отсчет показаний производится по шкале, при этом взгляд должен находиться на уровне поверхности жидкости.
Для этого понадобится специальный прибор – денсиметр, который состоит из ареометра, резиновой груши и стеклянной трубки с наконечником. Прибор вводится в банку аккумулятора через заливное отверстие, а затем осуществляется засасывание электролита с помощью резиновой груши. Оно происходит до тех пор, пока ареометр не всплывет. Показания считываются после того, как прекратятся колебания ареометра и появится возможность определения точного значения. Отсчет показаний производится по шкале, при этом взгляд должен находиться на уровне поверхности жидкости.
Полученное значение должно входить в диапазон 1.25-1.27 г/см 3 , если автомобиль эксплуатируется в средней полосе. В холодной климатической зоне (средняя месячная температура января ниже -15 °С) показатель должен находиться в интервале 1.27-1.29 г/см 3 . Проверять плотность электролита на соответствие этим числам нужно в каждой из шести банок аккумулятора. Показания не должны отличаться более чем на 0.01 г/см 3 , иначе потребуется их корректировка.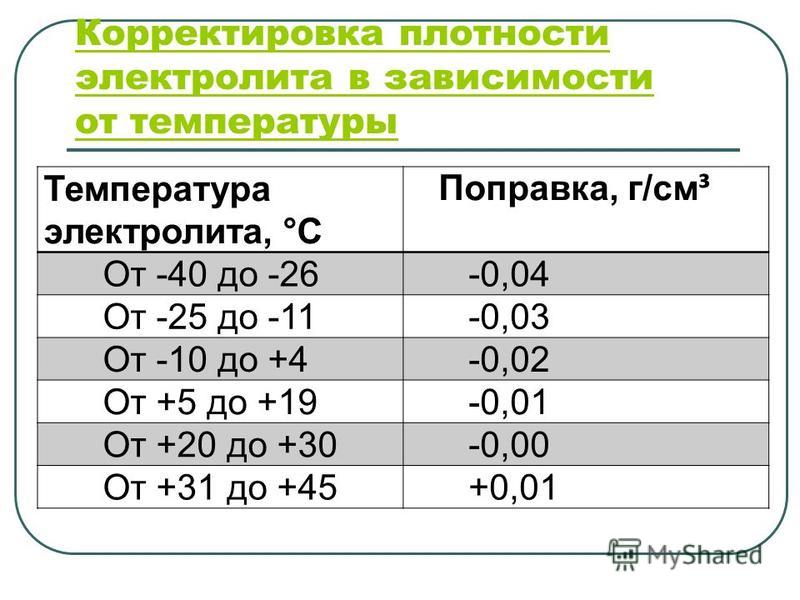
Как мы уже говорили, плотность электролита изменяется в зависимости от температуры. Это значит, что зимой и летом жидкость в одном и том же полностью исправном аккумуляторе будет иметь разную плотность. О том, насколько будут разниться показания, дает представление приведенная ниже таблица.
| Температура электролита, °С | Поправка к показанию денсиметра, г/см 3 | Температура электролита, °С | Поправка к показанию денсиметра, г/см 3 |
|---|---|---|---|
| -55…-41 | -0.05 | +5…+19 | -0.01 |
| -40…-26 | -0.04 | +20…+30 | |
| -25…-11 | -0.03 | +31…+45 | +0.01 |
| -10…+4 | -0.02 | +46…+60 | +0.02 |
Зависимость температуры замерзания электролита от его плотности демонстрирует еще одна таблица. На основе этих данных можно установить оптимальную плотность электролита для конкретных климатических условий. Нижняя граница подобранного интервала должна гарантировать, что электролит не замерзнет даже при самых сильных холодах и обеспечит требуемое для прокручивания стартера усилие. В то же время чрезмерно завышать плотность тоже нельзя, так как на положительных электродах аккумулятора начинают ускоряться коррозионные процессы, приводящие к сульфатации пластин.
Нижняя граница подобранного интервала должна гарантировать, что электролит не замерзнет даже при самых сильных холодах и обеспечит требуемое для прокручивания стартера усилие. В то же время чрезмерно завышать плотность тоже нельзя, так как на положительных электродах аккумулятора начинают ускоряться коррозионные процессы, приводящие к сульфатации пластин.
| Плотность электролита при 25 °С, г/см 3 | Температура замерзания, °С | Плотность электролита при 25 °С, г/см 3 | Температура замерзания, °С |
|---|---|---|---|
| 1.09 | -7 | 1.22 | -40 |
| 1.10 | -8 | 1.23 | -42 |
| 1.11 | -9 | 1.24 | -50 |
| 1.12 | -10 | 1.25 | -54 |
| 1.13 | -12 | 1.26 | -58 |
| 1.14 | -14 | 1.27 | -68 |
| 1.15 | -16 | 1.28 | -74 |
1. 16 16 | -18 | 1.29 | -68 |
| 1.17 | -20 | 1.30 | -66 |
| 1.18 | -22 | 1.31 | -64 |
| 1.19 | -25 | 1.32 | -57 |
| 1.20 | -28 | 1.33 | -54 |
| 1.21 | -34 | 1.40 | -37 |
Причины изменения плотности электролита
Зафиксированные в результате измерения плотности значения не всегда соответствуют требуемым показателям. Расхождения могут касаться как отдельных банок аккумулятора, так и всех вместе. Если плотность завышена, то нужно обратить в первую очередь внимание на уровень электролита. Низкий уровень в большинстве случае является последствием электролиза, приводящего к разложению входящей в состав электролита воды на водород и кислород. Этот процесс выражается в появлении на поверхности жидкости пузырьков, что обычно происходит при зарядке аккумулятора. Частое «кипение» может приводить к снижению концентрации воды, и этот вопрос решается ее простым добавлением. Доливать в аккумулятор стоит только дистиллированную воду, контролируя при этом уровень электролита. Подробнее о корректировке плотности электролита поговорим ниже.
Доливать в аккумулятор стоит только дистиллированную воду, контролируя при этом уровень электролита. Подробнее о корректировке плотности электролита поговорим ниже.
Если с повышенной плотностью все ясно, то с пониженной ситуация несколько сложнее. В теории, одной из причин понижения плотности, может быть то, что по какой-то причине в электролите уменьшилась доля серной кислоты. Однако на практике это маловероятно, так как сама по себе она обладает высокой температурой кипения, исключающей испарение даже при интенсивном нагреве, который происходит, например, при зарядке аккумуляторной батареи. Более распространенной причиной снижения плотности электролита является так называемая сульфатация пластин, заключающаяся в образовании на электродах сульфата свинца (PbSO4). На самом деле, это естественный процесс, происходящий при каждом разряде АКБ. Но дело в том, что при нормальном режиме работы после разряда аккумулятора обязательно происходит его заряд (на автомобиле аккумулятор постоянно подзаряжается от генератора). Заряд сопровождается обратным преобразованием сульфата свинца в свинец (на катоде) и двуокись свинца (на аноде) – в те активные вещества, которые составляют основу электродов и непосредственно участвуют в химическом процессе внутри аккумуляторной батареи. Если АКБ находится длительное время в разряженном состоянии, сульфат свинца кристаллизуется, безвозвратно теряя способность участвовать в химических реакциях. Это очень неприятный процесс, в результате которого аккумулятор уже не получится зарядить полностью даже при использовании внешнего зарядного устройства ввиду того, что не вся площадь пластин задействована в работе. Так как аккумулятор не заряжается до конца, то и плотность электролита не восстанавливается до своих исходных значений. По сути, здесь уже идет разговор об устранении нарушений в нормальном функционировании аккумулятора.
Заряд сопровождается обратным преобразованием сульфата свинца в свинец (на катоде) и двуокись свинца (на аноде) – в те активные вещества, которые составляют основу электродов и непосредственно участвуют в химическом процессе внутри аккумуляторной батареи. Если АКБ находится длительное время в разряженном состоянии, сульфат свинца кристаллизуется, безвозвратно теряя способность участвовать в химических реакциях. Это очень неприятный процесс, в результате которого аккумулятор уже не получится зарядить полностью даже при использовании внешнего зарядного устройства ввиду того, что не вся площадь пластин задействована в работе. Так как аккумулятор не заряжается до конца, то и плотность электролита не восстанавливается до своих исходных значений. По сути, здесь уже идет разговор об устранении нарушений в нормальном функционировании аккумулятора.
Частичную сульфатацию пластин можно устранить с помощью контрольно-тренировочных циклов, заключающихся в заряде и последующем разряде батареи до определенного уровня. Большинство современных зарядных устройств имеют такую функцию, поэтому имеет смысл ей воспользоваться, особенно если аккумулятор по какой-то причине долго находился в разряженном состоянии. Процедура десульфатации весьма длительная и может занять до нескольких дней. Если она не принесла результата, то крайней мерой является увеличение плотности с помощью добавления корректирующего электролита (плотность около 1.40 г/см 3 ). Такой способ можно рассматривать только как временное решение проблемы, потому что причина как таковая не устраняется.
Большинство современных зарядных устройств имеют такую функцию, поэтому имеет смысл ей воспользоваться, особенно если аккумулятор по какой-то причине долго находился в разряженном состоянии. Процедура десульфатации весьма длительная и может занять до нескольких дней. Если она не принесла результата, то крайней мерой является увеличение плотности с помощью добавления корректирующего электролита (плотность около 1.40 г/см 3 ). Такой способ можно рассматривать только как временное решение проблемы, потому что причина как таковая не устраняется.
Как поднять плотность электролита
Понизить или повысить плотность электролита в аккумуляторе можно путем откачивания его определенного количества, и долива взамен дистиллированной воды или электролита с повышенной плотностью (корректирующего). Данная процедура требует больших временных затрат, так как цикл откачки-долива может повторяться несколько раз, пока не будет достигнуто требуемое значение. После каждой корректировки необходимо поставить аккумулятор на зарядку (минимум на 30 минут), а затем дать ему постоять (0. 5-2 часа). Эти действия необходимы для лучшего перемешивания электролита и выравнивания плотности в банках.
5-2 часа). Эти действия необходимы для лучшего перемешивания электролита и выравнивания плотности в банках.
В процессе поднятия (или понижения) плотности электролита не стоит забывать и о контроле его уровня. Он осуществляется стеклянной трубкой с двумя отверстиями по краям. Один край погружается в электролит до тех пор, пока не упрется в предохранительную сетку. Далее верхний конец закрывается пальцем, а сама трубка осторожно поднимается вместе со столбиком жидкости внутри. Высота этого столбика указывает на расстояние от верхней кромки пластин до поверхности залитого электролита. Оно должно составлять 10-15 мм. Если аккумулятор имеет индикатор (тубус) или прозрачный корпус с нанесенными метками минимума и максимума, то контролировать уровень значительно проще.
Не стоит забывать, что все операции с электролитом необходимо выполнять осторожно, используя защитные перчатки и очки.
Страница не найдена — Вместе мастерим
- Контакты
Содержание1 Топ-5 блендеров для смузи1. 1 Ninja BL7701.2 NutriBullet Pro NB9-1301 – Самый удобный миксер для смузи1.3 Vitamix Pro 7501.4 Oster Pro 1200 – Лучшая классика1.5 Blendtec Classic 575 – лучший автоматизированный Блендеры — это универсальные кухонные приборы, которые могут измельчать ингредиенты для соуса сальса и превращать овощи в пюре для супов. Одной из задач, которую люди …
1 Ninja BL7701.2 NutriBullet Pro NB9-1301 – Самый удобный миксер для смузи1.3 Vitamix Pro 7501.4 Oster Pro 1200 – Лучшая классика1.5 Blendtec Classic 575 – лучший автоматизированный Блендеры — это универсальные кухонные приборы, которые могут измельчать ингредиенты для соуса сальса и превращать овощи в пюре для супов. Одной из задач, которую люди …
Читать далее
Содержание1 Wahl Lithium-Ion+ – самый дешевый триммер2 Remington MB4700 Smart – самый гибкий3 Wahl Aqua Blade Rechargeable – лучшая водостойкость4 Braun Beard BT7240 – самый портативный5 Panasonic ER-GB42-K – лучшее для начинающих Формирование привлекательной бороды требует времени, терпения и, конечно же, хорошего триммера. Триммеры оснащены функцией регулировки длины, которая позволяет установить нужную длину. Помимо того, …
Читать далее
Содержание1 Miele AutoDos G7566 – В целом лучший2 Bosch 300 Series – Самая прочная3 Frigidaire Gallery 24 – Лучшее соотношение4 KitchenAid KDPM604KPS – Лучший дизайн5 LG Smart QuadWash и TrueSteam – Лучшая умная посудомоечная машина Приобретение высококачественной посудомоечной машины — это достойная инвестиция, которую необходимо рассмотреть для своего дома. Это не только избавит от хлопот и времени, которое вы …
Это не только избавит от хлопот и времени, которое вы …
Читать далее
Содержание1 Факторы, которые следует учитывать перед покупкой фритюрницы2 Различные модели аэрогрилей и их характеристики2.1 Фритюрница Instant Vortex 4 в 12.2 Фритюрница Ninja2.3 Фритюрница COSORI Max XL2.4 Электрическая фритюрница GoWISE USA 5,8 Quarts 8-in-1 XL2.5 Компактная фритюрница Dash3.6 Gourmia 6 Quart Digital Air Fryer2.7 Аэрогриль Cuisinart TOA-602.8 Фритюрница с 2 корзинами и технологией DualZone Ninja Foodi …
Читать далее
Содержание1 Как выбрать хороший накопительный водонагреватель?1.1 Мощность1.2 Объём резервуара1.3 Материал бака1.4 Антикоррозийный анод2 Топ 5 лучших накопительных электрических водонагревателей2.1 Timberk SWH FSK7 30 V на 30 л — водонагреватель бюджетный и экономичный2.2 Ballu BWH/S 50 Smart WiFi на 50 л — водонагреватель с управлением со смартфона2. 3 Electrolux EWH 80 Centurio IQ 2.0 Silver на 80 …
3 Electrolux EWH 80 Centurio IQ 2.0 Silver на 80 …
Читать далее
Содержание1 Какую рожковую кофеварку лучше выбрать?2 Лучшие рожковые кофеварки с автоматическим капучинатором2.1 Polaris PCM 1536E Adore Cappuccino2.2 Kitfort КТ-7432.3 VITEK VT-15143 Лучшие рожковые кофеварки с ручным капучинатором 2022 года3.1 De’Longhi ECP 33.213.2 VITEK VT-15193.3 Dauken HC1204 Лучшие рожковые кофеварки 3 в 14.1 Ariete Moderna 13184.2 Jura E804.3 Gaggia Classic5 Лучшие недорогие рожковые кофеварки в 2022 …
Читать далее
Содержание1 Критерии выбора проточного электрического водонагревателя1.1 Тип устройства1.2 Мощность1.3 Управление нагревом2 Лучшие недорогие проточные электрические водонагреватели2.1 Atmor Platinum Tri 52.2 Thermex Surf 35002.3 Timberk WHEL-6 OSC2.4 Hyundai H – IWR1-3P-UIO57/S2.5 Electrolux Smartfix 2.0 5.5 TS3 Лучшие проточные электрические водонагреватели (премиум)3. 1 Stiebel Eltron DHC 63.2 Electrolux NPX 8 Flow Active3.3 Stiebel Eltron DHC 83.4 Electrolux NPX …
1 Stiebel Eltron DHC 63.2 Electrolux NPX 8 Flow Active3.3 Stiebel Eltron DHC 83.4 Electrolux NPX …
Читать далее
Содержание1 Критерии выбора1.1 Батарея1.2 Размер1.3 Мощность1.4 Функциональные возможности2 Рейтинг, плюсы и минусы2.1 Xiaomi Mi Robot Vacuum-Mop Essential2.2 Xiaomi Dreame F92.3 Xiaomi MiJia Sweeping Robot G12.4 Xiaomi Dreame D92.5 Roborock S5 MAX (RU)2.6 Xiaomi EVE Plus2.7 Kitfort KT-5322.8 Roborock E4 (RU)2.9 Roborock S6 MaxV (RU)2.10 Ecovacs DeeBot OZMO 9003 Так какой же выбрать? Роботы пылесосы являются …
Читать далее
Содержание1 Популярные модели и отзывы1.1 Gorenje WE 62S3 R – высокий класс энергопотребления и эффективная работоспособность.1.2 Gorenje Color W 65Z03R/S – большой выбор программ.1.3 Samsung WD1142XVR – вместительность и сушка1.4 Schaub Lorenz SLW MG5131 – стиль1.5 Стиральная машина ARTEL TE 452 Выводы В 2022 году процент покупок стиральных машин значительно увеличился. Производственные компании выяснили что …
Производственные компании выяснили что …
Читать далее
Содержание1 Виды электрических зубных щеток: плюсы и минусы1.1 Звуковые электрические зубные щетки1.2 Ротационные электрические зубные щетки1.3 Ультразвуковые зубные щетки1.4 3D-чистка2 Какая форма насадок бывает3 Какие батарейки и аккумуляторы ставят в щётки4 Классические электрические щётки: ТОП-3 лучших моделей4.1 1 место: Oral-B PRO 70004.2 2 место: Oral-B PRO 5004.3 3 место: Oral-B Vitality 3D White 3D White5 …
Читать далее
Экспериментальные измерения и моделирование вязкости и плотности тройных растворов хлоридов кальция и калия
1. Руис-Лламас А., Масиас-Салинас Р. Моделирование динамической вязкости ионных растворов. Инд.Инж. хим. Рез. 2015;54:7169–7179. doi: 10.1021/acs.iecr.5b01664. [CrossRef] [Google Scholar]
2. Магомедов Ю.Б., Алхасов А.Б. Динамическая вязкость водных растворов солей при высоких температурах, давлениях и концентрациях. Дж. Инж. физ. Термофиз. 2007; 80: 1216–1222. дои: 10.1007/s10891-007-0157-й. [CrossRef] [Google Scholar]
Дж. Инж. физ. Термофиз. 2007; 80: 1216–1222. дои: 10.1007/s10891-007-0157-й. [CrossRef] [Google Scholar]
3. Qiblawey H, Abu Jdayil B. Вязкость и плотность тройного раствора хлорида магния + хлорид натрия + вода от (293,15 до 318,15 K) J. Chem. англ. Данные. 2010;55:3322–3326. дои: 10.1021/je100111w. [CrossRef] [Google Scholar]
4. Васкес-Кастильоа Г., Иглесиас-Сильва Г.В., Холл К.Р. Расширение модели Макаллистера для корреляции кинематической вязкости растворов электролитов. Равновесие жидкой фазы. 2013; 58:44–49. doi: 10.1016/j.fluid.2013.07.052. [Перекрестная ссылка] [Академия Google]
5. Голдсак Д., Франкетто Р. Вязкость концентрированных растворов электролитов I. Концентрационная зависимость при фиксированной температуре. Можно. Дж. Хим. 1977; 55: 1062–1072. дои: 10.1139/v77-148. [CrossRef] [Google Scholar]
6. Majali F, Ettouney H, Abdel-Jabbar N, Qiblawey H. Конструкция и эксплуатационные характеристики установок обратного осмоса пилотного масштаба. Опреснение. 2008; 222:441–450. doi: 10.1016/j.desal.2007.01.169. [CrossRef] [Google Scholar]
Опреснение. 2008; 222:441–450. doi: 10.1016/j.desal.2007.01.169. [CrossRef] [Google Scholar]
7. Qiblawey H, Banat F, Al-Nasser Q. Лабораторная установка для очистки воды с использованием бытовой установки обратного осмоса с фотоэлектрическим приводом. Десалин. Водное лечение. 2009 г.;7:53–59. doi: 10.5004/dwt.2009.695. [CrossRef] [Google Scholar]
8. Панагопулос А., Хараламбус К.Дж., Лоизиду М. Методы утилизации рассола и технологии очистки опреснения — обзор. науч. Общая окружающая среда. 2019;693:133545. doi: 10.1016/j.scitotenv.2019.07.351. [PubMed] [CrossRef] [Google Scholar]
9. Menon AK, Haechler I, Kaur S, et al. Усиленное солнечное испарение с использованием фототермического зонта для управления сточными водами. Нац. Поддерживать. 2020;3:144–151. doi: 10.1038/s41893-019-0445-5. [CrossRef] [Google Scholar]
10. Mohameed H, Ulrich J. Влияние значения pH на скорость роста и растворения хлорида калия. Кристалл. Рез. Технол. 1996; 31: 27–31. doi: 10. 1002/crat.2170310107. [CrossRef] [Google Scholar]
1002/crat.2170310107. [CrossRef] [Google Scholar]
11. Mohameed H, Abdel-Jabbar N, Takrouri K, Nasr A. Оптимальная стратегия охлаждения на основе моделей для периодических процессов кристаллизации. хим. англ. Рез. Дес. 2003; 81: 578–584. doi: 10.1205/026387603765444528. [CrossRef] [Google Scholar]
12. Ахмад Н., Баддур Р. Обзор источников, эффектов, методов утилизации и правил попадания рассола в морскую среду. Океанское побережье. Управление 2014;87:1–7. doi: 10.1016/j.ocecoaman.2013.10.020. [Перекрестная ссылка] [Академия Google]
13. Эрреро-Гонсалес М., Ной Адмон Н., Домингес-Рамос А., Ибаньес Р., Вольфсон А., Ирабиен А. Оценка экологической устойчивости валоризации рассола методом обратного осмоса морской воды с помощью электродиализа с биполярными мембранами. Окружающая среда. науч. Загрязн. Рез. 2020;27:1256–1266. doi: 10.1007/s11356-019-04788-w. [PubMed] [CrossRef] [Google Scholar]
14. Pollyea R, Chapman M, Jayne R, Hao WuH. Сброс сточных вод с нефтяных месторождений с высокой плотностью вызывает более глубокие, сильные и продолжительные землетрясения. Нац. коммун. 2019;10:3077. doi: 10.1038/s41467-019-11029-8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Нац. коммун. 2019;10:3077. doi: 10.1038/s41467-019-11029-8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Kim B, et al. Очистка высокоминерализованных солевых растворов многоступенчатым ионно-концентрационным поляризационным опреснением. науч. Отчет 2016; 6: 31850. doi: 10.1038/srep31850. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
16. Джованни Г., Пабло С. Эффекты кинетической вязкости растворителя как зонды для изучения механизмов действия ферментов. Биохимия. 2018;57:3445–3453. doi: 10.1021/acs.biochem.8b00232. [PubMed] [CrossRef] [Академия Google]
17. Huitian J, Walid E, Aboudheir A, Mahinpey N. Плотность, вязкость, показатель преломления и электропроводность деградированных растворов моноэтаноламина при стандартных температурах. Дж. Хим. англ. Данные. 2018; 63:1969–1976. doi: 10.1021/acs.jced.7b01101. [CrossRef] [Google Scholar]
18. Qiblawey H, Arshad MH, Easa A, Atilhan M. Вязкость и плотность тройного раствора хлорида кальция + хлорид натрия + вода от T = (293,15 до 323,15) K. J. Chem. англ. Данные. 2014;59:2133–2143. doi: 10.1021/je500070k. [Перекрестная ссылка] [Академия Google]
J. Chem. англ. Данные. 2014;59:2133–2143. doi: 10.1021/je500070k. [Перекрестная ссылка] [Академия Google]
19. Чжан Х.Л., Чен Г.Х., Хань С.Дж. Вязкость и плотность H 2 O + NaCl + CaCl 2 и H 2 O + KCl + CaCl 2 при 298,15 К. J. Chem. англ. Данные. 1997; 42: 526–530. doi: 10.1021/je9602733. [CrossRef] [Google Scholar]
20. Out DJP, Los JM. Вязкость водного раствора одновалентных электролитов от 5 до 95 °С. Дж. Солют. хим. 1980; 9:19–35. doi: 10.1007/BF00650134. [CrossRef] [Google Scholar]
21. Цзян Дж., Стэнли И.С. Новая модель вязкости растворов электролитов. Инд.Инж. хим. Рез. 2003;42:6267–6272. doi: 10.1021/ie0210659. [CrossRef] [Google Scholar]
22. Кестин Дж., Шенкленд И.Р., Пол Р. Вязкость водных растворов KCl в диапазоне температур 25–200 и диапазоне давлений 0,1–30 МПа. Междунар. Дж. Термофиз. 1981;2(4):301–314. doi: 10.1007/BF00498761. [CrossRef] [Google Scholar]
23. Каминский М. Концентрация и температурная зависимость вязкости водных растворов сильных электролитов. III. KCl, K 2 SO 4 , MgCl 2 , BeSO 4 и MgSO 4 растворы. З. Физ. хим. 1957; 12: 206–231. doi: 10.1524/зпч.1957.12.3_4.206. [CrossRef] [Google Scholar]
III. KCl, K 2 SO 4 , MgCl 2 , BeSO 4 и MgSO 4 растворы. З. Физ. хим. 1957; 12: 206–231. doi: 10.1524/зпч.1957.12.3_4.206. [CrossRef] [Google Scholar]
24. Маркус Ю. Влияние ионов на структуру воды: создание и разрушение структуры. хим. 2009; 109:1346–1370. doi: 10.1021/cr8003828. [PubMed] [CrossRef] [Google Scholar]
25. Leyendekkers JV. Вязкость водных растворов электролитов и модель ТТГ. Дж. Солют. хим. 1979;8(12):853–859. doi: 10.1007/BF00644882. [Перекрестная ссылка] [Академия Google]
26. Goldsack DE, Franchetto RC. Вязкость концентрированных растворов электролитов. II. Температурная зависимость. Можно. Дж. Хим. 1978; 56: 1442–1450. дои: 10.1139/v78-236. [CrossRef] [Google Scholar]
27. Zafarani-Moattar MT, Majdan-Cegincara RM. Моделирование и прогнозирование вязкости водных смешанных растворов электролитов. Инд.Инж. хим. Рез. 2009; 48: 5833–5844. doi: 10.1021/ie801933u. [CrossRef] [Google Scholar]
28. Hu Y, Zhang X, Jin C, Peng X. Теория полуидеального решения. 3. Расширение вязкости многокомпонентных водных растворов. Дж. Солют. хим. 2010;39: 1828–1844. doi: 10.1007/s10953-010-9565-2. [CrossRef] [Google Scholar]
Hu Y, Zhang X, Jin C, Peng X. Теория полуидеального решения. 3. Расширение вязкости многокомпонентных водных растворов. Дж. Солют. хим. 2010;39: 1828–1844. doi: 10.1007/s10953-010-9565-2. [CrossRef] [Google Scholar]
29. Абдулагатов ИМ, Азизов НД. Вязкость водных растворов хлорида кальция при высоких температурах и высоких давлениях. Равновесие жидкой фазы. 2006; 240:204–219. doi: 10.1016/j.fluid.2005.12.036. [CrossRef] [Google Scholar]
30. Zhang J, Moosavi M, Rostami AA, Vargas MM. Моделирование вязкости смесей вода + алкандиолы. Дж. Мол. жидкость 2018; 249:326–333. doi: 10.1016/j.molliq.2017.11.005. [Перекрестная ссылка] [Академия Google]
31. Лалиберте М. Модель расчета теплоемкости водных растворов с обновленными данными о плотности и вязкости. Дж. Хим. англ. Данные. 2009; 54: 1725–1760. doi: 10.1021/je8008123. [CrossRef] [Google Scholar]
32. Гонсалвес Ф.А., Кестин Дж. Вязкость растворов CaCl 2 в диапазоне 20–50 °C. Бер. Бунзенгес. физ. хим. 1979; 83: 24–27. doi: 10.1002/bbpc.19790830105. [CrossRef] [Google Scholar]
хим. 1979; 83: 24–27. doi: 10.1002/bbpc.19790830105. [CrossRef] [Google Scholar]
33. Александров А.А., Джураева Е.В., Утенков В.Ф. Вязкость водного раствора хлорида натрия. Высокий темп. 2012;50:354–358. дои: 10.1134/S0018151X12030029. [CrossRef] [Google Scholar]
34. Кестин Дж., Халифа Х.Э., Коррейя Р.Дж. Таблицы динамической и кинематической вязкости водных растворов NaCl в интервале температур 20–150 °С и диапазоне давлений 0,1–35 МПа. Дж. Физ. хим. Ссылка Данные. 1981; 10: 71–80. дои: 10.1063/1.555641. [CrossRef] [Google Scholar]
35. Hu YF, Lee H. Прогнозирование вязкости смешанного раствора электролита на основе абсолютной теории Эрвина и полуидеальной модели гидратации. Электрохим. Акта. 2003;48:1789–1796. doi: 10.1016/S0013-4686(03)00226-3. [CrossRef] [Google Scholar]
36. Glasstone S, Laidler KJ, Eyring H. Theory of Rate Process. Нью-Йорк: Макгроу-Хилл; 1941. [Google Scholar]
37. Кумар А. Простые уравнения для прогнозирования объемных свойств водных концентрированных смесей электролитов. проц. Индийская акад. науч. хим. науч. 1986; 96: 97–101. [Google Scholar]
проц. Индийская акад. науч. хим. науч. 1986; 96: 97–101. [Google Scholar]
38. Yang J, et al. Систематическое изучение простых подходов к прогнозированию термодинамических и транспортных свойств многокомпонентных растворов. Инд.Инж. хим. Рез. 2010;49: 7671–7677. doi: 10.1021/ie100752w. [CrossRef] [Google Scholar]
39. Махиуддин С., Исмаил К. Зависимость вязкости системы Mg(NO3) 2 –H 2 O от температуры и концентрации. Можно. Дж. Хим. 1982; 60: 2883–2888. дои: 10.1139/v82-413. [CrossRef] [Google Scholar]
40. Махиуддин С., Исмаил К. Концентрационная зависимость вязкости водных растворов электролитов от более высокой концентрации. Дж. Физ. хим. 1983; 87: 5241–5244. doi: 10.1021/j150643a036. [Перекрестная ссылка] [Академия Google]
41. Афзал М., Салим М., Махмуд М.Т. Температурная и концентрационная зависимость вязкости водных электролитов от 20 до 50 °С. Хлориды Na+, K+, Mg2+, Ca2+, Ba2+, Sr2+, Co2+, Ni2+, Cu2+ и Cr3+ J. Chem. англ. Данные. 1989; 34: 339–346. doi: 10.1021/je00057a023. [CrossRef] [Google Scholar]
Данные. 1989; 34: 339–346. doi: 10.1021/je00057a023. [CrossRef] [Google Scholar]
42. Goldsack DE, Franchetto AA. Вязкость концентрированных растворов электролитов. III. Закон смеси. Электрохим. Акта. 1977; 22: 1287–1294. doi: 10.1016/0013-4686(77)87012-6. [Перекрестная ссылка] [Академия Google]
43. Новлан М.Ф. Прогнозирование вязкости растворов смешанных электролитов по данным по одной соли. Можно. Дж. Хим. англ. 1980; 58: 637–642. doi: 10.1002/cjce.5450580514. [CrossRef] [Google Scholar]
44. Патвардхан В.С., Кумар А. Единый подход к прогнозированию термодинамических свойств водных растворов смешанных электролитов. Часть I: давление пара и теплота парообразования. Айше Дж. 1986; 32:1419–1428. doi: 10.1002/aic.690320903. [CrossRef] [Google Scholar]
45. Патвардхан В.С., Кумар А. Единый подход к прогнозированию термодинамических свойств водных растворов смешанных электролитов. Часть II: объемные, тепловые и другие свойства. Айше Дж. 1986;32:1429–1438. doi: 10. 1002/aic.690320904. [CrossRef] [Google Scholar]
1002/aic.690320904. [CrossRef] [Google Scholar]
46. Sun, Y. et al. Экспериментальные и модельные исследования плотности водных растворов хлорида 1-карбоксиметил-3-метилимидазолия, хлорида 1-карбоксиметил-3-пропилимидазолия и хлорида 1-(2-гидроксиэтил)-3-пропилимидазолия при (29315, 29815 и 30315) ) К. J. Chem. англ. Данные 59 , 250–249 (2014).
Плотность поверхностного заряда на кремнеземе в растворах электролитов хлоридов щелочных и щелочноземельных металлов
- Дав, Патрисия М. ;
- Крейвен, Колин М.
Аннотация
Плотность поверхностного заряда коллоидного SiO 2 (Аэросил 380) измеряли в хлоридах щелочных металлов (0,067 и 0,20 М LiCl, NaCl и KCl) и хлоридах щелочноземельных металлов (0,067 М MgCl 9 ). 0039 2 , CaCl 2 , SrCl 2 , BaCl 2 ) растворы. Измерения проводили при 25°С методом потенциометрического титрования с использованием метода постоянной ионной среды в системе, не содержащей СО 2 . План эксперимента измерял поверхностный заряд для растворов с постоянной ионной силой, а также постоянной концентрацией катионов. Растворы хлорида щелочного металла способствуют отрицательной плотности поверхностного заряда в порядке LiCl < NaCl < KCl, что дает «обычное» лиотропное поведение, о котором сообщалось ранее. Напротив, растворы хлоридов щелочноземельных металлов демонстрируют обратную лиотропную тенденцию с увеличением кристаллографического радиуса, где способствует увеличению отрицательного заряда в порядке BaCl 2 < SrCl 2 < CaCl 2 < MgCl 2 . Происхождение противоположных тенденций сродства исследуется путем проверки гипотезы о том, что это изменение коренится в различных характеристиках структурирования растворителя катионов IA и IIA на границе раздела кремнезем-вода.
0039 2 , CaCl 2 , SrCl 2 , BaCl 2 ) растворы. Измерения проводили при 25°С методом потенциометрического титрования с использованием метода постоянной ионной среды в системе, не содержащей СО 2 . План эксперимента измерял поверхностный заряд для растворов с постоянной ионной силой, а также постоянной концентрацией катионов. Растворы хлорида щелочного металла способствуют отрицательной плотности поверхностного заряда в порядке LiCl < NaCl < KCl, что дает «обычное» лиотропное поведение, о котором сообщалось ранее. Напротив, растворы хлоридов щелочноземельных металлов демонстрируют обратную лиотропную тенденцию с увеличением кристаллографического радиуса, где способствует увеличению отрицательного заряда в порядке BaCl 2 < SrCl 2 < CaCl 2 < MgCl 2 . Происхождение противоположных тенденций сродства исследуется путем проверки гипотезы о том, что это изменение коренится в различных характеристиках структурирования растворителя катионов IA и IIA на границе раздела кремнезем-вода. Эта идея возникает из более ранних постулатов о том, что эффекты структурирования растворителя увеличивают энтропию за счет разупорядочения растворителя, и этот выигрыш должен быть намного больше, чем небольшая положительная энтальпия, связанная с электростатическими взаимодействиями. Сопоставляя измеренную плотность заряда с прокси-фактором способности катионов к структурированию растворителя, это исследование показывает, что поверхностная плотность заряда кремнезема максимизируется за счет тех электролитов, которые оказывают наиболее сильное влияние на структурирование растворителя. Мы предполагаем, что для данного твердого материала энтропия сольватации играет роль в определении ионной специфичности электростатических взаимодействий, и повторяем идею о том, что концепция лиотропии коренится в способности катионов к структурированию растворителя на границе раздела.
Эта идея возникает из более ранних постулатов о том, что эффекты структурирования растворителя увеличивают энтропию за счет разупорядочения растворителя, и этот выигрыш должен быть намного больше, чем небольшая положительная энтальпия, связанная с электростатическими взаимодействиями. Сопоставляя измеренную плотность заряда с прокси-фактором способности катионов к структурированию растворителя, это исследование показывает, что поверхностная плотность заряда кремнезема максимизируется за счет тех электролитов, которые оказывают наиболее сильное влияние на структурирование растворителя. Мы предполагаем, что для данного твердого материала энтропия сольватации играет роль в определении ионной специфичности электростатических взаимодействий, и повторяем идею о том, что концепция лиотропии коренится в способности катионов к структурированию растворителя на границе раздела.
- Публикация:
Геохимика и Космохимика Acta
- Дата публикации:
- ноябрь 2005 г.


 Как раз через эти отверстия (обычно их число равно шести, как и количество секций) и осуществляется забор состава для замера плотности.
Как раз через эти отверстия (обычно их число равно шести, как и количество секций) и осуществляется забор состава для замера плотности.