Приготовление электролита для аккумуляторов своими руками
В настоящее время выбор аккумуляторных батарей огромен — в продаже можно найти уже готовые к использованию источники питания, а также сухозаряженные батареи, которые требуют осуществить приготовление электролита и его заливку до начала эксплуатации. Дальнейшее обслуживание аккумуляторов многие часто осуществляют в сервисах. По разным причинам может возникнуть необходимость самостоятельно приготовить раствор. Чтобы это мероприятие увенчалось успехом, следует знать, как сделать электролит в домашних условиях.
Содержание:
- 1 Что такое электролит?
- 2 Концентрация серной кислоты в АКБ
- 3 Отличия электролитов для разных типов аккумуляторов
- 3.1 Щелочные АКБ
- 3.2 Кислотные АКБ
- 4 Другие виды АКБ: можно ли приготовить электролит для них самостоятельно?
- 4.1 Кадмиевоникелевые и железоникелевые аккумуляторы
- 5 Как правильно приготовить электролит в домашних условиях: техника безопасности
- 5.
 1 Оборудование
1 Оборудование - 5.2 Последовательность процесса: делаем электролит для кислотно-свинцового источника питания
- 5.
- 6 Способ развести электролит для щелочного источника питания
Что такое электролит?
Электролит — электропроводящий раствор, содержащий в своём составе дистиллированную воду и серную кислоту, едкий калий или натрий в зависимости от типа источника питания.
Концентрация серной кислоты в АКБ
Этот показатель кислотности напрямую зависит от необходимой плотности электролита. Изначально средняя концентрация этого раствора в автомобильном аккумуляторе — около 40% в зависимости от температуры и климата, в которых используется источник питания. Во время эксплуатации концентрация кислоты падает до 10–20%, что сказывается на работоспособности АКБ.
Вместе с тем стоит понимать, что аккумуляторная серная составляющая — наичистейшая жидкость, которая на 93% состоит непосредственно из кислоты остальные 7% — примеси. На территории России производство этого химиката строго регламентировано — продукция должна соответствовать требованиям ГОСТ.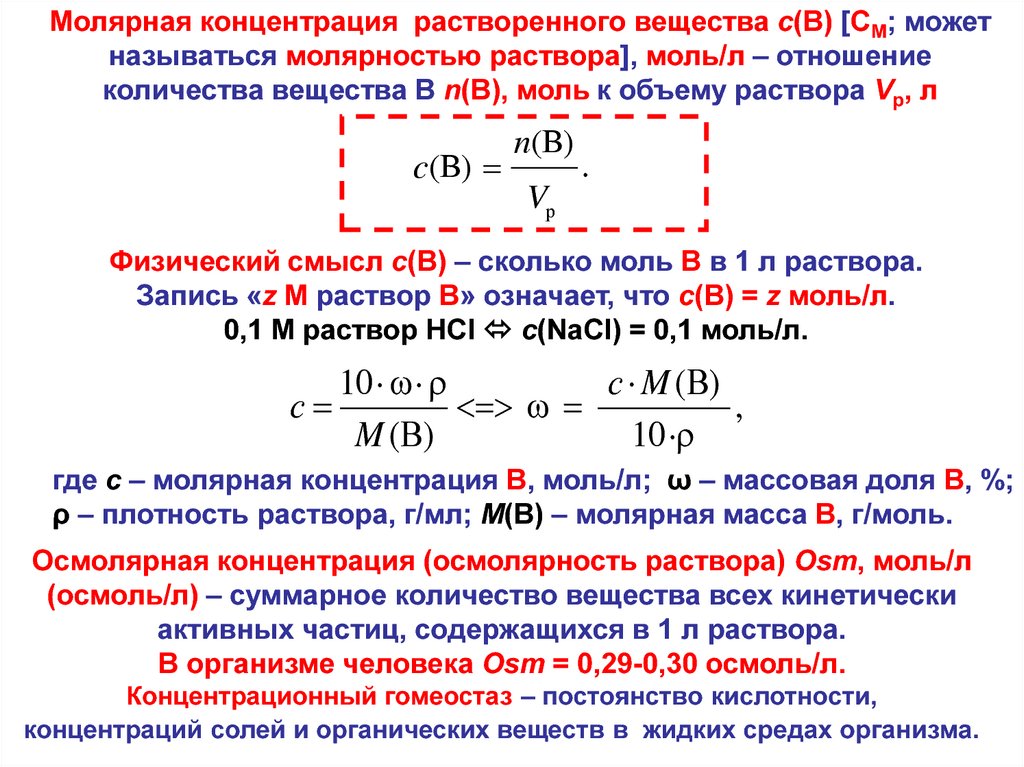
Отличия электролитов для разных типов аккумуляторов
Несмотря на то что принцип работы раствора одинаков для разных источников питания, следует знать о некоторых различиях составов. В зависимости от состава принято выделять щелочной и кислотный электролиты.
Щелочные АКБ
Этот вид источников питания характеризуется наличием гидроокиси никеля, окиси бария и графита. Электролит в этом виде аккумуляторов представляет собой 20% раствор едкого калия. Традиционно используется добавка моногидрата лития, которая позволяет продлить срок эксплуатации АКБ.
Щелочные источники питания отличаются отсутствием взаимодействия калийного раствора с веществами, образуемыми во время работы аккумулятора, что способствует аксимальному уменьшению расхода.
Кислотные АКБ
Этот вид источников питания является одним из самых традиционных, поэтому и раствор в них знаком многим — смесь дистиллированной воды и серного раствора. Концентрат электролита для свинцово-кислотных аккумуляторов дешёво стоит и характеризуется способностью проводить ток большой величины. Плотность жидкости должна соответствовать климатическим показателям.
Плотность жидкости должна соответствовать климатическим показателям.
Таблица 1. Рекомендуемая плотность электролита
Другие виды АКБ: можно ли приготовить электролит для них самостоятельно?
Отдельно хотелось бы обратить внимание на современные свинцово-кислотные источники питания — гелевые и AGM. Они также могут быть заправлены собственноручно приготовленным раствором, который в них находится в специфической форме — в виде геля или внутри сепараторов. Для заправки гелевых аккумуляторов понадобится ещё один химический компонент — силикагель, который загустит кислотный раствор.
Кадмиевоникелевые и железоникелевые аккумуляторы
В отличие от свинцовых источников питания, кадмиево- и железоникелевые заливаются щелочным растовром, который является смесью дистиллированной воды и едкого калия или натрия. Гидроксид лития, входящий в состав этого раствора для определённых температурных режимов, позволяет увеличить срок службы АКБ.
Таблица 2.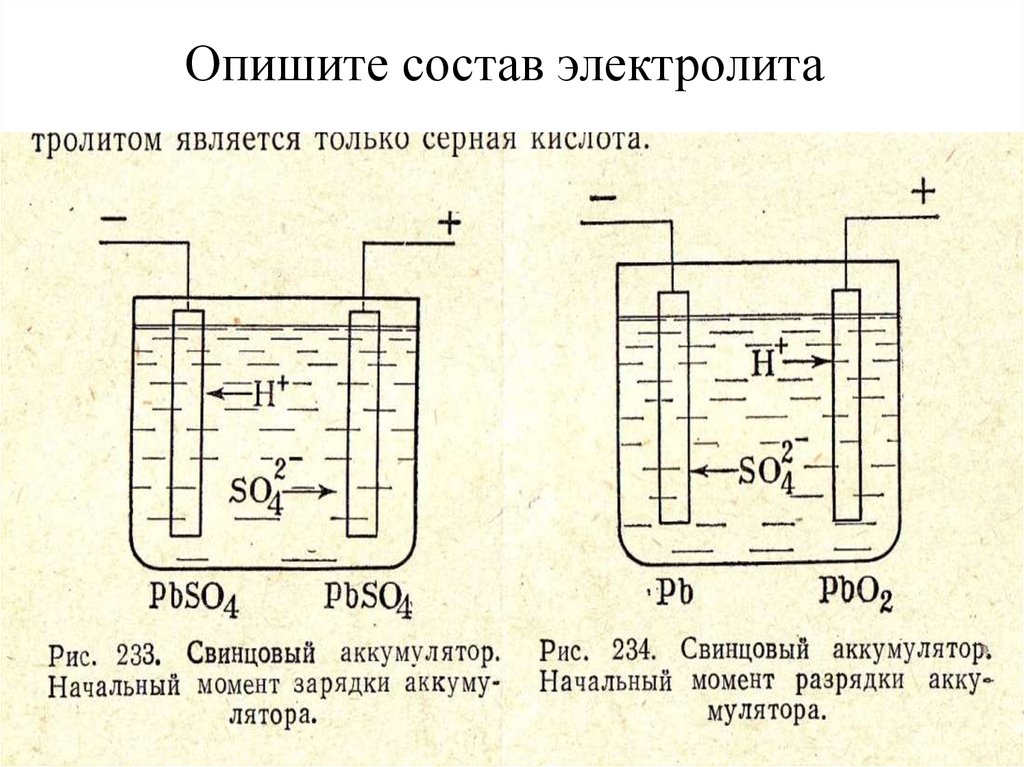 Состав и плотность электролита для кадмиево- и железоникелевых и аккумуляторов.
Состав и плотность электролита для кадмиево- и железоникелевых и аккумуляторов.
Железоникелевые источники питания рекомендуется эксплуатировать в тех же условиях, что и кадмиево-никелевые. Однако стоит отметить, что они более восприимчивы к низким температурам. Поэтому их следует использовать до минус 20 градусов.
Как правильно приготовить электролит в домашних условиях: техника безопасности
Приготовление раствора — работа с кислотами и щелочами, поэтому соблюдение мер предосторожности необходимо для самых опытных людей. Перед началом действия подготовьте средства защиты:
- резиновые перчатки
- одежду и фартук, устойчивый химическим веществам;
- защитные очки;
- нашатырный спирт, кальцинированную соду или борный раствор, чтобы нейтрализовать кислоту и щёлочь.
Оборудование
Для приготовления аккумуляторного электролита помимо самого источника питания потребуются следующие предметы:
- ёмкость и палочка, устойчивые к воздействию кислот и щелочей;
- дистиллированная вода;
- инструменты для измерения уровня, плотности и температуры раствора;
- аккумуляторная серная жидкость — для кислотной АКБ, твёрдые или жидкие щелочи, литий — для соответствующих видов АКБ, силикагель — для гелевых аккумуляторов.

Последовательность процесса: делаем электролит для кислотно-свинцового источника питания
Перед началом работ ознакомьтесь с информацией, приведённой в таблице 3. Она позволит выбрать необходимый объем жидкостей. В аккумуляторах залито от 2,6 до 3,7 литра кислотного раствора. Мы рекомендуем разводить примерно 4л электролита.
Таблица 3. Пропорции воды и серной кислоты.
- В ёмкость, устойчивую к едким веществам, налейте нужный объем воды.
- Разбавлять воду кислотой следует постепенно.
- По окончании процесса вливания замеряйте плотность получившегося электролита с помощью ареометра.
- Дайте составу отстояться около 12 часов.
Таблица 4. Плотность электролита для разных климатов.
Концентрация кислотного раствора должна соотноситься с минимальной температурой, при которой эксплуатируется аккумулятор. Если жидкость получилась слишком концентрированной, её необходимо разбавить дистиллированной водой.
Смотрите видео, как измерить плотность электролита.
Внимание! Вливать воду в кислоту нельзя! В результате этой химической реакции может возникнуть закипание состава, что приведёт к его расплескиванию и возможности получить кислотные ожоги!
Обращаем ваше внимание, что во время смешивания компонентов выделяется тепло. В подготовленный аккумулятор следует заливать остывший раствор.
Способ развести электролит для щелочного источника питания
Плотность и количество электролита в таких аккумуляторах указана в инструкции по эксплуатации источника питания или на сайте компании-производителя.
Необходимая плотность раствора | Количество твёрдой щелочи равняется количеству электролита, разделенному на |
1,17–1,19 г/см³ | 5 |
1,19–1,21 г/см³ | 3 |
1,25–1,27 г/см³ | 2 |
- Влейте в посуду дистиллированную воду.

- Добавьте щелочь.
- Смешайте раствор, герметично его закройте и дайте настояться в течение 6 часов.
- По истечении времени слейте образовавшийся светлый раствор — электролит готов.
При появлении осадка следует его перемешивать. Если к концу отстаивания он остаётся, слейте электролит так, чтобы осадок не попал в аккумулятор — это приведёт к уменьшению срока его эксплуатации.
Внимание! Во время работ температура щелочного раствора не должна превышать 25 градусов по Цельсию. Если жидкость чрезмерно нагревается, охладите её.
После приведения раствора к комнатной температуре и его заливке в аккумулятор, источник питания необходимо полностью зарядить током, составляющим 10% от ёмкости АКБ (60Ач — 6А).
Как видите, приготовление раствора электролита не такое сложное дело. Главное, следует чётко определиться с необходимым количеством ингредиентов и помнить о безопасности. Вы пробовали развести электролит своими руками? Поделитесь опытом с нашими читателями в комментариях.
Серная кислота аккумуляторная
Оптовые поставки по России и странам СНГ
Узнать стоимость
Формула: h3SO4
Код ТН ВЭД: 2807001000
Стандарт: ГОСТ 667-73
Описание:
Серная кислота — бесцветная маслянистая жидкость, не имеющая запаха. С водой и серным ангидридом смешивается в любых соотношениях с выделением большого количества тепла. Контактная серная кислота с массовой долей моногидрата 92,5-94,0% является водным раствором моногидрата (100% серной кислоты). В технике под серной кислотой подразумевают любые соединения H
Серная кислота — одна из самых активных неорганических кислот.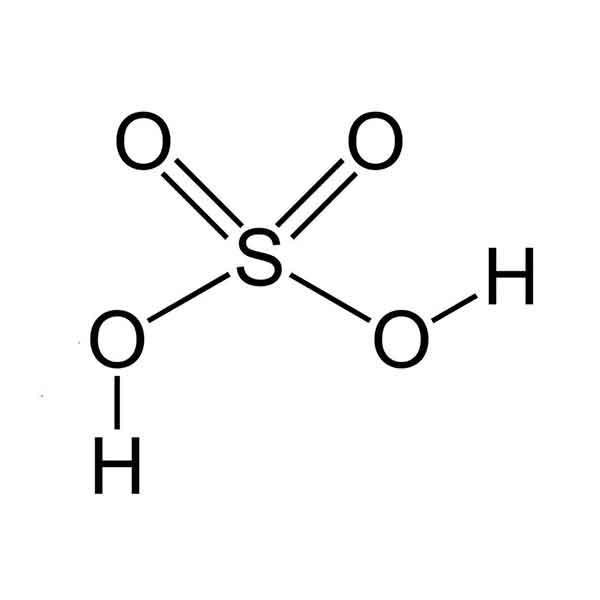 Она реагирует почти со всеми металлами и их оксидами, вступает в реакции обмена, обладает окислительными и другими важными свойствами. Основные физико-химические свойства растворов серной кислоты зависят от соотношения в ней воды и серного ангидрида (триоксида серы).
Она реагирует почти со всеми металлами и их оксидами, вступает в реакции обмена, обладает окислительными и другими важными свойствами. Основные физико-химические свойства растворов серной кислоты зависят от соотношения в ней воды и серного ангидрида (триоксида серы).
Применение:
Серная кислота используется в производстве минеральных удобрений, красителей, химических волокон, а также в металлургии. Она применяется для различных технологических целей в текстильной, пищевой и др. отраслях промышленности. Аккумуляторная серная кислота применяется после разбавления ее дистиллированной водой в качестве электролита для заливки свинцовых аккумуляторов.
В качестве электролита для аккумуляторных батарей применяют раствор серной аккумуляторной кислоты в дистиллированной воде. Для различных климатических и температурных условий, в которых батарее предстоит работать, используют электролит различной плотности. Плотность электролита зависит от концентрации раствора серной аккумуляторной кислоты — чем больше концентрация раствора, тем больше плотность электролита и от температуры раствора — чем выше температура, тем ниже плотность. Концентрация или плотность электролита является точным критерием степени разряженности аккумулятора. В качестве точки отсчета, для определения текущей степени разряженности аккумулятора, принимается нормативная плотность электролита, т.е. плотность, приобретенная после первого полого заряда. Для свинцовых аккумуляторов характерно сильное разбавление электролита во время разряда из-за участия в реакции серной аккумуляторной кислоты с образованием воды. В заряженных аккумуляторах концентрация кислоты равна 30…40%. Чем меньше объем электролита, в сравнении с массой электродов, тем быстрее снижается концентрация кислоты при разряде. В конце разряда она составляет от 10 до 25%.
Концентрация или плотность электролита является точным критерием степени разряженности аккумулятора. В качестве точки отсчета, для определения текущей степени разряженности аккумулятора, принимается нормативная плотность электролита, т.е. плотность, приобретенная после первого полого заряда. Для свинцовых аккумуляторов характерно сильное разбавление электролита во время разряда из-за участия в реакции серной аккумуляторной кислоты с образованием воды. В заряженных аккумуляторах концентрация кислоты равна 30…40%. Чем меньше объем электролита, в сравнении с массой электродов, тем быстрее снижается концентрация кислоты при разряде. В конце разряда она составляет от 10 до 25%.
ГОСТ 667-73
Влияние суперпластификатора и ускорителя набора прочности ПФМ-НЛК на подвижность бетонной смеси и прочностные характеристики бетона
Оставить заявку
| Технические характеристики | Высший сорт | Первый сорт |
|---|---|---|
| Массовая доля моногидрата (H 2SO4), % | 92-94 | 92-94 |
| Массовая доля железа (Fe), % | 0,005 | 0,01 |
| Массовая доля остатка после прокаливания, %, не более | 0,02 | 0,03 |
| Массовая доля оксидов азота (N2O4), %, не более | 0,00003 | 0,00001 |
| Массовая доля мышьяка (As), %, не более | 0,00005 | 0,00008 |
| Массовая доля хлористых соединений (Cl), %, не более | 0,0002 | 0,0003 |
| Массовая доля марганца (Mn), %, не более | 0,00005 | |
| Массовая доля суммы тяжелых металлов в пересчете на свинец (Pb), %, не более | 0,01 | 0,01 |
| Массовая доля меди (Cu), %, не более | 0,0005 | 0,0005 |
| Массовая доля веществ, восстанавливающих KMnO4, см3 раствора с (1/5 KMnO4) = 0,01 моль/дм3, не более | 4,5 | 7 |
| Прозрачность | Должна выдерживать испытание по п. 3.13 3.13 |
|
Упаковка:
Серная кислота упаковывается в ж/д и авто цистерны, канистры, кубовые емкости.
Хранение:
Техническая серная кислота и олеум (концентрированная серная кислота) должны храниться в емкостях из стали или спецстали, как нефутерованных, так и футерованных кислотоупорным кирпичом или кислотоустойчивым материалом.
Транспортировка:
Серную кислоту техническую транспортируют в железнодорожных сернокислотных цистернах в соответствии с правилами перевозок грузов. На цистерны должны быть нанесены специальные трафареты в соответствии с правилами перевозок грузов, действующими на ж.д. транспорте.
Техника безопасности:
Кислота серная пожаро- и взрывобезопасна, при соприкосновении ее с водой происходит бурная реакция с большим выделением тепла, паров и газов. Токсична. По степени воздействия на организм относится к веществам 2-го класса опасности. При работе с серной кислотой обязательно применять спецодежду.
Токсична. По степени воздействия на организм относится к веществам 2-го класса опасности. При работе с серной кислотой обязательно применять спецодежду.
Выгодно
Низкие цены за счёт прямых контрактов с производителями
Надёжно
Работаем более 20 лет (с 1997 года) под одним ИНН.
Товар на складе
Более 3 000 тонн продукции в наличии на наших складах
Качество гарантируем
Работаем только с проверенными поставщиками.
Доставим как надо
Контролируем товар на всем пути
Введите ваше имя
Введите ваш телефон
Нажимая кнопку «Получить бесплатную консультацию», Вы соглашаетесь с условиями Политики конфиденциальности.Наш специалист свяжется с Вами в ближайшее время.
Заявка направленная после 17:00 (+7 GMT),
обрабатывается на следующий день в рабочее время.
Введите ваше имя
Введите ваш телефон
Укажите ваш регион (город)
Нажимая кнопку «Узнать стоимость», Вы соглашаетесь с условиями Политики конфиденциальности.
Наш специалист свяжется с Вами в ближайшее время.
Заявка направленная после 17:00 (+7 GMT),
обрабатывается на следующий день в рабочее время.
Введите ваше имя
Введите ваш телефон
Укажите ваш регион (город)
Нажимая кнопку «Оставить заявку», Вы соглашаетесь с условиями Политики конфиденциальности.
Кислотная формула батареи: введение, качество и соотношение_ Аккумулятор Greenway
Электролит, присутствующий внутри аккумулятора, играет наиболее важную роль в работе аккумулятора. Он очень тщательно помещается в аккумулятор для обеспечения лучшей производительности, и здесь мы обсудим все о аккумуляторной кислоте, которая используется для производства аккумуляторной кислоты.
Помимо общих знаний, это будет очень полезно для вас, чтобы повысить производительность вашей батареи, если вы когда-нибудь будете восстанавливать или ремонтировать свои старые батареи.
Какова формула аккумуляторной кислоты? Аккумуляторная кислота производится из серной кислоты и дистиллированной воды, однако в производстве аккумуляторной кислоты используется именно серная кислота. Формула этой кислоты «h3so4». Здесь следующие элементы представляют следующую информацию:
?H означает, что в этой кислоте есть атом водорода, а 2 означает, что в кислоте есть два атома водорода.
?S означает, что в кислоте есть атом серы, а рядом с S нет числа, поэтому имеется только один атом серы.
?Последняя буква О представляет кислород, а рядом с О стоит цифра 4, что означает, что всего имеется 4 атома кислорода.
Итак, это формула серной кислоты, также известной как аккумуляторная кислота.??
Почему внутри батареи требуется серная кислота? Батарея вырабатывает электричество в результате химической реакции, происходящей внутри батареи. Эта реакция происходит между пластинами батареи, и этим пластинам батареи нужна среда, в которой электроны могут перемещаться без каких-либо проблем.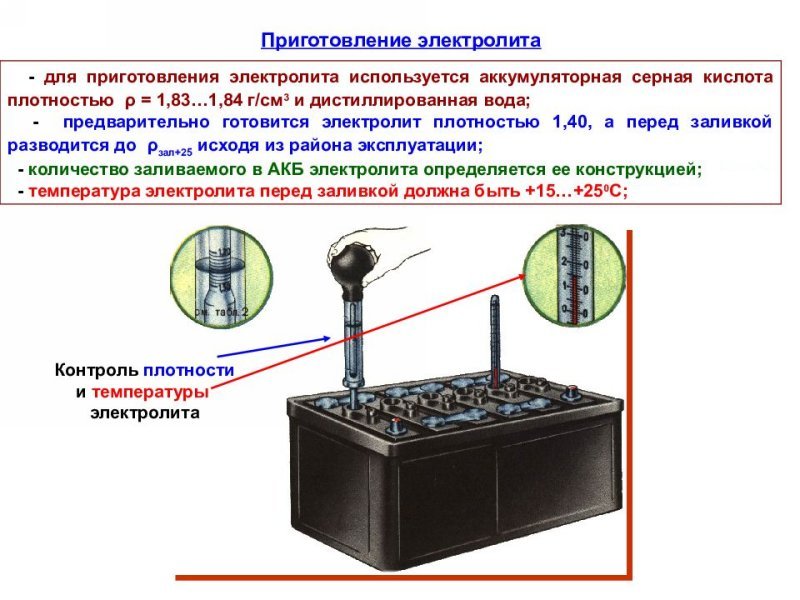 Что ж, серная кислота — это среда, обеспечивающая наилучшие характеристики батарей, потому что она очень помогает в реакции, называемой электролизом.
Что ж, серная кислота — это среда, обеспечивающая наилучшие характеристики батарей, потому что она очень помогает в реакции, называемой электролизом.
Почему в кислотных батареях используется только серная кислота? Хотя есть много других кислот, которые менее сильны, чем серная кислота, и некоторые из них могут даже не нуждаться в разбавлении. Тогда почему в батареях используется серная кислота?
Кислота в батареях играет большую роль в функционировании батареи.
Причина использования серной кислоты, особенно в разбавленной форме, заключается в том, что она обеспечивает наилучшие характеристики по сравнению со всеми другими кислотами. Если же говорить о разбавлении кислоты, то она работает еще лучше в течение длительного времени.
Сколько серной кислоты содержится в аккумуляторной кислоте? Все мы знаем, что аккумуляторная кислота представляет собой серную кислоту, но в разбавленном виде. Итак, нам любопытно, сколько серной кислоты используется в аккумуляторе при производстве аккумуляторной кислоты. Если рассматривать изготовление аккумуляторной кислоты частями, то можно сказать, что две из пяти или одна из трех частей аккумуляторной кислоты будет содержать серную кислоту, а остальные части будут состоять из торированной воды.
Если рассматривать изготовление аккумуляторной кислоты частями, то можно сказать, что две из пяти или одна из трех частей аккумуляторной кислоты будет содержать серную кислоту, а остальные части будут состоять из торированной воды.
Почему кислотные батареи разбавлены серной кислотой? Зачем разбавлять серную кислоту при производстве кислоты, если она так хорошо работает внутри батареи? Ну а в разбавлении серной кислоты, когда ее требуется заливать в аккумуляторы, есть целая логика.
Как мы знаем, это очень реактивный материал, когда он используется в батарее, он не только вызывает повреждение пластин батареи, но также повреждает внешний пластиковый слой крышки батареи.
Из-за этого очень сложно поддерживать работоспособность батареи в течение длительного времени. Вот почему серную кислоту разбавляют, чтобы сделать ее немного слабой, чтобы она не вступала в реакцию с внутренностями и корпусом батареи.
Почему аккумуляторы заполняются серной кислотой только до определенного уровня? Когда мы заправляем аккумулятор, он заполняется только до определенного уровня. Почему мы не можем превысить этот уровень кислоты в аккумуляторе, когда вода в конечном итоге испарится. В этом случае внутренние компоненты батареи тщательно спроектированы для обеспечения требуемой производительности.
Почему мы не можем превысить этот уровень кислоты в аккумуляторе, когда вода в конечном итоге испарится. В этом случае внутренние компоненты батареи тщательно спроектированы для обеспечения требуемой производительности.
В этом случае мощность электролита определяется количеством пластин. По этой причине уровень серной кислоты в аккумуляторе очень тщательно поддерживается.
Каково соотношение между кислотой и водой в аккумуляторе?Соотношение кислоты и воды внутри аккумуляторов составляет от 15% до 35% кислоты, а оставшееся количество заполняется дистиллированной водой. Это соотношение воды и кислоты в аккумуляторе очень важно поддерживать, поскольку оно оказывает серьезное влияние на производительность. Здесь мы подробно обсудим значение соотношения электролита и воды в аккумуляторе.
Почему очень важно поддерживать такое соотношение воды и кислоты в аккумуляторах? Когда производится аккумуляторная кислота или электролит, это делается с использованием серной кислоты и воды в определенном соотношении. Это соотношение очень важно поддерживать, потому что оно определяет, насколько хорошо батарея будет работать. Если мы увеличим количество воды в аккумуляторной кислоте, аккумулятор не будет работать эффективно, потому что он не будет заряжаться так, как он должен заряжаться.
Это соотношение очень важно поддерживать, потому что оно определяет, насколько хорошо батарея будет работать. Если мы увеличим количество воды в аккумуляторной кислоте, аккумулятор не будет работать эффективно, потому что он не будет заряжаться так, как он должен заряжаться.
С другой стороны, если увеличить количество серной кислоты, это может привести к необратимому повреждению внутренних частей батареи и не принесет пользы в долгосрочной перспективе.
Каковы преимущества поддержания соотношения кислоты и воды в батареях и как с этим бороться в долгосрочной перспективе?
Поддержание кислотно-щелочного баланса в электролитах очень важно и имеет ряд преимуществ. Здесь мы обсудим некоторые из этих преимуществ поддержания соотношения кислоты и воды в аккумуляторе.
Батарея работает очень хорошо, когда поддерживается это соотношение.
Батарея выполняет свои функции в течение длительного времени.
Поскольку батарея работает хорошо в течение длительного времени, можно значительно сэкономить.
Что делать в долгосрочной перспективе:
В долгосрочной перспективе вы можете добавить в аккумулятор немного дистиллированной воды, чтобы поддерживать уровень кислоты. Кроме того, не допускайте, чтобы уровень воды опускался ниже нижнего предела уровня воды внутри аккумулятора.
Заключение: Аккумуляторная кислота играет важную роль в работе аккумулятора. Здесь мы обсудили формулу и значение аккумуляторной кислоты в аккумуляторе. Эта информация может быть очень полезна при ремонте и обслуживании аккумулятора.
литий-ионный аккумулятор аккумулятор для электровелосипеда литиевый аккумулятор
химические окислительно-восстановительные щелочные батареи
химические окислительно-восстановительные щелочные батареиЩелочные батареи | ||
В щелочных батареях анод (отрицательный полюс) изготовлен из цинкового порошка. Это позволяет увеличить площадь поверхности, что приводит к увеличению скорости реакции и, следовательно, к большей скорости потока электронов. Они служат примерно в пять раз дольше, чем сухие элементы, изображенные ниже, и находят применение в приборах, требующих прерывистых всплесков сильного тока, таких как игрушечная машинка. Полуреакции:
|
| |
Справа изображена сухая камера. Нажмите, чтобы увидеть внутреннюю структуру. Электролит представляет собой пасту, состоящую из хлорида аммония и хлорида цинка, а не гидроксида калия, как в случае с щелочными батареями. При анодном (-) окислении цинкового корпуса образуются электроны в соответствии с приведенным ниже уравнением Zn(s) => Zn 2+ (водн.) + 2e — На катоде (+) происходит восстановление MnO 2 в соответствии с приведенным ниже уравнением. 2MnO 2 + 2NH 4 + (водн.) + 2e — => Mn 2 O 3 (тв) + 2NH 3 (водн.)0083 2 О(л)
| ||
Новый элемент выдает около 1,5 вольт, но это значение значительно меняется в зависимости от используемой батареи. Когда элемент разряжается, продукты накапливаются вокруг электродов и могут эффективно остановить прямую реакцию. Это происходит после длительного использования, и батарея может восстановиться, если оставить ее на некоторое время, чтобы позволить продуктам диффундировать от электродов. Например, газообразный аммиак может накапливаться на катоде и эффективно изолировать его от электролита. Через некоторое время газ рассеивается. Нагревание клетки увеличивает скорость диффузии и помогает клетке быстрее восстанавливаться. Это происходит после длительного использования, и батарея может восстановиться, если оставить ее на некоторое время, чтобы позволить продуктам диффундировать от электродов. Например, газообразный аммиак может накапливаться на катоде и эффективно изолировать его от электролита. Через некоторое время газ рассеивается. Нагревание клетки увеличивает скорость диффузии и помогает клетке быстрее восстанавливаться. | ||
| Помимо разницы в электролите, чем отличается щелочной элемент от сухого? Он производит в два раза больше напряжения, чем сухой элемент. Он работает дольше, чем сухой элемент, и производит больший ток. Он производит меньше тока, но работает дольше, чем сухой элемент. | ||
| Щелочная батарея использует цинковый порошок в качестве анода. Это имеет эффект Увеличивает скорость реакции и, следовательно, поток электронов. Продлевает срок службы батареи. Делает батарею более долговечной. | ||
Аккумулятор, проработавший в игрушечной машинке несколько недель, начинает разваливаться. Разное Разное | ||

 1 Оборудование
1 Оборудование

 Катод (положительный полюс) состоит из диоксида марганца. Щелочные батареи сравнимы с угольно-цинковыми батареями, но разница в том, что в щелочных батареях в качестве электролита используется гидроксид калия (КОН), а не хлорид аммония или хлорид цинка.
Катод (положительный полюс) состоит из диоксида марганца. Щелочные батареи сравнимы с угольно-цинковыми батареями, но разница в том, что в щелочных батареях в качестве электролита используется гидроксид калия (КОН), а не хлорид аммония или хлорид цинка. При попытке зарядить неперезаряжаемую батарею по крайней мере одна из окислительно-восстановительных реакций может быть необратимой, и иногда происходят нежелательные реакции с образованием газа. Это может быть опасной ситуацией.
При попытке зарядить неперезаряжаемую батарею по крайней мере одна из окислительно-восстановительных реакций может быть необратимой, и иногда происходят нежелательные реакции с образованием газа. Это может быть опасной ситуацией.