Как поднять плотность электролита в аккумуляторе в домашних условиях
У грамотного владельца автомобиля аккумулятор всегда заряжен. Владение знаниями и навыками проверки плотности электролита гарантирует отсутствие неприятностей при старте двигателя и работе сигнализации.
Важность аккумулятора в системе обеспечения функционирования автомобиля нельзя переоценить. Сам запуск двигателя, в первую очередь, зависит от стабильной работы аккумулятора. Одной из причин внезапной или несвоевременной разрядки АКБ является отклонение значения параметра густоты электролита от нормы.
Содержание статьи
Какая должна быть концентрация кислоты?
Плотность отражает отношение массовой доли серной кислоты и дистиллированной воды в составе электролита.
Требуемое соотношение – 1:2, в процентах это выглядит как 35%/65%. Более привычным для автомобилистов и специалистов по обслуживанию является измерение в граммах на кубический сантиметр (г/см³).
Измеряется показатель специальным прибором — ареометром. Показания в диапазоне 1,27-1,29 г/см³ говорят о нормальной плотности, обеспечивающей стабильную работу аккумулятора.
Важно! Именно благодаря наличию электролита строго определенной плотности происходит накопление заряда.
Аккумуляторная батарея – это последовательно подключенные изолированные друг от друга отсеки, в которых загружены пластины-электроды (плюс и минус). Каждый отсек генерирует такое напряжение, которое в сумме составляет примерно 12 вольт.
Почему падает насыщенность раствора в АКБ
Изменения концентрации электролита во время использования АКБ закономерно. Основными причинами падения значения параметра являются:
- Испарение раствора в результате закипания, которое может произойти при долгой зарядке;
- Просачивание жидкости через пробки на корпус, когда автомобиль эксплуатируется на дорогах с ухабами или на бездорожье;
- Разрядка АКБ, которая приводит к оседанию серной кислоты на пластинах (сульфатация)
Подробно рассмотрим почему падает плотность:
Испарение электролита.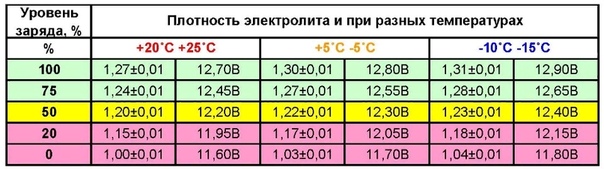 Обычно это длительный процесс, который продолжительное время позволяет АКБ работать, обеспечивая двигатель питанием, но он может быть стремительным, в случае закипания жидкости.
Обычно это длительный процесс, который продолжительное время позволяет АКБ работать, обеспечивая двигатель питанием, но он может быть стремительным, в случае закипания жидкости.
Аккумулятор у большинства автомобилей располагается рядом с двигателем. Нагрев устройства происходит естественным образом во время работы двигателя. В летний период, когда температура окружающей среды способствует скорейшему испарению жидкостей, следует проверять плотность электролита еженедельно.
При испарении достаточным действием является доливание дистиллированной воды в банки АКБ, поскольку испариться может только вода. Обязательной должна стать процедура перемешивания добавленной воды с имеющимся в банках раствором кислоты. Крайне важным этот процесс становится в период холодов, когда вода может замерзнуть.
Вытекание. Если замечено выплескивание или вытекание из отсеков аккумулятора смеси кислоты и дистиллированной воды, следует доливать электролит. Предварительно важно удалить с поверхности АКБ пролитый электролит при помощи чистой ветоши, раствором кальцинированной соды или нашатырным спиртом. Верхнюю часть корпуса батареи необходимо содержать в чистоте всегда.
Верхнюю часть корпуса батареи необходимо содержать в чистоте всегда.
Механическая очистка производится щеткой, имеющей жесткую щетину, исключая попадание устройства грязи.. Разрядка аккумулятора приводит к появлению на пластинах кристаллов сульфата свинца. Продолжительное отсутствие зарядки усугубляет ситуацию – кристаллы увеличиваются в размерах, покрывая всю поверхность металла. Это приводит в невозможности зарядки аккумулятора в связи с отсутствием контакта пластин с раствором кислоты.
Сульфатация. Процесс образования сульфита свинца – плохо растворимого кристаллического вещества, является результатом взаимодействия серной кислоты и не дистиллированной воды в аккумуляторе. Оседая на металлических пластинах, кристаллы становятся препятствием для прохождения заряда между электролитом и активной массой. Реакция возникает при особых условиях, в которых находиться аккумуляторная батарея. Например:
- АКБ хранился без зарядки продолжительное время
- использовался при высокой температуре
- зарядка АКБ производилась частично.
 Ежемесячно необходим 100% заряд батареи
Ежемесячно необходим 100% заряд батареи - батарея оказалась разряженной по предельного минимального значения.
Начавшийся процесс сульфатации можно остановить зарядным устройством, используя специальные режимы зарядки.
Внимание! После зарядки удельный вес кислоты повышается.
Опасности низкой и высокой концентрации кислоты
Повышенный показатель плотности раствора, сохраняющийся стабильно станет причиной сокращения срока эксплуатации аккумуляторной батареи. В результате повышения концентрации кислоты в электролите выше нормы, произойдет разрушение металлических пластин, ведь растворы с высокой концентрацией серной кислоты способны разрушить даже изделия из стали.
Свинцовые пластины, станут легкой добычей кислоты уже при плотности 1,35 г./см³.
Низкая концентрация раствора серной кислоты (менее 1,27 г/см³) станет причиной такого процесса, как сульфатация. Это оседание на пластинах кристаллов сульфита свинца, что лишает металл возможности накопления заряда.
Это оседание на пластинах кристаллов сульфита свинца, что лишает металл возможности накопления заряда.
При низком значении плотности (1,17 г/см³) порог замерзания -5 градусов. Жидкость замерзнет и сломает металлические пластины. Восстановить АКБ после замерзания и подобных деформаций еще никому не удавалось.
Внимание! Электролит замерзнет при температуре -7 градусов, если его густота 1,11 г/см³ и ниже, но если его плотность 1,28 г/см³, то он замёрзнет только при -58 градусах.
В таблице приведены данные зависимости плотности от температуры.
| плотность г/см3 | температура замерзания | плотность г/см3 | температура замерзания |
| 1,1 | -8 °С | 1,19 | -25 °С |
| 1,11 | 1,2 | -28 °С | |
| 1,12 | -10 °С | 1,21 | -34 °С |
| 1,13 | -12 °С | 1,22 | -40 °С |
| 1,14 | -14 °С | 1,23 | -45 °С |
| 1,15 | -16 °С | 1,24 | -50 °С |
| 1,16 | -18 °С | 1,25 | -54 °С |
| 1,17 | -20 °С | 1,28 | -58 °С |
| 1,18 | -22 °С |
Низкая концентрация электролита становится причиной затруднительного запуска двигателя и приводит к замерзанию жидкости при минусовых температурах.
А теперь посмотрим что делать при неполадках.
Как поднять самостоятельно плотность
Чтобы устранить причину неудовлетворительного состояния АКБ, необходимо выяснить причину падения плотности электролита.
В случае повреждения пластин, придется привлекать специалистов, учитывая, что вероятность восстановления батареи минимальна.
При условии, что падение концентрации произошло в результате изменения количества раствора или его состава, поднять плотность возможно в домашних условиях, следуя инструкции:
- Измерить концентрацию электролита в каждом отсеке (банке) отдельно.
- При полученных значениях густоты в диапазоне 1,18-1,20 г/см³, правильным решением станет процедура замены части электролита в банке на новый, нормальной концентрации- 1,27 г/см³.
- Грушей откачать отработанный раствор, замерить объем.
- Долить половину от изъятого объема новым. Потрясти АКБ, чтобы перемешать жидкость в банке.

- Измерить плотность.
- Повторять действия из пунктов 1-4 до получения необходимого значения параметра.
- Закрыть банки, приступить к зарядке аккумулятора.
Для проведения мероприятий, направленных на повышение плотности раствора серной кислоты понадобятся:
- Перчатки резиновые
- Прибор для измерения плотности –ареометр
- Резиновая груша
- Электролит
- Мерный стакан
- Емкость для слива жидкости из отсеков.
Внимание! Контакт со смесью кислоты и воды может вызвать ожоги, причем, не только кожных покровов, но и дыхательных путей. Самостоятельной заменой раствора кислоты следует заниматься с высокой степенью осторожности.
При отсутствии готового электролита возможно приготовление нужного раствора. Правильно вливать кислоту в воду, важно помнить, что вливать воду в кислоту – ОПАСНО.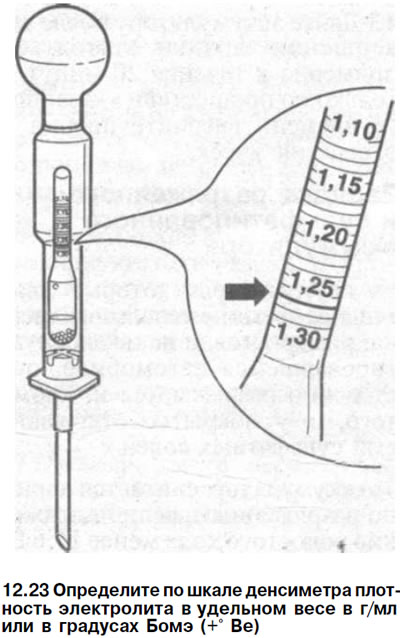
Вот подробная инструкция, как восстановить концентрацию кислоты в домашних условиях.
Подробная инструкция
Для обоснования необходимости проведения процедуры корректировки плотности электролита, измерение этого показателя обязательно должно быть произведено только при полностью заряженной батарее.
До начала процедуры важно определиться с уровнем густоты состава, который является целью. Корректировка плотности заключается в замене части раствора кислоты, находящегося в отсеках АКБ, тем же объемом электролита нужной плотности.
Вот подробная инструкция, как восстановить концентрацию кислоты в домашних условиях.
- Замену кислотно-водного раствора необходимо производить только после полной разрядки батареи током 10-часового разряда.
- Проверить уровень электролита в каждом отсеке, используя трубку для измерения. В процессе корректировки проверять уровень необходимо регулярно.
 Нормальным считается уровень, выше верхнего края пластин на 15-20 мм.
Нормальным считается уровень, выше верхнего края пластин на 15-20 мм. - Подготовить корректирующий раствор кислоты. Концентрация кислоты в таком составе должна быть не менее, чем 1,4 г/см³, если необходимо повысить плотность. Понижение плотности происходит путем замены части электролита на дистиллированную воду.
- АКБ должен простоять выключенным не менее 30 минут. Это время необходимо для выравнивания концентрации в отсеках.
- Батарею поставить заряжаться минимальным током на 30 минут.
- Отключить АКБ от зарядного устройства на 2 часа.
- Получить значения показателей плотности и уровня электролита.
- Повторять действия пунктов 2-6 до получения необходимого значения показателя.
Внимание! Концентрация раствора кислоты в отсеках не должна отличаться более, чем на 0,02 г/см³. В противном случае необходимо подзарядить АКБ током от 1 до 2 А в течение 24 часов.
Полезное видео
Популярный блогер подробно рассказал о плотности электролита в видео:
Заключение.
Проводить проверку уровня плотности раствора, содержащегося в банках автомобильного аккумулятора необходимо не дожидаясь признаков изменения этого параметра. Специалисты рекомендуют делать это не реже одного раза в месяц, если владелец автомобиля не отмечает изменений в работе АКБ, и значительно чаще, при особых условиях эксплуатации.
Только поддержание значения показателя плотности на оптимальном (рекомендованном) уровне, гарантирует стабильное накопление и сохранение заряда, что обеспечит безупречную работу двигателя.
Как поднять плотность электролита в аккумуляторе
Одним из главных параметров для автомобильного аккумулятора, который напрямую влияет на срок его службы – производительность и способность держать заряд является плотность электролита. Сразу же после приобретения новой батареи, это значение соответствует заявленному производителем для конкретной климатической полосы. При его выборе на это нужно обращать особое внимание, поскольку электролит также, как и моторное масло, предназначен для конкретных температур.
Сразу же после приобретения новой батареи, это значение соответствует заявленному производителем для конкретной климатической полосы. При его выборе на это нужно обращать особое внимание, поскольку электролит также, как и моторное масло, предназначен для конкретных температур.
Совет! Как приготовить электролит для аккумулятора.
Так, аккумулятор, плотность электролита в котором высока, может легко использоваться при сильных морозах, обеспечивая сохранение заряда и нормальный, уверенный пуск двигателя. В то же время батарея, плотность электролита в которой низкая можно использовать лишь в теплом климате. Низкая плотность батареи грозит не только плохим пуском при отрицательной температуре, но и постоянным недозарядом, что для любого аккумулятора является серьезным моментом для снижения срока его эксплуатации.
Содержание статьи
Замеряем плотность электролита правильно
Не секрет, что в процессе эксплуатации аккумулятора количество и плотность электролита меняется, поэтому автомобилисту приходится постоянно контролировать эти параметры самостоятельно. Для этого проводится техническое обслуживание АКБ. При этом важно, чтобы обслуживание проводилось правильно. Так, далеко не каждый автовладелец знает, что такой показатель, как плотность электролита в аккумуляторе измеряется лишь на полностью заряженной батарее.
Для этого проводится техническое обслуживание АКБ. При этом важно, чтобы обслуживание проводилось правильно. Так, далеко не каждый автовладелец знает, что такой показатель, как плотность электролита в аккумуляторе измеряется лишь на полностью заряженной батарее.
Т. е. замерить ее, не снимая АКБ с машины нельзя, поскольку автомобильная система заряда батареи не в состоянии зарядить ее на 100%. Кроме того, прежде всего нужно проверить и откорректировать уровень электролита. Это важно по той причине, что в процессе эксплуатации батарея нагревается, и происходит испарение воды из электролита, а более тяжелая кислота остается. Этот момент также негативно сказывается на состоянии внутренних пластин, поэтому нужно периодически добавлять в раствор именно воду, доводя объем электролита до нормы.
После восстановления объема аккумулятор необходимо полностью зарядить. Для этого используются зарядные устройства с возможностью регулировки силы зарядного тока. Поскольку перед тем, как измерить плотность электролита в аккумуляторе, его необходимо на 100% зарядить, целесообразно использовать ток небольшой величины, но длительное время, к примеру, в течении всей ночи. Лишь после окончания цикла заряда, отключения АКБ от источника напряжения и «отдыха» батареи не менее 6-ти часов можно приступать к измерению – результаты будут точно соответствовать действительности.
Лишь после окончания цикла заряда, отключения АКБ от источника напряжения и «отдыха» батареи не менее 6-ти часов можно приступать к измерению – результаты будут точно соответствовать действительности.
Алгоритм замера
Совет! Рекомендованная частота проверки состояния аккумулятора – 1раз/3 месяца, с обязательными промежуточными замерами напряжения на выводах.
Непосредственно сам замер начинается с демонтажа, очистки и визуального осмотра корпуса. После этого потребуется приготовить прибор для измерения плотности электролита и полую стеклянную трубочку, требующуюся для контроля уровня имеющегося в батарее раствора. Перед замером аккумулятор ставится на ровную поверхность, из него выкручиваются все пробки. Стеклянная трубочка опускается в одну из банок, свободный конец ее зажимается пальцем и извлекается для оценки. Нормальным уровнем считается 12-15 см. Если он ниже – требуется долить дистиллированной воды.
После этого аккумулятор полностью заряжается. Как правило, на это требуется ночь, а величина зарядного тока не должна превышать 1-1,5 А. С утра, когда батарея отключена от зарядного устройства, необходимо выждать 4-6 часов, после чего можно замерять плотность электролита автомобильного аккумулятора. Перед тем как измерить плотность электролита в аккумуляторе ареометром, желательно приготовить либо таблицу значений, либо инструкцию к данной модели батареи, где указаны конкретные значения плотности для различных регионов нашей страны. В дальнейшем берется ареометр, сжимается его резиновая груша для вытеснения воздуха, наконечник погружается в первую банку и необходимое количество раствора набирается в прибор.
Как правило, на это требуется ночь, а величина зарядного тока не должна превышать 1-1,5 А. С утра, когда батарея отключена от зарядного устройства, необходимо выждать 4-6 часов, после чего можно замерять плотность электролита автомобильного аккумулятора. Перед тем как измерить плотность электролита в аккумуляторе ареометром, желательно приготовить либо таблицу значений, либо инструкцию к данной модели батареи, где указаны конкретные значения плотности для различных регионов нашей страны. В дальнейшем берется ареометр, сжимается его резиновая груша для вытеснения воздуха, наконечник погружается в первую банку и необходимое количество раствора набирается в прибор.
После извлечения из батареи можно приступать к оценке результатов. Первое, что оценивается – это положение поплавка. Прибор имеет три цветовых зоны, из которых зеленая соответствует норме. Для более подробных данных можно использовать градуированную шкалу, по которой можно измерить плотность электролита в г/см3. Это значение должно составлять 1,25-1,27 для центральных регионов страны, где возможны достаточно сильные морозы. Но для регионов Крайнего Севера такого значения может не хватить, и его, как правило, немного повышают. После измерения в первой банке, аналогичным образом проверяются все оставшиеся. Показания в них должны быть одинаковыми или отличаться минимально. Оценивая результаты важно держать ареометр на уровне глаз, в противном случае можно ошибиться, считывая значения с мелкой шкалы. О правильной последовательности работ можно посмотреть на видео:
Это значение должно составлять 1,25-1,27 для центральных регионов страны, где возможны достаточно сильные морозы. Но для регионов Крайнего Севера такого значения может не хватить, и его, как правило, немного повышают. После измерения в первой банке, аналогичным образом проверяются все оставшиеся. Показания в них должны быть одинаковыми или отличаться минимально. Оценивая результаты важно держать ареометр на уровне глаз, в противном случае можно ошибиться, считывая значения с мелкой шкалы. О правильной последовательности работ можно посмотреть на видео:
Какие показатели плотности требуются для зимы
Естественно, что плотность электролита в аккумуляторе зимой и летом несколько отличается. В норме зимой она должна быть выше, летом можно использовать менее концентрированный раствор. Это связано не только с возможностью банального замерзания, но и с ускоренным саморазрядом батареи, а также большими нагрузками. К примеру, чтобы обеспечить стартеру возможность провернуть коленвал в загустевшем на морозе масле, аккумулятору «приходится» выдавать ток максимальной величины. Поэтому плотность электролита зимой должна быть выше.
К примеру, чтобы обеспечить стартеру возможность провернуть коленвал в загустевшем на морозе масле, аккумулятору «приходится» выдавать ток максимальной величины. Поэтому плотность электролита зимой должна быть выше.
Не следует чрезмерно завышать значения плотности заливаемого в аккумулятор электролита, поскольку после полной зарядки батареи это значение и без этого возрастет на 0,1-,03 г/см3. Если есть сомнения относительно того, какая плотность электролита в аккумуляторе зимой считается нормальной, выручит все та же инструкция к самому аккумулятору – там дано правильное значение с учетом не только климатического региона, но и технических особенностей самой батареи. Если после проверки оказывается, что плотность не соответствует норме, ситуацию следует исправлять, а не оставлять как есть – это чревато разрядом аккумулятора на морозе.
Для многих автовладельцев вопрос – как поднять плотность электролита в аккумуляторе – является непонятным и сложным, хотя на деле ничего сверхординарного в этом нет.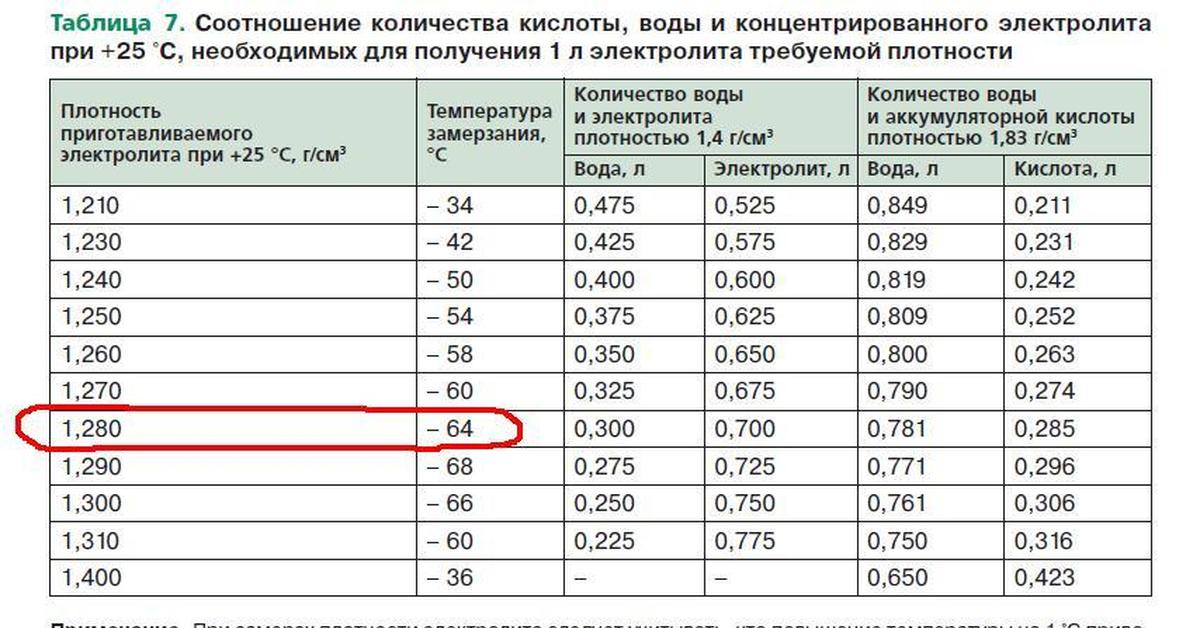 Чтобы повысить значение раствора до нормы потребуется запастись концентрированным электролитом и чистой дистиллированной водой. Перед тем как повысить плотность электролита в аккумуляторе рекомендуется разбавить концентрат водой. Занимаясь этим самостоятельно следует вначале налить в чистую емкость воды, и лишь потом понемногу добавлять в нее кислоту. Сделав наоборот можно получить реакцию, схожую с взрывом, в результате чего гарантированы химические ожоги.
Чтобы повысить значение раствора до нормы потребуется запастись концентрированным электролитом и чистой дистиллированной водой. Перед тем как повысить плотность электролита в аккумуляторе рекомендуется разбавить концентрат водой. Занимаясь этим самостоятельно следует вначале налить в чистую емкость воды, и лишь потом понемногу добавлять в нее кислоту. Сделав наоборот можно получить реакцию, схожую с взрывом, в результате чего гарантированы химические ожоги.
После того как раствор для добавления готов, его можно заливать в аккумулятор. Делать это нужно понемногу, соблюдая предельную осторожность. Естественно, что работать нужно только в защитных перчатках и очках. Добавив свежий электролит, необходимо подключить аккумулятор к зарядному устройству на полчаса, чтобы весь раствор внутри батареи тщательно перемешался за счет газовыделения. После этого значение плотности в каждой банке перепроверяется, и при необходимости корректируется вновь.
Совет! Стоит отметить, что прибор для измерения плотности электролита в аккумуляторе после каждой серии замеров следует обильно промыть дистиллированной водой чтобы исключить получение неточных данных.
Почему меняется плотность электролита
При эксплуатации аккумулятора он подвергается достаточно сильному нагреву – как со стороны атмосферы, так и со стороны работающего двигателя. естественно, что при этом активно начинает испаряться вода из электролита. Кислота при этом остается на месте. Во время проведения обслуживания водитель доливает воду, и плотность АКБ восстанавливается. После этого обновленный раствор замеряется ареометром. Это в идеале. На практике многие ограничиваются простым доливом, а в ряде случаев используется даже не вода, а концентрат. Это является ответом на вопрос почему падает плотность электролита в аккумуляторе, или же она, наоборот, повышается. Повысить плотность можно и в том случае, если используется неисправный ареометр.
Если не поднимается плотность электролита при зарядке, это является верным признаком того, что его пора заменить – частично или полностью. Оставлять батарею «как есть» в этом случае нельзя, поскольку она полностью разрядится в любой момент. Кроме того, неправильная плотность – как низкая, так и высокая, одинаково вредна АКБ, существенно снижая срок ее эксплуатации. Отсюда можно сделать простой вывод – измерение плотности электролита в аккумуляторе следует проводить каждый раз после зарядки батареи. Это не занимает много времени, но эффект от постоянного наличия в батарее достаточного количества электролита с нормальной плотностью не заставит себя ждать – легкий пуск двигателя в любой мороз и стабильная работа всей электроники в автомобиле гарантированы.
Кроме того, неправильная плотность – как низкая, так и высокая, одинаково вредна АКБ, существенно снижая срок ее эксплуатации. Отсюда можно сделать простой вывод – измерение плотности электролита в аккумуляторе следует проводить каждый раз после зарядки батареи. Это не занимает много времени, но эффект от постоянного наличия в батарее достаточного количества электролита с нормальной плотностью не заставит себя ждать – легкий пуск двигателя в любой мороз и стабильная работа всей электроники в автомобиле гарантированы.
Доливать электролит при низкой плотности
Множеству автомобилистов знакома такая проблема, как быстрая разрядка аккумулятора даже при отсутствии высокой нагрузки.
Встречаются совсем тяжёлые случаи — заряженный сегодня на 50% аккумулятор завтра же становится полностью разряженным и это обнаруживается во время попытки завести двигатель. Автомобилист заряжает аккумулятор на 100%, но завтра он снова наполовину разряжен. Как решить эту проблему? Покупка новой АКБ — это недёшево, но замена объективно требуется не в каждом случае, иногда достаточно проверки плотности и доливания электролита.
Множество автовладельцев волнует, насколько целесообразно доливание электролита в АКБ при недостаточной плотности. Возможно, лучше выполнить замену? Рассмотрим разные ситуации, чтобы выяснить, как лучше поступить в том или ином случае.
Когда доливание электролита в АКБ более целесообразно, чем замена АКБ?
Составляющими электролита любой АКБ являются кислота и дистиллированная вода. Данные жидкости образуют смесь, в составе которой преобладает вода, тогда как кислоты намного меньше. К примеру, Вам нужен электролит, плотность которого должна составлять 1,28 г/куб. см. В этом случае в 1 л дистиллированной воды необходимо влить 0,36 л кислоты. Пропорция будет составлять примерно 1:3.
Для безопасности требуется заливание кислоты в воду, но ни в коем случае не на оборот! Поскольку в противном случае имеет место высокий риск химической реакции, сопровождаемой выделением тепла и разбрызгиванием. Попадание аккумуляторной кислоты на кожу приводит к сильным ожогам. Причина этого заключается в более низкой плотности воды по сравнению с кислотой, вследствие чего эти жидкости смешиваются крайне медленно.
Объёмную пропорцию воды и кислоты выясняют с помощью ареометра. Этот прибор определяет плотность жидкости. После понижения плотности электролита до определённого значения он недостаточно хорошо удерживает заряд. При плотности немного ниже нужных 1,3 г/куб см, следует доливать электролит.
Изменение плотности электролита зависит заряда аккумулятора. По этой причине точную плотность аккумуляторной жидкости возможно только когда аккумулятор заряжен на 100%. Как правильно заряжать АКБ вы можете прочитать в отдельной статье.
%rtb-4%
Низкая плотность электролита — как решить проблему?
Если АКБ не держит заряд, нужна ли её замена? Целесообразно ли доливание электролита в случае недостаточной плотности? Или это всё равно не позволит восстановить работоспособность аккумулятора? Здесь всё определяется возрастом АКБ, а также показателями ареометра.
В случае, когда АКБ довольно старая (четыре года и более), потеря ею способности удерживать заряд прежде всего вызывается не недостатком плотности электролита, а разрушением пластин аккумуляторных банок. В подобной ситуации не поможет даже восстановление прежнего уровня плотности электролита. Но в случае сравнительной свежести аккумулятора решение проблемы возможно путём доливания электролита. Однако не всегда необходимо лить именно его.
В подобной ситуации не поможет даже восстановление прежнего уровня плотности электролита. Но в случае сравнительной свежести аккумулятора решение проблемы возможно путём доливания электролита. Однако не всегда необходимо лить именно его.
Среднестатистическая плотность этой жидкости в исправном аккумуляторе — от 1,25 до 1,3 г/куб. см. Необходимо, чтобы эта величина была приблизительно одинаковой у всех аккумуляторных банок. Максимальное допустимое отклонение — 0,03. В случае, когда плотность ниже 1,25, однако выше 1,20, доливанием электролита можно будет устранить проблему.
Плотность жидкости менее 1,2 г/куб. см
Можно ли доливать электролит в данном случае?
Ответ: Да. Однако таким путём не удастся добиться восстановления работоспособности аккумулятора, поскольку при доливании электролита не выйдет довести плотность до 1,25 г/куб. см. При плотности в диапазоне 1…1,2, целесообразней долить аккумуляторную кислоту, поскольку её плотность намного выше плотности электролита.
Плотность жидкости менее 1 г/куб. см
Когда ареометр показывает плотность электролита менее 1 г/куб. см, даже доливанием кислоты решить проблему не получится. Но в случае, когда невозможно заменить аккумулятор, можно попытаться заменить электролит. Для выполнения этой операции требуется откачивание из всех аккумуляторных банок с помощью груши максимально возможного объёма жидкости с последующим укладыванием его набок. Потом высверлить в днищах всех аккумуляторных банок маленькие дырочки, диаметр каждой из которых должен составить три-пять мм. Промыть банки дистиллированной водой. После чего отверстия можно запаять (для этого подходит пластмасса, устойчивая к воздействию кислот, предварительно рекомендуется проверить её реакцию на электролит) и заливать во все банки новый электролит.
Однако даже в случае выполнения этой операции АКБ будет служить недолго, поскольку время эксплуатации определяется многими факторами. После полного сливания электролита, аккумуляторные банки в течение какого-то времени имеют контакты с кислородом, вследствие чего начинается быстрая коррозия. По этой причине долго эксплуатировать АКБ после полной замены электролита нежелательно, лучше заменить АКБ при первой появившейся возможности.
Как часто заряжать автомобильный аккумулятор?
Методики проверки уровня зарядки аккумулятора
Как работает аккумулятор и 3 способа его испортить
Одно из самых полезных электронных устройств, доступных нам, также является одним из самых распространенных. Современные аккумуляторы используются во многих из наших любимых технологий, что можно почти простить за то, что вы не тратите время на изучение их работы.
Но теперь для вас настало время расширить свою базу знаний, поняв, как работает смартфон в вашем кармане, каковы распространенные типы аккумуляторов и что вы можете сделать, чтобы продлить срок их службы.
Краткая история батарей
Алессандро Вольта продемонстрировал первую работающую электромагнитную батарею в 1800 году.Его стопка из медных и цинковых пластин, разделенных пропитанными рассолом бумажными дисками, вырабатывала стабильное напряжение в течение «разумного» времени. Это было известно как гальваническая батарея и послужило предшественником поколения экспериментов с батарейным питанием.
В 1836 году Джон Фредерик Дэниелл стандартизировал конструкцию батареи.Медный горшок, наполненный раствором медного купороса, погруженный в неглазурованный глиняный сосуд, наполненный серной кислотой, и цинковый электрод стали де-факто стандартом аккумуляторов, распространенным в бесчисленных электрических телеграфных сетях.
Перенесемся в Оксфордский университет, 1979 год.Джон Гуденаф и Коичи Мидзусима продемонстрировали работающий перезаряжаемый элемент с диапазоном 4 В, в котором в качестве положительного электрода использовался оксид лития-кобальта, а в качестве отрицательного — металлический литий. Предшественник литиевого элемента в том виде, в каком мы его знаем, родился, но был коммерциализирован только в 1991 году Sony и Asahi Kasei в своих портативных электронных устройствах.
Что такое современная батарея?
Мы используем термин современная батарея для описания электрохимических элементов, которые питают наши портативные технологические устройства.Батареи делятся на две общие категории:
- Одноразовые: одноразовые батарейки с электродами, которые необратимо меняются во время использования.
- Аккумуляторные: многоразовые батареи с электродами, восстанавливаемыми обратным током.
В большинстве современных портативных электронных устройств используется литиевая батарея, наиболее распространенной из которых является литий-ионный ( Li-ion ) элемент. Вы также можете встретить литий-полимерный ( Li-Po ) элемент, который имеет такой же электрохимический состав и общий химический состав, что и его аналог, но стоит дороже в производстве и имеет более низкую плотность энергии.
Тем не менее, Li-Po аккумуляторы по-прежнему популярны из-за их легкого, гибкого дизайна и улучшенных рабочих характеристик при более высоких и низких температурах, с чем Li-ion может бороться.
Литий-ионные батареи обычно содержат интеркалированное соединение лития, такое как оксид лития-кобальта (LiCoO 2 ) в качестве одного электрода, графит в качестве второго и органический растворитель в качестве электролита.Это соединение используется из-за его высокой плотности энергии и медленной потери заряда, когда он не используется, а также из-за того, что не требуется циклическое переключение памяти для продления срока службы батареи.
Все литиевые батареи содержат температурный коэффициент давления.Это отказоустойчивый выключатель или датчик, предназначенный для предотвращения перегрева батареи в экстремальных условиях или чрезмерного использования, процесса, который обычно делает батарею бесполезной из-за необратимого повреждения химических соединений, которые делают возможным процесс заряда / разряда.
Процесс зарядки
Литиевые батареи стали предпочтительными для портативных технологий благодаря их высокой плотности энергии и перезаряжаемым качествам.
Во время процесса зарядки ионы лития перемещаются через электролит от положительного электрода из оксида лития-кобальта к отрицательному электроду из графита.При разряде или использовании ионы возвращаются через электролит, от отрицательного к положительному. Этот процесс происходит при относительно высоком напряжении — 3,7 вольт по сравнению с щелочной батареей AA при 1,5 вольт — поэтому литиевые батареи стали предпочтительным портативным источником питания для многих потребительских электронных устройств.
Литиевые батареи также входят в состав более крупных аккумуляторных блоков, таких как аккумулятор для ноутбука.Эти аккумуляторные блоки содержат ряд литий-ионных элементов, связанных в один более крупный компонент, и будут содержать ряд дополнительных компонентов:
- Датчик температуры : Датчик, отслеживающий температуру внутри упаковки, чтобы обеспечить безопасность и долговечность ячеек.
- Регулятор напряжения : Датчик и схема для контроля и регулирования выхода / емкости каждой ячейки внутри блока.
- Состояние заряда аккумулятора : Датчик, информирующий операционную систему о текущем состоянии заряда (например, 47% заряда)
- Разъем : Комплектный разъем для ноутбука, зависит от марки.
Литиевые батареи могут выполнить тысячи циклов заряда / разряда, прежде чем качество элемента начнет действительно ухудшаться, но есть несколько способов испортить батарею, потенциально подвергая себя опасности.
Обслуживание батареи
Положительный электрод, встречающийся в большинстве литиевых батарей, LiCoO 2 , может представлять ряд опасностей в случае повреждения элемента.В отличие от ряда других вариантов батарей, использование горючего компаунда под давлением может привести к экстремальным результатам. Чтобы смягчить это, элементы литиевых батарей подвергаются ряду тестов на безопасность, многие из которых более строгие, чем их аналоги на кислотной основе.
Тепло
Было несколько случаев воспламенения литиевых батарей в условиях экстремальной жары.Батареи под воздействием тепла в сочетании с любым дополнительным, неожиданным давлением или коротким замыканием могут «взорваться», оставив разрушенный аккумулятор и, чаще всего, поврежденный элемент портативной техники.
Каждая литиевая батарея имеет встроенный сепаратор внутри элемента.Это различает положительный и отрицательный электроды в процессе заряда / разряда. Если этот разделитель будет перфорирован или поврежден, существует вероятность контакта электродов. Это приводит к быстрому нагреву аккумулятора, что может привести к взрыву.
Батарея имеет вентиляционный механизм, чтобы предотвратить такое возникновение, но, в конечном счете, из-за природы удаляемого химического соединения, вероятность взрывной реакции все еще сохраняется из-за тепла, выделяемого химической реакцией.
Номинальные значения разрядки
Литиевые батареи предпочитают частичный разряд, а не «глубокий» или «полный».У них нет зарядной памяти, поэтому частичный разряд не повлияет на будущую производительность.
Однако «глубокая» разрядка i.е. полный разряд батареи вызовет падение напряжения литиевой батареи и может привести к необратимому повреждению батареи.
Процесс старения
Литиевые батареи стареют.Предполагается, что их максимальный срок службы составляет от 2 до 4 лет в зависимости от количества циклов заряда / разряда. Это не значит, что вам следует отслеживать количество раз, когда вы используете батарею, поскольку это было бы довольно сложно. Но отказ от использования новой батареи и оставление ее на полке не продлит срок службы батареи — батареи все равно прослужат те же 2-4 года.
Также стоит проверить, когда была произведена батарея, при покупке нового портативного технического продукта.Если он простаивал на складе в течение года, срок службы батареи уже истощился. Свяжитесь с производителем продукта и по возможности попросите новую батарею.
Существуют современные приложения для управления батареями, которые заявляют, что могут со временем обратить вспять текущую приемлемую деградацию ячеек, например, batteryOS, продукт, который будет запущен в феврале 2015 года.
Li-Air
В литиевых батареях следующего поколения будет использоваться химический состав литий-воздух, обеспечивающий чрезвычайно высокую плотность энергии во все более легких конструкциях.Литий-воздушные батареи получают преимущество в плотности энергии по сравнению с традиционными аналогами за счет использования большого количества кислорода для индукции тока, вместо того, чтобы хранить необходимый химический окислитель внутри.
К сожалению, до того, как коммерчески жизнеспособный продукт Li-Air появится в наших портативных устройствах, все еще необходимы исследования в ряде ключевых областей.
Помогло ли это вам понять батареи в ваших портативных устройствах? Дайте нам знать, что вы думаете ниже!
Кредиты на изображения: Батареи через Wikimedia Commons, Voltaic Pile через Wikimedia Commons, Литий-ионные батареи через Wikimedia Commons, Литий-полимерные батареи через Wikimedia Commons, 3GS со сломанной батареей через Wikimedia Commons, Пустая батарея через Pixabay, Плотность энергии батареи через Wikimedia Commons
Что такое Windows Core OS?Windows Core OS — это урезанная версия Windows, но заменит ли она WIndows 10?
Об авторе Гэвин Филлипс (Опубликовано 653 статей)Гэвин — младший редактор отдела Windows and Technology Explained, регулярный участник Really Useful Podcast и редактор дочернего сайта MakeUseOf, посвященного криптографии, Blocks Decoded.У него есть степень бакалавра (с отличием) в области современного письма с использованием методов цифрового искусства, разграбленных на холмах Девона, а также более десяти лет профессионального писательского опыта. Он любит много пить чая, настольные игры и футбол.
Ещё от Gavin PhillipsПодпишитесь на нашу рассылку новостей
Подпишитесь на нашу рассылку, чтобы получать технические советы, обзоры, бесплатные электронные книги и эксклюзивные предложения!
Еще один шаг…!
Подтвердите свой адрес электронной почты в только что отправленном вам электронном письме.
Battery Technologies — learn.sparkfun.com
Опции батарей
Доступно множество различных аккумуляторных технологий. Есть несколько действительно отличных ресурсов для мельчайших деталей химического состава батарей. Википедия особенно хороша и всеобъемлющая. В этом руководстве основное внимание уделяется наиболее часто используемым батареям для встроенных систем и электроники DIY.
Рекомендуемая литература
Есть некоторые концепции и знания, которые вы, возможно, захотите узнать перед чтением этого руководства:
Что такое схема?
Каждый электрический проект начинается со схемы. Не знаю, что такое схема? Мы здесь, чтобы помочь.
Что такое электричество?
Мы можем видеть электричество в действии на наших компьютерах, освещающее наши дома, как удары молнии во время грозы, но что это такое? Это непростой вопрос, но этот урок прольет на него некоторый свет!
Хотите изучить различные батареи?
Мы вас прикрыли!
Щелочная батарея 9 В
В наличии PRT-10218Это ваши стандартные щелочные батареи на 9 вольт от Rayovac.Даже не думайте пытаться перезарядить их. Используйте их с…
1Терминология
Вот несколько терминов, которые часто используются при разговоре об аккумуляторах.
Емкость — Батареи имеют разные номиналы в зависимости от количества энергии, которое может хранить данная батарея. Когда аккумулятор полностью заряжен, его емкость — это количество энергии, которое в нем содержится.Батареи одного типа часто оцениваются по величине тока, которую они могут выдавать с течением времени. Например, есть батареи емкостью 1000 мАч (миллиампер-час) и 2000 мАч.
Номинальное напряжение ячейки — Среднее напряжение, выводимое ячейкой при зарядке. Номинальное напряжение батареи зависит от химической реакции за ней. Свинцово-кислотный автомобильный аккумулятор выдает 12 В. Литиевая батарейка типа «таблетка» выдает 3 В.
Ключевым словом здесь является «номинальное», фактическое измеренное напряжение на аккумуляторе будет уменьшаться по мере его разряда.Полностью заряженный LiPo аккумулятор будет вырабатывать около 4,23 В, а в разряженном состоянии его напряжение может быть ближе к 2,7 В.
Форма — Батареи бывают разных размеров и форм. Термин «AA» относится к определенной форме и стилю ячейки. Есть большое разнообразие.
Первичная и вторичная — Первичные батареи синонимичны одноразовым . После полного опорожнения первичные элементы нельзя заряжать (надежно / безопасно). Вторичные батареи более известны как аккумуляторные .Для их полной резервной зарядки требуется другой источник питания, но они могут полностью заряжаться / разряжаться много раз в течение своего срока службы. Как правило, первичные батареи имеют более низкую скорость разряда, поэтому они служат дольше, но они могут быть менее экономичными, чем аккумуляторные батареи.
| Форма батареи | Химия | Номинальное напряжение | Перезаряжаемый? |
|---|---|---|---|
| AA, AAA, C и D | Щелочной или цинк-углеродный | 1.5В | Нет |
| 9V | Щелочной или угольно-цинковый | 9V | Нет |
| Ячейка для монет | Литий | 3V | Нет |
| Silver Flat Pack | Литий-полимерный (LiPo) | 3,7 В | Да |
| AA, AAA, C, D (перезаряжаемый) | NiMH или NiCd | 1,2 В | Да |
| Автомобильный аккумулятор | Шестиэлементный свинцово-кислотный | 12.6В | Есть |
Плотность энергии — Комбинируя емкость с формой и размером батареи, можно рассчитать плотность энергии батареи. Разные технологии допускают разную плотность. Например, литиевые батареи обычно содержат больше сока в заданном объеме, чем щелочные батареи или батарейки типа «таблетка».
Скорость внутреннего разряда — Вы когда-нибудь пытались завести машину, которая простаивает 6 месяцев? Батареи разряжаются, когда они лежат на полке или когда они не используются.Скорость, с которой батарея со временем разряжается, называется скоростью внутренней разрядки.
Безопасность — Поскольку батареи накапливают энергию, они представляют собой очень крошечные взрывчатые вещества. Чтобы предотвратить повреждение, батареи должны быть максимально безопасными. Большинство технологий аккумуляторов предназначены для безопасной разрядки в случае неправильного использования. Если вы неправильно подключите щелочную батарею, она может стать горячей на ощупь, но не должна загореться. Большинство литий-полимерных батарей имеют встроенные схемы безопасности, предотвращающие повреждение батареи и предотвращающие ее небезопасное использование.
Полный список терминов и технический обзор Википедия — [отличный ресурс] (http://en.wikipedia.org/wiki/Battery_ (электричество)).
Литий-полимерный
Литий-полимерные батареи(часто сокращенно LiPo) очень полезны для встроенной электроники. Они предлагают самую высокую плотность, доступную на рынке. Поскольку в сотовых телефонах преимущественно используются батареи этого типа, их легко найти по разумным ценам. Они от до требуют специальной зарядки, поэтому обязательно используйте правильное зарядное устройство для работы.SparkFun оснащен различными литий-полимерными батареями 3,7 В, многие из которых перечислены ниже. Емкость выбранной вами батареи будет зависеть от предполагаемого времени работы вашего проекта, ограничений по размеру и других факторов.
Номинальное напряжение
Индивидуальная ячейка LiPo имеет номинальное напряжение 3,7 В . При полной зарядке вы увидите почти 4,3 В на элементе, но при нормальном использовании оно быстро упадет до 3,7 В. Когда батарея разряжена, она будет около 3 В. Это означает, что ваш проект должен будет обрабатывать различные напряжения, если вы работаете непосредственно от ячейки.Если вам нужно 5 В, вам нужно будет соединить два LiPos последовательно, чтобы создать блок на 7,4 В и стабилизировать его до 5 В.
Разъемы
В мире малогабаритной электроники большинство литий-полимерных аккумуляторов имеют различные 2-контактные разъемы. В SparkFun мы используем разъем JST . Это предотвращает неправильное подключение аккумулятора. Разъем имеет фрикционную посадку, поэтому для аккуратного извлечения аккумулятора часто используются плоскогубцы.
Зарядка и разрядка
Для зарядки LiPo аккумуляторов создано множество недорогих зарядных устройств.Обычно они используют USB для зарядки аккумулятора. Не пытайтесь заряжать LiPos без зарядного устройства. Аккумулятор LiPo может быть поврежден из-за перезарядки, поэтому используйте специально разработанное зарядное устройство LiPo, например, здесь:
Перед зарядкой литий-ионного аккумулятора убедитесь, что вы знаете его емкость и ток заряда, подаваемый зарядным устройством. Дополнительную информацию можно найти в следующем руководстве:
Что такое батарея? — learn.sparkfun.com
Добавлено в избранное Любимый 20Введение
Батареи представляют собой совокупность одной или нескольких ячеек, химические реакции которых создают поток электронов в цепи.Все батареи состоят из трех основных компонентов: анода (сторона «-»), катода (сторона «+») и какого-то электролита (вещество, которое химически реагирует с анодом и катодом).
Когда анод и катод батареи подключены к цепи, между анодом и электролитом происходит химическая реакция. Эта реакция заставляет электроны проходить через цепь и обратно к катоду, где происходит другая химическая реакция.Когда материал в катоде или аноде расходуется или больше не может быть использован в реакции, батарея не может производить электричество. В этот момент ваша батарея «разряжена».
Батареи, которые необходимо выбросить после использования, известны как первичные батареи . Аккумуляторы, которые можно перезаряжать, называются вторичными батареями и .
Литий-полимерные батареи, например, заряжаемые
Без батарей ваш квадрокоптер пришлось бы привязать к стене, вам пришлось бы вручную заводить машину, а ваш контроллер Xbox должен был бы быть постоянно подключен к розетке (как в старые добрые времена).Батареи позволяют хранить потенциальную электрическую энергию в переносном контейнере.
Батареи бывают разных форм, размеров и химического состава.
Изобретение современной батареи часто приписывают Алессандро Вольта. На самом деле все началось с удивительной аварии, связанной с рассечением лягушки.
Что вы узнаете
В этом руководстве будут подробно рассмотрены следующие темы:
- Как были изобретены батарейки
- Из каких частей состоит аккумулятор
- Как работает аккумулятор
- Общие термины, используемые для описания батарей
- Различные способы использования батарей в схемах
Рекомендуемая литература
Есть несколько концепций, с которыми вы, возможно, захотите ознакомиться перед тем, как начать читать это руководство:
Хотите изучить различные батареи?
Мы вас прикрыли!
Щелочная батарея 9 В
В наличии PRT-10218Это ваши стандартные щелочные батареи на 9 вольт от Rayovac.Даже не думайте пытаться перезарядить их. Используйте их с…
1История
Термин Батарея
Исторически слово «батарея» использовалось для описания «серии подобных объектов, сгруппированных вместе для выполнения определенной функции», как в случае артиллерийской батареи. В 1749 году Бенджамин Франклин впервые использовал этот термин для описания серии конденсаторов, которые он соединил вместе для своих экспериментов с электричеством.Позже этот термин будет использоваться для любых электрохимических ячеек, соединенных вместе с целью обеспечения электроэнергии.
Батарея «конденсаторов» Лейденской банки, соединенная вместе(Изображение любезно предоставлено Альвинруном из Wikimedia Commons)
Изобретение батареи
В один роковой день 1780 года итальянский физик, врач, биолог и философ Луиджи Гальвани вскрыл лягушку, прикрепленную к медному крючку. Когда он коснулся лягушачьей лапы железным ножом, нога дернулась.Гальвани предположил, что энергия исходит от самой ноги, но его коллега-ученый Алессандро Вольта считал иначе.
Вольта предположил, что импульсы лягушачьей лапки на самом деле вызываются разными металлами, пропитанными жидкостью. Он повторил эксперимент, используя ткань, пропитанную рассолом, вместо трупа лягушки, что привело к аналогичному напряжению. Вольта опубликовал свои выводы в 1791 году, а позже создал первую батарею, гальваническую батарею, в 1800 году.
Гальваническая свая состояла из набора цинковых и медных пластин, разделенных тканью, пропитанной рассолом
СтопкаVolta страдала от двух основных проблем: из-за ее веса электролит вытекал из ткани, а особые химические свойства компонентов приводили к очень короткому сроку службы (около часа).Следующие двести лет уйдут на совершенствование конструкции Вольты и решение этих проблем.
Исправления в гальванической куче
Уильям Круикшанк из Шотландии решил проблему утечки, положив гальваническую батарею на бок, чтобы сформировать «желобную батарею».
Лотковая батарея решила проблему утечки гальванической сваи
Вторая проблема, короткий срок службы, была вызвана разложением цинка из-за примесей и скоплением пузырьков водорода на меди.В 1835 году Уильям Стерджен обнаружил, что обработка цинка ртутью предотвратит разложение.
Британский химик Джон Фредерик Дэниелл использовал второй электролит, который вступал в реакцию с водородом, предотвращая накопление на медном катоде. Батарея Даниэля с двумя электролитами, известная как «ячейка Даниэля», станет очень популярным решением для обеспечения энергией зарождающихся телеграфных сетей.
Коллекция клеток Даниэля из 1836 г.
Первая аккумуляторная батарея
В 1859 году французский физик Гастон Планте создал батарею из двух прокатанных листов свинца, погруженных в серную кислоту.Путем изменения направления электрического тока через батарею химический состав вернется в исходное состояние, создав первую перезаряжаемую батарею.
Позже, в 1881 году, Камилла Альфонс Фор улучшила конструкцию Планте, превратив листы свинца в пластины. Эта новая конструкция упростила производство аккумуляторов, и свинцово-кислотные аккумуляторы получили широкое распространение в автомобилях.
-> Дизайн обычного «автомобильного аккумулятора» существует уже более 100 лет
(Изображение любезно предоставлено Эмилианом Робертом Виколом из Wikimedia Commons) <-
Сухая камера
Вплоть до конца 1800-х годов электролит в батареях был в жидком состоянии.Это сделало транспортировку аккумуляторов очень осторожным делом, и большинство аккумуляторов никогда не предназначались для перемещения после подключения к цепи.
В 1866 году Жорж Лекланше создал батарею, используя цинковый анод, катод из диоксида марганца и раствор хлорида аммония в качестве электролита. Хотя электролит в элементе Лекланше был все еще жидким, химический состав батареи оказался важным шагом для изобретения сухого элемента.
Карл Гасснер придумал, как создать электролитную пасту из хлорида аммония и гипса.Он запатентовал новую батарею «сухих элементов» в 1886 году в Германии.
Эти новые сухие элементы, обычно называемые «угольно-цинковыми батареями», производились массово и пользовались огромной популярностью до конца 1950-х годов. Хотя углерод не используется в химической реакции, он играет важную роль в качестве электрического проводника в углеродно-цинковой батарее.
-> Цинк-угольная батарея 3 В 1960-х годов
(Изображение любезно предоставлено PhFabre из Wikimedia Commons) <-
В 1950-х годах Льюис Урри, Пол Марсал и Карл Кордеш из компании Union Carbide (позже известной как «Eveready», а затем «Energizer») заменили электролит хлористого аммония щелочным веществом на основе химического состава батареи, сформулированного Вальдемаром. Юнгнер в 1899 году.Щелочные батареи с сухими элементами могут содержать больше энергии, чем угольно-цинковые батареи того же размера, и имеют более длительный срок хранения.
Щелочные батареи приобрели популярность в 1960-х годах, обогнали угольно-цинковые батареи и с тех пор стали стандартными первичными элементами для потребительского использования.
-> Щелочные батареи бывают разных форм и размеров
(Изображение любезно предоставлено Aney ~ commonswiki из Wikimedia Commons) <-
Аккумуляторы 20-го века
В 1970-х годах компания COMSAT разработала никель-водородную батарею для использования в спутниках связи.Эти батареи хранят водород в газообразной форме под давлением. Многие искусственные спутники, такие как Международная космическая станция, по-прежнему используют никель-водородные батареи.
Исследования нескольких компаний с конца 1960-х годов привели к созданию никель-металлгидридной (NiMH) батареи. NiMH батареи были выпущены на потребительский рынок в 1989 году и стали более дешевой альтернативой никель-водородным аккумуляторным элементам меньшего размера.
Asahi Chemical из Японии построила первую литий-ионную батарею в 1985 году, а Sony создала первую коммерческую литий-ионную батарею в 1991 году.В конце 1990-х годов был создан мягкий гибкий корпус для литий-ионных аккумуляторов, в результате чего появилась «литий-полимерная» или «LiPo» батарея.
Химические реакции в литий-полимерной батарее практически такие же, как и в литий-ионной батарее
Очевидно, что было изобретено, произведено и устарело гораздо больше химических элементов батарей. Если вы хотите узнать больше о современных и популярных технологиях аккумуляторов, ознакомьтесь с нашим руководством по технологиям аккумуляторов.
Компоненты
Батареисостоят из трех основных компонентов: анода , катода и электролита . Сепаратор часто используется для предотвращения соприкосновения анода и катода, если электролита недостаточно. Для хранения этих компонентов аккумуляторы обычно имеют какой-то кожух .
Хорошо, большинство батарей на самом деле не разделены на три равные части, но вы поняли.Лучшее поперечное сечение щелочной ячейки можно найти в Википедии.И анод, и катод относятся к типу электродов . Электроды — это проводники, через которые электричество входит или выходит из компонента в цепи.
Анод
Электроны выходят из анода в устройстве, подключенном к цепи. Это означает, что обычный «ток» течет в анод.
На аккумуляторах анод отмечен как отрицательная (-) клемма
В батарее химическая реакция между анодом и электролитом вызывает накопление электронов на аноде.Эти электроны хотят двигаться к катоду, но не могут пройти через электролит или сепаратор.
Катод
Электроны текут в катод в устройстве, подключенном к цепи. Это означает, что обычный «ток» проходит от катода .
На батареях катод помечен как положительный (+) вывод
В батареях в химической реакции внутри катода или вокруг него используются электроны, образующиеся на аноде.Электроны могут попасть на катод только через цепь, внешнюю по отношению к батарее.
Электролит
Электролит — это вещество, часто жидкость или гель, которое способно переносить ионы между химическими реакциями, происходящими на аноде и катоде. Электролит также препятствует потоку электронов между анодом и катодом, так что электроны легче проходят через внешнюю цепь, чем через электролит.
-> В щелочных батареях может протекать электролит, гидроксид калия, если они подвергаются воздействию высоких температур или обратного напряжения
(Изображение любезно предоставлено Wiliam Davies из Wikimedia Commons) <-
Электролит имеет решающее значение в работе аккумулятора.Поскольку электроны не могут проходить через него, они вынуждены проходить через электрические проводники в виде цепи, соединяющей анод с катодом.
Сепаратор
Сепараторы представляют собой пористые материалы, которые предотвращают соприкосновение анода и катода, что может вызвать короткое замыкание в батарее. Сепараторы могут быть изготовлены из различных материалов, включая хлопок, нейлон, полиэстер, картон и синтетические полимерные пленки. Сепараторы не вступают в химическую реакцию ни с анодом, ни с катодом, ни с электролитом.
В гальванической куче использовалась ткань или картон (разделитель), пропитанные рассолом (электролитом), чтобы электроды разнесены
Ионы в электролите могут быть положительно заряженными, отрицательно заряженными и иметь различные размеры. Могут быть изготовлены специальные сепараторы, которые пропускают одни ионы, но не пропускают другие.
Кожух
Для большинства аккумуляторов требуется способ удержания их химических компонентов. Кожухи, также известные как «кожухи» или «оболочки», представляют собой просто механические конструкции, предназначенные для удержания внутренних компонентов батареи.
Свинцово-кислотный аккумулятор в пластиковом корпусе
Корпуса батареймогут быть изготовлены практически из чего угодно: из пластика, стали, чехлов из мягкого полимерного ламината и так далее. В некоторых батареях используется токопроводящий стальной кожух, который электрически соединен с одним из электродов. В случае обычного щелочного элемента AA стальной кожух соединен с катодом.
Операция
Аккумуляторы обычно требуют нескольких химических реакций для работы.По крайней мере, одна реакция происходит внутри анода или вокруг него, и одна или несколько реакций происходят внутри или вокруг катода. Во всех случаях реакция на аноде дает дополнительные электроны в процессе, называемом окислением , а реакция на катоде использует дополнительные электроны во время процесса, известного как восстановление .
Когда переключатель замкнут, цепь замыкается, и электроны могут течь от анода к катоду. Эти электроны активируют химические реакции на аноде и катоде.
По сути, мы разделяем определенный вид химической реакции, реакцию восстановления-окисления или окислительно-восстановительную реакцию, на две отдельные части. Окислительно-восстановительные реакции происходят при переносе электронов между химическими веществами. Мы можем использовать движение электронов в этой реакции, чтобы они выходили за пределы батареи и питали нашу цепь.
Анодное окисление
Эта первая часть окислительно-восстановительной реакции, окисление, происходит между анодом и электролитом и производит электроны (обозначенные как e — ).
Некоторые реакции окисления образуют ионы, например, в литий-ионной батарее. В других химических реакциях расходуются ионы, как в обычных щелочных батареях. В любом случае ионы могут свободно проходить через электролит, а электроны — нет.
Катодное восстановление
Другая половина окислительно-восстановительной реакции, восстановление, происходит в катоде или рядом с ним. Электроны, образующиеся в результате реакции окисления, расходуются во время восстановления.
В некоторых случаях, например, в литий-ионных батареях, положительно заряженные ионы лития, образующиеся во время реакции окисления, расходуются во время восстановления.В других случаях, например, в щелочных батареях, во время восстановления образуются отрицательно заряженные ионы.
Электронный поток
В большинстве аккумуляторов некоторые или все химические реакции могут происходить, даже если аккумулятор не подключен к цепи. Эти реакции могут повлиять на срок годности батареи.
По большей части, реакции будут происходить с полной силой только тогда, когда между анодом и катодом замыкается электрически проводящая цепь. Чем меньше сопротивление между анодом и катодом, тем больше электронов может течь и тем быстрее протекают химические реакции.
Короткое замыкание в аккумуляторе (в данном случае даже случайное) может быть опасным. Известно, что литий-ионные батареи перегреваются и даже задыхаются или загораются при коротком замыкании.
Мы можем пропускать эти движущиеся электроны через различные электрические компоненты, известные как «нагрузка», чтобы достичь чего-то полезного. В анимационном ролике в начале этого раздела мы зажигаем виртуальную лампочку движущимися электронами.
Разряженная батарея
Химические вещества в аккумуляторе в конечном итоге достигают состояния равновесия. В этом состоянии химические вещества больше не будут реагировать, и в результате аккумулятор больше не будет генерировать электрический ток. На данный момент аккумулятор считается «мертвым».
Первичные элементы необходимо утилизировать, когда батарея разряжена. Вторичные элементы можно перезаряжать, и это достигается путем подачи через батарею обратного электрического тока.Перезарядка происходит, когда химические вещества выполняют еще одну серию реакций, чтобы вернуть их в исходное состояние.
Терминология
Люди часто используют общий набор терминов, говоря о напряжении батареи, емкости, возможности источника тока и так далее.
Ячейка
Элемент относится к одному аноду и катоду, разделенным электролитом, используемым для выработки напряжения и тока. Батарея может состоять из одной или нескольких ячеек.Например, одна батарея AA — это одна ячейка. Автомобильные аккумуляторы содержат шесть ячеек по 2,1 В.
Обычная 9-вольтовая батарея содержит шесть щелочных элементов по 1,5 В, установленных друг над другом
Первичный
Первичные клетки содержат химический состав, который нельзя обратить вспять. В результате аккумулятор необходимо выбрасывать после того, как он разрядился.
Среднее
Вторичные элементы можно перезаряжать, и их химический состав возвращается в исходное состояние.Эти элементы, также известные как «аккумуляторные батареи», можно использовать много раз.
Номинальное напряжение
Номинальное напряжение аккумулятора — это напряжение, указанное производителем.
Например, щелочные батареи АА имеют напряжение 1,5 В. В этой статье Mad Scientist Hut показано, что их испытанные щелочные батареи начинаются с напряжения около 1,55 В, а затем медленно теряют напряжение по мере разряда. В этом примере номинальное напряжение «1,5 В» относится к максимальному или пусковому напряжению батареи.
Этот аккумулятор Storm для квадрокоптеров показывает кривую разряда для их LiPo-элементов, начиная с 4,2 В и снижаясь до 2,8 В при разряде. Номинальное напряжение, указанное для большинства литий-ионных и LiPo-элементов, составляет 3,7 В. В этом случае номинальное напряжение «3,7 В» относится к среднему напряжению аккумулятора в течение его цикла разряда.
Вместимость
Емкость аккумулятора — это величина электрического заряда, который он может доставить при определенном напряжении. Большинство аккумуляторов рассчитаны на ампер-часы (Ач) или миллиампер-часы (мАч).
Этот LiPo аккумулятор рассчитан на 1000 мАч, что означает, что он может обеспечить 1 ампер в течение 1 часа, прежде чем он будет считаться разряженным.
Большинство графиков разряда батареи показывают напряжение батареи как функцию от емкости, например, эти тесты батареи AA, проведенные PowerStream. Чтобы выяснить, достаточно ли емкости аккумулятора для питания вашей схемы, найдите самое низкое допустимое напряжение и найдите соответствующий номинал мАч или Ач.
C-скорость
Многие батареи, особенно мощные литий-ионные, обозначают ток разряда как «C-Rate», чтобы более четко определить характеристики батареи.C-Rate — это скорость разряда относительно максимальной емкости аккумулятора.
1С — это количество тока, необходимое для разрядки аккумулятора за 1 час. Например, батарея емкостью 400 мАч, обеспечивающая ток 1С, будет обеспечивать 400 мА. 5C для той же батареи будет 2 A.
Большинство батарей теряют емкость при повышенном потреблении тока. Например, этот график информации о продукте от Chargery показывает, что их LiPo-элемент имеет меньше мАч при более высоких показателях C-Rates.
ПРИМЕЧАНИЕ: Общий совет гласит, что вы должны заряжать LiPo батареи при 1С или меньше.
У Массачусетского технологического института есть фантастическое руководство по спецификациям и терминологии батарей, которое идет намного дальше этого обзора.
Использование
Однокамерный
Некоторые схемы могут питаться от одного элемента, но убедитесь, что батарея может обеспечивать достаточное напряжение и ток.
Этот экран для фотонной батареи питается от одного элемента LiPoЕсли напряжение слишком высокое или слишком низкое для вашей схемы, вам, вероятно, понадобится преобразователь постоянного тока в постоянный.
серии
Чтобы увеличить напряжение между выводами батареи, вы можете расположить элементы последовательно. Последовательность означает штабелирование ячеек встык, соединение анода одного с катодом следующего.
Последовательно соединяя батареи, вы увеличиваете общее напряжение. Сложите напряжение всех ячеек, чтобы определить рабочее напряжение. Емкость остается прежней.
В этом примере четыре ячейки на 1,5 В соединены последовательно.Напряжение на нагрузке составляет 6 В, а общий набор аккумуляторов имеет емкость 2000 мАч.
В большинстве бытовых электронных устройств, в которых используются щелочные батареи, батареи устанавливаются последовательно. Например, этот держатель батареек 2x AA может поднять номинальное напряжение до 3 В для проекта.
ПРИМЕЧАНИЕ: Если вы заряжаете литий-ионные или LiPo аккумуляторы последовательно, вам необходимо использовать специальные схемы, известные как «балансир», чтобы гарантировать, что напряжения между элементами остаются одинаковыми.Некоторые зарядные устройства, такие как это, имеют балансиры для безопасной зарядки.Параллельный
Если напряжение отдельного элемента соответствует нагрузке, вы можете добавить батареи параллельно, чтобы увеличить емкость. Обратите внимание, что это также означает увеличение доступного тока (C-Rate).
Будьте осторожны при параллельном подключении аккумуляторов! Все элементы должны иметь одинаковое номинальное напряжение и одинаковый уровень заряда. Если есть какая-либо разница в напряжении, может произойти короткое замыкание, что приведет к перегреву и, возможно, возгоранию.
В этом примере четыре ячейки 1,5 В подключены параллельно. Напряжение на нагрузке остается на уровне 1,5 В, но общая емкость увеличивается до 8000 мАч.
серии и параллельный
Если вы хотите увеличить напряжение и емкость, вы можете комбинировать последовательные и параллельные батареи. Еще раз убедитесь, что уровень напряжения одинаков для батарей, включенных параллельно, поскольку может произойти короткое замыкание.
В этом примере полное напряжение на нагрузке составляет 3 В, а общая емкость аккумуляторов составляет 4000 мАч.
В больших аккумуляторных блоках, особенно литий-ионных, вы часто видите конфигурацию, указанную с использованием «S» и «P» для последовательного и параллельного подключения. Конфигурация схемы выше — 2S2P. В качестве практического примера современные электромобили используют массивные массивы батарей, соединенных последовательно и параллельно.
Ресурсы и дальнейшее развитие
К настоящему времени вы должны понимать, как были изобретены батарейки и как они работают. Батареи — это один из способов обеспечения вашего проекта электроэнергией, и они могут быть невероятно полезны, если вам нужен портативный источник питания.
Если вы хотите больше узнать о батареях, вот еще несколько уроков:
Хотите увидеть аккумуляторы в действии? Взгляните на эти проекты, в которых используются разные батареи в разных конфигурациях:
Simon Splosion Wireless
Это учебное пособие, демонстрирующее один из многих методов «взлома» Саймона Сэйса. Мы выделим технику, чтобы взять ваш Simon Says Wireless.
Как заменить батарею CMOS
Обновлено: 30.06.2020, Computer Hope
Существует несколько причин, по которым батарею CMOS необходимо заменить в вашем компьютере.На этой странице представлена информация о том, почему вам может понадобиться замена, и шаги по ее устранению.
Почему мне нужно заменить батарею CMOS?
- Компьютер теряет настройки времени или даты.
- При загрузке компьютера отображается сообщение об ошибке или предупреждение, подобное приведенному ниже.
- Ошибка чтения CMOS
- Ошибка контрольной суммы CMOS
- Отказ батареи CMOS
- Низкое напряжение аккумуляторной батареи системы
Если возникнут какие-либо проблемы или сообщения, указанные выше, вероятно, потребуется заменить батарею CMOS.Процесс его замены подробно описан в следующих разделах.
Найдите аккумулятор CMOS
ОсторожноНаходясь внутри компьютера, убедитесь, что вы знаете об электростатическом разряде и его опасностях.
Откройте корпус компьютера и найдите аккумулятор на материнской плате. Убедитесь, что он доступен и может быть удален. Сегодня в большинстве компьютеров используется батарея CMOS типа «таблетка», такая как батарея CR2032, показанная на рисунке.
НаконечникНекоторые батареи CMOS могут удерживаться металлическим зажимом или стержнем.Батарею можно извлечь, вытащив ее из-под зажима. Не сгибайте этот зажим, чтобы вытащить аккумулятор, так как изгиб зажима может привести к тому, что новый аккумулятор не останется в гнезде.
Если вы не можете найти батарею CMOS, обратитесь к документации материнской платы или обратитесь к производителю компьютера. Если у вас больше нет документации к материнской плате, скорее всего, вы сможете найти ее в Интернете.
ЗаписьНа некоторых компьютерах вам может потребоваться отсоединить кабели, отсоединить диски или другие части компьютера, чтобы получить полный доступ к батарее CMOS.
Получить информацию о батарее
К сожалению, большинство производителей не указывают точный тип и модель батареи CMOS. После того, как вы нашли аккумулятор, мы рекомендуем вам записать его характеристики (напряжение, химический состав, проводка). Если возможно, извлеките аккумулятор и отнесите его в магазин.
НаконечникДля большинства компьютеров модель аккумулятора — CR2032 .
Извлечение аккумулятора
Если в вашем компьютере используется батарейка типа «таблетка», извлечь батарею относительно просто.Возьмитесь пальцами за край аккумулятора и вытащите его из гнезда, удерживая на месте. На некоторых материнских платах есть зажим, удерживающий аккумулятор. Если на материнской плате вашего компьютера есть этот зажим, возможно, вам придется одной рукой поднять зажим, а другой рукой вытащить аккумулятор.
ОсторожноНаходясь внутри компьютера, убедитесь, что вы знаете об электростатическом разряде и всех его потенциальных опасностях.
К сожалению, не все батареи CMOS съемные. Некоторые производители разрешают добавлять только сменную батарею.Если в вашем компьютере нет батарейки типа «таблетка», обратитесь к документации или обратитесь к производителю компьютера за дополнительной помощью.
Если на материнской плате вашего компьютера нет съемного аккумулятора, вам необходимо установить перемычку на материнской плате, чтобы установить новый аккумулятор.
Вставьте новую батарею
После покупки нового аккумулятора удалите старый аккумулятор и замените его новым. Некоторые компьютеры могут не иметь съемной батареи, так как эти компьютеры вставляют новую батарею в гнездо вторичной батареи на материнской плате.
Введите значения CMOS
После замены батареи включите компьютер и сбросьте значения CMOS на значения по умолчанию. После ввода всех значений убедитесь, что сохранили настройки перед выходом. Многие настройки CMOS позволяют вам нажать клавишу, например F10, для сохранения значений и выхода одним действием.
Неисправное оборудование
Если вы продолжаете получать сообщение об ошибке после выполнения всех вышеперечисленных шагов, это признак более серьезной проблемы. Наиболее вероятные причины — плохой блок питания или неисправная материнская плата.Возможно, вам придется заменить блок питания или материнскую плату, чтобы решить эту проблему. На этом этапе мы рекомендуем отнести ваш компьютер в мастерскую по ремонту компьютеров, чтобы они диагностировали проблему.
Аккумулятор Dell не может быть идентифицирован
Предупреждение: аккумулятор не может быть идентифицирован. Эта система не сможет зарядить эту батарею, нажмите любую кнопку, чтобы продолжить ».
Это сообщение чаще всего встречается в линейке ноутбуков Dell Inspiron, причем больше всего сообщений об ошибках поступает от inspiron 1501, inspiron 3521, inspiron 5521, но другие пользователи Dell также сообщали об этом на других ноутбуках.
Это неприятно, когда ноутбук dell не распознает собственную батарею. Особенно если это оригинальный аккумулятор.
В этом нет смысла.
Есть несколько способов исправить это, в зависимости от того, в чем именно проблема. Обычно это либо аккумулятор, либо зарядное устройство, либо конфигурация Dell Bios, либо, если вам повезет, ноутбук, временно не считывающий чип зарядного устройства.
Следующие решения применимы к любому ноутбуку Dell, будь то Vostro, Latitude или Inspiron.
Неисправный аккумулятор не может быть идентифицирован
Если проблема заключается в батарее, вы можете купить батарею Dell по дешевке здесь или получить ее на Amazon. Убедитесь, что вы ищете батарею именно той модели вашего ноутбука, иначе вы перестанете причинять себе больше вреда.
Если у вас есть кто-то с такой же моделью, вы можете проверить аккумулятор, чтобы увидеть, не связана ли проблема с аккумулятором. Поменяйте местами батареи и загрузите ноутбук и посмотрите, все ли говорит, что батарея не может быть идентифицирована. Если сообщение об ошибке исчезло, значит, вы точно знаете, что вам нужна замена батареи.
Закажите один по указанной выше ссылке и замените неисправный аккумулятор.
Блошиное питание или принудительное отключение
Еще одно решение было бы сделать блошиный слив питания.
Как ни назовут это технические специалисты, высвобождение блошиного питания, принудительное завершение работы или принудительное завершение работы действительно решает множество проблем.
Обычно вы нажимаете и удерживаете кнопку питания около 15 секунд, а затем перезагружаете компьютер.
Я бы порекомендовал сначала отключить зарядное устройство адаптера переменного тока, вынув аккумулятор.Затем нажмите и удерживайте кнопку питания в течение 15 секунд.
То, что это делает, истощает остаточную мощность, которая остается на материнской плате, даже когда компьютер выключен и отсоединен от источника питания.
После этого подключите зарядное устройство и посмотрите, распознает ли компьютер зарядное устройство и сможет ли ноутбук загрузиться только от зарядного устройства.
Исправление зарядного устройства
Примеры поврежденного адаптера переменного тока DellТеперь это важно.
Если зарядное устройство деформировано, изношено или поцарапано, как показано на фотографиях выше, просто купите другое.
Они дешевые. Менее 20 баксов. Тут не о чем думать.
Рисковать не стоит.
Сломанная головка зарядного устройства может дорого обойтись вашей материнской плате. Это доставляет вам больше головной боли и стоит больше денег, чем если бы вы купили подходящее зарядное устройство.
Зарядные устройстватакже могут вызывать сообщения об ошибках и не заряжать ноутбук. Я также писал об этом ранее, что делать, если ноутбук подключен, но не заряжается
. Зарядные устройства Dellимеют чип, который используется в ноутбуках для определения подлинности аккумулятора Dell для данной модели.Так что, если чип выходит из строя, его больше не идентифицируют. Вот почему вы получаете сообщения об ошибках, подобные приведенным выше, если покупаете зарядные устройства в сомнительных местах.
Опять же, если у вас есть доступ к другому зарядному устройству той же модели, поменяйте их местами. Затем проверьте и посмотрите, решает ли это проблему.
Обновление BIOS для Dell
Еще один вариант для технических вопросов, обновление BIOS также может решить проблему и заставить ваш ноутбук распознавать аккумулятор.
Подождите, а как обновить биос, если ноутбук не распознает батарею? Что ж, вам нужно использовать командную строку.Ноутбук Dell не обновляет BIOS, если аккумулятор не распознается. Это сделано для того, чтобы вы не сломали ноутбук. Если вы отключите питание во время обновления BIOS, вы можете серьезно повредить свой компьютер.
Однако через командную строку вы можете принудительно обновить BIOS. Вот статья об обновлении BIOS.
Для принудительного обновления BIOS без батареи нажмите клавишу F1, чтобы продолжить, когда появится сообщение об ошибке «батарея не распознана».
Используйте другой компьютер с доступом в Интернет, чтобы загрузить последнюю версию BIOS.Чтобы убедиться, что вы загрузили правильное обновление BIOS, используйте сервисную метку Dell, чтобы идентифицировать ваш ноутбук.
Обновление Dell BIOS до более новой версииЕсли вам удалось получить другую батарею, которая заряжена более чем на 20%, установите загруженный файл BIOS. Чтобы установить, щелкните файл правой кнопкой мыши и запустите от имени администратора, следуя инструкциям по установке.
Если вам нужно принудительно установить BIOS без зарядки аккумулятора, сделайте следующее.
- Скопируйте файл, который вы загружаете, в каталог, который вы можете легко ввести, чтобы избежать ошибки при вводе
- Запустить командную строку в административном режиме
- введите имя файла, например E840A12.exe, затем добавьте / forceit после конца. Он должен выглядеть как E840A12.exe / forceit (замените имя файла на имя загруженного вами файла BIOS.
- Дождитесь установки обновления.
- После завершения обновления перезагрузите ноутбук и посмотрите, идентифицирован ли аккумулятор и заряжается.
Заключительная записка
Итак, если система не заряжает аккумулятор, потому что он не может идентифицироваться, проверьте
- Батарея в случае необходимости замены
- Зарядное устройство для адаптера переменного тока
- Блошиный питание, сток
- обновить BIOS
Надеюсь, это не проблема материнской платы, так как она выходит за рамки данной статьи.
Если вам удалось решить проблему, оставьте комментарий ниже и поделитесь, что сработало для вас, так как это может быть полезно для кого-то еще, у кого такая же головная боль
.
 Ежемесячно необходим 100% заряд батареи
Ежемесячно необходим 100% заряд батареи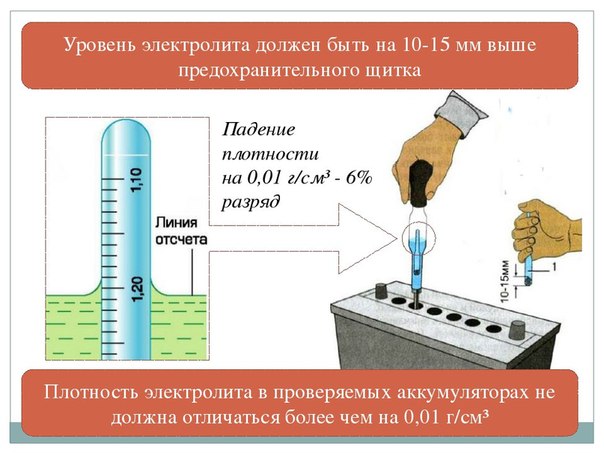
 Нормальным считается уровень, выше верхнего края пластин на 15-20 мм.
Нормальным считается уровень, выше верхнего края пластин на 15-20 мм.