Неисправности аккумуляторов | Эко Технологии
Из-за неправильного ухода и обслуживания, аккумуляторная батарея может выйти из строя. Неисправности и методы их устранения у тяговых и стартерных аккумуляторов аналогичны. Рассмотрим основные признаки поломок аккумуляторов и способы их устранения.
1. СульфатацияПризнаки:
Повышено напряжение на аккумуляторах в начале зарядки. Низкая плотность электролита к концу зарядки, не достаточная ёмкость. На пластинах образуется крупный кристаллический серно-кислый свинец, вследствие этого аккумулятор не принимает ток.
Причины:
- Нерегулярная и недостаточная зарядка во время эксплуатации.
- Простой в разряженном состоянии.
- Эксплуатация при низком уровне электролита.
- Доливка электролита, вместо дистиллированной воды.
- Эксплуатация при высоких температурах.
Что делать?
Неглубокая сульфатация устраняется при помощи нескольких выравнивающих зарядов. При глубокой сульфатации проводятся более трудоёмкие работы, они описаны в каждом паспорте аккумулятора. Но процесс сульфатации необратим, поэтому в скором времени придется менять аккумулятор.
При глубокой сульфатации проводятся более трудоёмкие работы, они описаны в каждом паспорте аккумулятора. Но процесс сульфатации необратим, поэтому в скором времени придется менять аккумулятор.
Признаки:
Плотность электролита не увеличивается во время зарядки. Высокая температура электролита и сильное отделение газов в неисправных аккумуляторах. Систематическое снижение плотности электролита в неисправном аккумуляторе при неполном коротком замыкании.
Причины:
В аккумуляторе может произойти короткое замыкание, связанное с осыпанием активной массы и разрушением свинцовой основы сепараторов.
Что делать?
В этом случае Вам лучше купить новый аккумулятор. Неустранимый дефект.
3. Повышенная саморазрядка аккумулятораПризнаки:
Аккумулятор быстро разряжается. Быстрое снижение напряжения и плотности электролита в неработающей батарее.
Причины:
Причиной быстрого саморазряда аккумулятора может быть либо загрязнение аккумуляторной батареи, либо загрязнение электролита.
Что делать?
В этом случае Вам надо протереть насухо контактные части аккумулятора, проверить чистоту электролита, по результату заменить электролит на новый.
Признаки:
Отсутствие напряжения на полюсных выводах или между отдельными аккумуляторами.
Причины:
Дефект сварки полюсного вывода или соединителя между аккумуляторами. Плохой контакт у болтовых соединений в результате плохой затяжки с неподходящим моментом вращения.
Что делать?
Новая сварка. Дополнительное затягивание болтовых соединений и проверка динамометрическим ключом.
5. Смена полярности аккумулятораПризнаки:
Пониженное общее напряжение аккумуляторной батареи. Глубокая разрядка батареи без интервалов для восстановления. Отделение газов из аккумуляторов.
Глубокая разрядка батареи без интервалов для восстановления. Отделение газов из аккумуляторов.
Причины:
Неправильная связь с токовыпрямителем.
Что делать?
Трудноустранимый дефект. Рекомендуется замена аккумуляторной батареи.
6. Сильное окисление полюсных клемм аккумулятораПризнаки:
Напряжение на выводах батареи есть, а стартер не крутится. Клеммы греются. Это приводит к прекращению подачи тока или увеличению сопротивления в цепи, что может вывести из строя всю электрику.
Причины:
Не проводилась очистка полюсных клемм.
Что делать?
Необходимо снять клеммы и зачистить их, а также зачистить выводные штыри аккумулятора, потом поставить все на место, проверить надежность крепления клемм. Клемма должна крепко сидеть на штырях и не двигаться, затем сверху смазать клеммы техническим вазелином или его заменителем.
Как зарядить аккумулятор автомобиля Рено Логан
Очищаем, обслуживаем и заряжаем аккумуляторную батарею…
Приветствуем автолюбителей в автоблоге AAuhadullin.
Для очистки корпуса АКБ предварительно приготовил содовый раствор, растворив в воде чайную ложку соды. Такой раствор нейтрализует кислоту на пластиковом корпусе, исключая поверхностный саморазряд аккумулятора. Проверить это можно с помощью мультиметра в режиме постоянного напряжения, установив щупы прибора, между одним из свинцовых выводов и корпусом. Если корпус чист, то напряжение на приборе будет отсутствовать.
Предварительно снимаем клеммы со свинцовых выводов для удобства обслуживания. Сами клеммы также обрабатываем раствором, по окончании работы вытираем батарею насухо чистой ветошью.
В первую очередь проверяем уровень электролита в банках. Для этого использую прозрачную пластиковую трубку, нашедшую в гараже, как выход из положения можно взять прозрачный корпус от шариковой авторучки.
Однако помимо такого параметра, как уровень электролита необходимо знать и его плотность, определить которую можно, использовав ареометр. Прибор покажет и неисправную банку, где плотность будет явно занижена. В средней полосе России плотность должна быть порядка1.27-1.28г/см. При сильных морозах низкая плотность может привести к замерзанию электролита и раздутию её корпуса,
Откручиваем пробки плоской отвёрткой (можно воспользоваться монетой) и поочерёдно начинаем проверку уровня электролита в банках. Опускаем один конец трубки до упора в пластины и зажимаем пальцем второй конец трубки, не отпуская палец, вынимаем трубку и замеряем количество электролита с помощью обычной линейки, приложив к ней конец трубки с электролитом.
В среднем уровень должен быть порядка 10-16мм на свинцовых аккумуляторах и 20-25мм на свинцово-кальциевых аккумуляторах…
Лишнее количество дистиллированной воды, нарушает концентрацию электролита в банках, что снижает его плотность и если воды окажется гораздо больше нормы, то поднять плотность не удастся даже при длительной зарядке батареи,
Плотность показывает степень заряженности батареи, помогая контролировать процесс зарядки.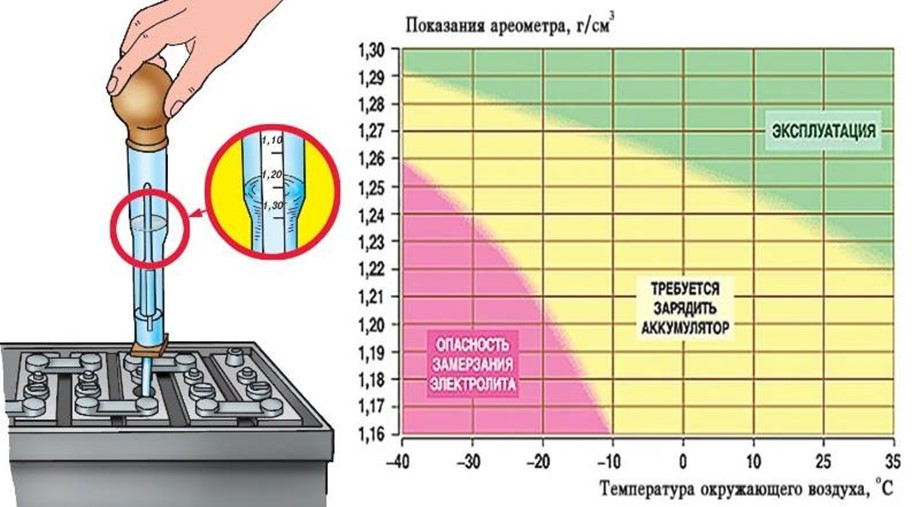
Для поднятия плотности в первой банке отбираем из неё электролит и доливаем корректирующий с плотностью 1,34, то же самое повторяем и с последней банкой, где также низкая плотность.
Теперь поезжу пару недель и вновь проверим уровень и плотность электролита…
Продолжение борьбы за живучесть аккума
Сегодня за бортом -18 градусов холода. Напомню, что было сделано с нашим аккумулятором. В первой банке была низкая плотность, где был добавлен корректирующий электролит, плотностью 1.34, предварительно отобрав старый. Добавлял с помощью медицинского 50г. шприца –сколько отобрал жидкости, столько и добавил. Подобную процедуру провёл и с последней банкой, где тоже была низкая плотность.
Пока езжу на этом аккуме, электролит пускай полностью перемешается, и проверю все параметры батареи…
Пытаемся в итоге запустить мотор, но как видим, аккум не справляется. Поставил на замену годовалый аккумулятор б/у, который предварительно был уже хорошо заряжен.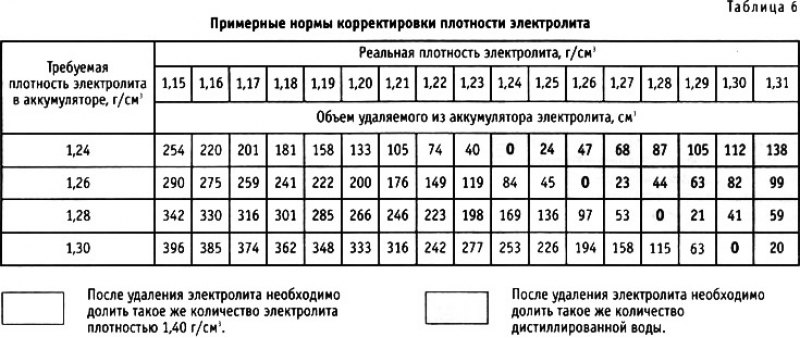 Двигатель сразу же завёлся.
Двигатель сразу же завёлся.
Резюме — аккумулятор с замкнутой банкой требует замены…
Третья попытка спасения нашего аккумулятора
Сульфатация происходит при глубоком разряде батареи, а также при отрицательных значениях температуры и долгом хранение недозаряжённого аккумулятора. В основном на положительных пластинах откладываются кристаллы сульфата свинца в виде налёта, уменьшая площадь пластины и, соответственно, уменьшая ёмкость самой батареи и пусковой ток.
Батарея первый раз стояла на зарядке в режиме цикл порядка 24 часа, потом ещё на сутки оставил в режиме автомат. Сегодня установил заряжать в режиме цикл на 2-3 дня, пока позволяют выходные дни. В этом режиме происходит десульфатация пластин, очищаются пластины от кристаллов сульфата свинца, очищается их поверхность.
При неоднократном сильном разряде батареи, более 60% особенно созданной по технологии кальций-кальций, то такая батарея уже восстановлению не подлежит и потребуется её замена.
Поэтому лучше не доводить до такого состояния и необходимо несколько раз в год заряжать аккумулятор от зарядного устройства. При этом нужно помнить, что перезаряд также опасен для батареи. Так, 1 1 час перезаряда равен 72-м часам её работы на автомобиле.
Резюме…
Если пластины батареи уже выработали свой ресурс и уже не подлежат восстановлению, то спасение такого аккумулятора сравнимо с попыткой введения курса антибиотиков пациентам в морге. Остается его сдать на металлолом продавцам аккумуляторов.
Уделяйте больше внимания аккумулятору, уделяя проверке работы генератора и сезонно проверяя уровень и плотность электролита в каждой банке.
Зарядка АКБ в режиме автомат и цикл видео
Доливка дистиллированной воды и зарядка АКБ в режиме автомат видео
Восстановление аккума в режиме десульфатации видео
Проверка напряжения аккумулятора видео
Как проверить плотность электролита на аккумуляторе видео
Как долить электролит в аккумулятор автомобиля видео
Аккумулятор с замкнутой банкой поменял на б/у видео
Окисление клемм и выводов аккумулятора Рено Логан видео
На этом сегодня всё.
До свидания! Пишите свои комментарии и ставьте лайки.
Читайте также:
Ареометр для замера плотности электролита
Как обслуживать аккумулятор
Как эксплуатировать аккумулятор
Зарядка аккумулятора с прибором кедравто
Добавка дистиллированной воды в аккумулятор
Окисление клемм на аккумуляторе
литий-металлический анод для аккумуляторов
литий-металлический анод для аккумуляторовМун Сек Ким
23 октября 2020 г.
Представлено в качестве курсовой работы для Ph340, Стэнфордский университет, осень 2020 г.
Преимущества использования литий-металлических анодов
Рис. 1: Емкость металлического анода Li
Q A по сравнению с толщиной лития T Li рассчитано с использованием
уравнение (1). |
Металлический литий является идеальным анодным материалом для Li батарей благодаря следующим свойствам. [1]
Низкая плотность: 0,534 г см -3
Низкий восстановительный потенциал: -3,04 В по сравнению с SHE
Высокая теоретическая удельная мощность: 3861 мАч г -1 и 2061 мАч см -3
Низкая плотность лития помогает уменьшить общую массу и объем, что помогает улучшить как гравиметрические, так и объемные емкости и плотность энергии литиевой батареи. Кроме того, низкий восстановительный потенциал Li позволяет ячейке работать при относительно высоком напряжение, которое также увеличивает плотность энергии литиевой батареи.
Теоретическая весовая и объемная емкости литий-металлического анода
| Q г | = | н·Ф·М Вт = 3861,328 мАч г -1 |
| Q v | = | Q г ·ρ = 2061,949 мАч см -3 |
где
| Q г | ≡ | Гравиметрическая емкость Li [мА·ч·г -1 ] |
| п | ≡ | Количество переданных электронов = 1 |
| Ф | ≡ | Постоянная Фарадея = 26,8014814 [Ач моль -1 ] |
| М ш | ≡ | Молекулярная масса Li = 6,941 [г моль -1 |
| Q v | ≡ | Объемная емкость лития [мАч см -3 ] |
| р | ≡ | Плотность Li = 0,534 [г см -3 ] |
Значения производительности, рассчитанные выше, являются верхними
предел всех возможных анодных материалов, которые могут быть использованы в качестве
анод для литиевых аккумуляторов, а это означает, что литий по своей сути является самым высоким
энергоемкий анодный материал для литиевых аккумуляторов. [1-3] Однако эти теоретические
значения трудно достичь в реальности, так как высокая химическая и
электрохимическая активность Li вызывает побочные реакции во время
батарея зацикливается. [4]
[1-3] Однако эти теоретические
значения трудно достичь в реальности, так как высокая химическая и
электрохимическая активность Li вызывает побочные реакции во время
батарея зацикливается. [4]
Повышение плотности энергии батареи путем замены графита на литий Металлический анод
В общем, есть два репрезентативных энергетических метрики плотности для батарей: 1) гравиметрическая плотность энергии (энергия хранится на единицу веса батареи) и 2) объемная плотность энергии (энергия запасается на единицу объема батареи). Низкая плотность Li помогает улучшить гравиметрическую и объемную плотность энергии за счет уменьшение веса и объема анода в батареях. Его низкое снижение потенциал необходим для увеличения рабочего напряжения ячейки (В ячейка ).
Графитовый анод широко используется в коммерческих литий-ионных батареях.
аккумуляторы (LiB). Графитовый анод демонстрирует теоретическую специфику
емкость 372 мАч г -1 .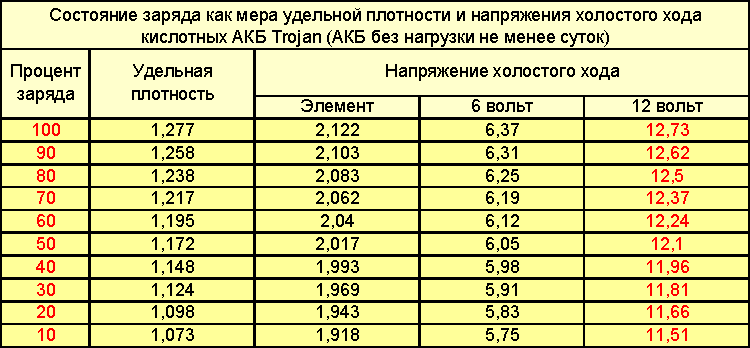 Сравнивая расчетные теоретические
емкость лития (3861 мАч г -1 ), металлический литиевый анод вмещает около 10
имеет более высокую удельную емкость, чем графит. Однако
Основная емкость, которая диктует плотность энергии батареи, — это
разрядная емкость, зависящая от катода. Это потому, что
электрическая энергия получается от батареи во время разряда
процесс. С другой стороны, емкость анода определяет общую
накопление ионов лития в процессе зарядки. В общем,
неравное соотношение мощностей между анодом и катодом используется, когда
создание литиевых аккумуляторов. Соотношение емкости между анодом (
отрицательный электрод) и катод (положительный электрод), известный как N/P
отношение, является важным параметром проектирования ячейки для определения практического
производительность батареи и плотность энергии. [2] Приведенные ниже уравнения
проиллюстрируйте, как рассчитывается плотность энергии батареи.
Сравнивая расчетные теоретические
емкость лития (3861 мАч г -1 ), металлический литиевый анод вмещает около 10
имеет более высокую удельную емкость, чем графит. Однако
Основная емкость, которая диктует плотность энергии батареи, — это
разрядная емкость, зависящая от катода. Это потому, что
электрическая энергия получается от батареи во время разряда
процесс. С другой стороны, емкость анода определяет общую
накопление ионов лития в процессе зарядки. В общем,
неравное соотношение мощностей между анодом и катодом используется, когда
создание литиевых аккумуляторов. Соотношение емкости между анодом (
отрицательный электрод) и катод (положительный электрод), известный как N/P
отношение, является важным параметром проектирования ячейки для определения практического
производительность батареи и плотность энергии. [2] Приведенные ниже уравнения
проиллюстрируйте, как рассчитывается плотность энергии батареи.
Рис. 2: Левое изображение представляет
обычная литий-ионная ячейка с выступающим
гравиметрическая и объемная плотности энергии. Правильный образ
представляет структуру ячейки Li-Metal в заряженном состоянии с
N/P=0,2 вместе с расчетными гравиметрическими и объемными
плотности энергии. Прогнозируемые значения взяты из
Альбертус и др. [4] (Источник: М. С. Ким) 2: Левое изображение представляет
обычная литий-ионная ячейка с выступающим
гравиметрическая и объемная плотности энергии. Правильный образ
представляет структуру ячейки Li-Metal в заряженном состоянии с
N/P=0,2 вместе с расчетными гравиметрическими и объемными
плотности энергии. Прогнозируемые значения взяты из
Альбертус и др. [4] (Источник: М. С. Ким) |
| В ячейка | = | В катод — В анод |
| Е г | = | Q dis ·V ячейка ·M ячейка -1 |
| Е v | = | Q dis ·V ячейка ·N ячейка -1 |
где
| В ячейка | ≡ | Рабочее напряжение элемента [В относительно Li/Li + ] |
| В катод | ≡ | Рабочее напряжение катода [В относительно Li/Li + ] |
| В анод | ≡ | Рабочее напряжение анода [В относительно Li/Li + ] |
| Q дис | ≡ | Разрядная емкость ячейки [Ач] |
| Е г | ≡ | Гравиметрическая плотность энергии [Втч кг -1 ] |
| М ячейка | ≡ | Общий вес ячейки [кг] |
| Е v | ≡ | Объемная плотность энергии [Втч л -1 ] |
| N ячейка | ≡ | Общий объем ячейки [л] |
Плотность энергии батареи зависит от
емкость, рабочее напряжение элемента, вес элемента и объем элемента.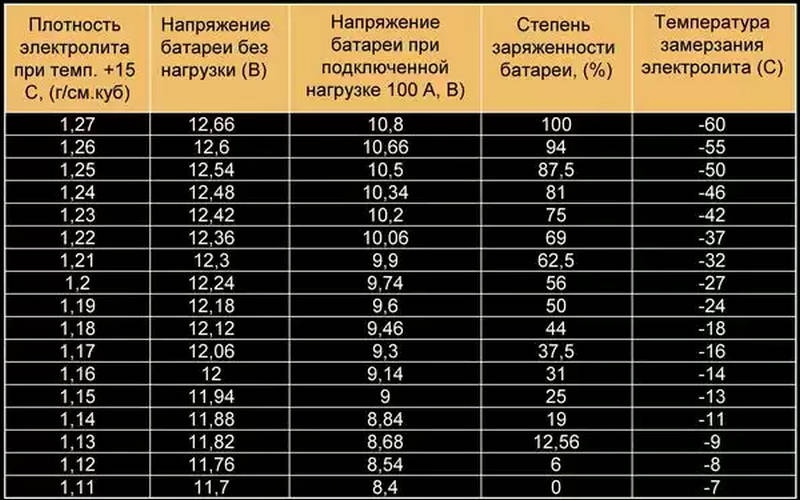 Разрядная емкость используется для расчета плотности энергии батареи. Для
рабочее напряжение ячейки, опорное напряжение всегда относительно
к Ли/Ли + для литиевых аккумуляторов, и это показывает еще одно преимущество
использование металлического литиевого анода вместо графитового. Поскольку ссылка
это Li/Li + , рабочее напряжение для литиевого металлического анода составляет 0 В,
в котором напряжение на ячейке является единственной функцией потенциала катода.
Однако среднее рабочее напряжение графитового анода равно
примерно 0,1 В, при котором в ячейке происходит снижение примерно на 0,1 В
рабочее напряжение. Это снижение напряжения рабочего элемента приводит к
снижение плотности энергии примерно на 3% при условии, что разрядная емкость
одинаковы, а современные катодные материалы демонстрируют средние
рабочее напряжение 3,9V против Li/Li + . [2]
Разрядная емкость используется для расчета плотности энергии батареи. Для
рабочее напряжение ячейки, опорное напряжение всегда относительно
к Ли/Ли + для литиевых аккумуляторов, и это показывает еще одно преимущество
использование металлического литиевого анода вместо графитового. Поскольку ссылка
это Li/Li + , рабочее напряжение для литиевого металлического анода составляет 0 В,
в котором напряжение на ячейке является единственной функцией потенциала катода.
Однако среднее рабочее напряжение графитового анода равно
примерно 0,1 В, при котором в ячейке происходит снижение примерно на 0,1 В
рабочее напряжение. Это снижение напряжения рабочего элемента приводит к
снижение плотности энергии примерно на 3% при условии, что разрядная емкость
одинаковы, а современные катодные материалы демонстрируют средние
рабочее напряжение 3,9V против Li/Li + . [2]
Соотношение N/P для литий-металлической батареи
Отношение N/P описывает соотношение мощностей между
электроды в аккумуляторной ячейке. Интерпретация соотношения N/P
немного отличается в зависимости от литированных состояний катодных материалов.
Кроме того, существует два основных типа механизмов, отвечающих за
электрохимические реакции в аккумуляторах: 1) Интеркаляция и 2)
Механизмы конверсионного типа. [5,6] Механизм интеркаляции
внедрение ионов Li в слоистые структуры (или любые другие
термодинамически благоприятные кристаллические структуры) электродных материалов
(примерами электродов на основе интеркаляции являются графитовый анод и
ЛиНи x Mn y Co z O 2 (NMC)
катод). Таким образом, электродные материалы на основе интеркаляции
считается хозяином для хранения ионов лития. С другой стороны,
Механизм превращения включает образование нового продукта после окислительно-восстановительного процесса.
реакции с ионами лития. Несколько примеров электродов конверсионного типа
материалы: анод из литиевого металла, катод из элементарной серы (S 8 ),
и кислородный (O 2 ) катод.
Интерпретация соотношения N/P
немного отличается в зависимости от литированных состояний катодных материалов.
Кроме того, существует два основных типа механизмов, отвечающих за
электрохимические реакции в аккумуляторах: 1) Интеркаляция и 2)
Механизмы конверсионного типа. [5,6] Механизм интеркаляции
внедрение ионов Li в слоистые структуры (или любые другие
термодинамически благоприятные кристаллические структуры) электродных материалов
(примерами электродов на основе интеркаляции являются графитовый анод и
ЛиНи x Mn y Co z O 2 (NMC)
катод). Таким образом, электродные материалы на основе интеркаляции
считается хозяином для хранения ионов лития. С другой стороны,
Механизм превращения включает образование нового продукта после окислительно-восстановительного процесса.
реакции с ионами лития. Несколько примеров электродов конверсионного типа
материалы: анод из литиевого металла, катод из элементарной серы (S 8 ),
и кислородный (O 2 ) катод. Следовательно, электродные материалы, которые
принять механизм преобразования не рассматриваются в качестве хоста для Li
ионы. Разница в терминах между литий-ионными и литий-металлическими батареями
просто возникает из типов электродных электрохимических реакций. В
Как правило, литий-металлическая батарея относится к любому типу батареи, в которой используется литий.
металл в качестве анода. Таблица 1 поясняет общие термины, введенные в
аккумуляторные поля:
Следовательно, электродные материалы, которые
принять механизм преобразования не рассматриваются в качестве хоста для Li
ионы. Разница в терминах между литий-ионными и литий-металлическими батареями
просто возникает из типов электродных электрохимических реакций. В
Как правило, литий-металлическая батарея относится к любому типу батареи, в которой используется литий.
металл в качестве анода. Таблица 1 поясняет общие термины, введенные в
аккумуляторные поля:
Большинство катодных материалов на основе интеркаляции в литированном состоянии, когда клетки впервые построены, тогда как Катодные материалы конверсионного типа не являются. Это связано с термодинамикой связанных с электродными материалами. Таким образом, интерпретация N/P соотношение немного отличается для каждого из типов батарей. Таблица 2 обобщенные интерпретации отношения N/P для каждого из точных термины батареи, за которыми следует практический диапазон отношений N/P.
| |||||||||||||||
Таблица 1: В этой таблице объясняется термин батареи на основе
на электродных механизмах электрохимических реакций. |
Интерпретация соотношения N/P определяется
электродный механизм электрохимической реакции, в котором интеркаляция
механизм включает литий-ионный носитель, тогда как тип преобразования включает
объемная электрохимическая реакция между Li и катодными частицами. Однако,
Литий-ионный аккумулятор в этом случае является исключением, так как он включает в себя как
механизмы преобразования и интеркаляции в аноде и катоде,
соответственно. Поскольку в катоде уже хранится ион лития
материала (т. е. любых литированных катодов), в идеале не должно быть дополнительных ионов лития.
требуется на аноде для работы батареи. Поэтому новый аккумулятор
термин введен для нулевого отношения N/P для ионно-литиевого аккумулятора, который
безанодный литий-металлический аккумулятор. [7] Кроме того, широко используемый металлический литий
Термин батареи представляет собой отношение N / P больше нуля для ионно-литиевого металла.
батарея. Важно отметить, что термин «литий-металлическая батарея» относится к
любой тип аккумуляторов, в которых в качестве анода используется металлический литий; однако литий-металл
Аккумулятор в полевых условиях часто относится к литий-ионным аккумуляторам.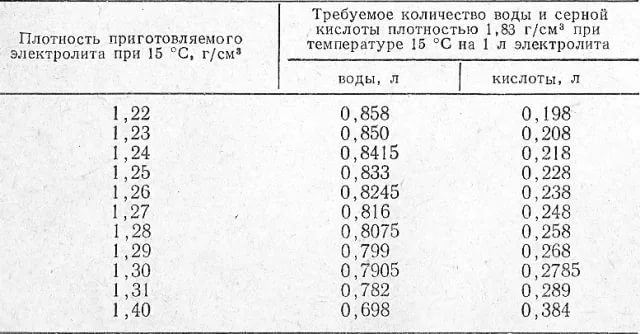 Кроме того, есть две конфигурации, которые описывают ион металла лития.
батареи, которые представляют собой безанодную литий-металлическую конфигурацию (N/P = 0) и
Конфигурация металла лития (N/P > 0).
Кроме того, есть две конфигурации, которые описывают ион металла лития.
батареи, которые представляют собой безанодную литий-металлическую конфигурацию (N/P = 0) и
Конфигурация металла лития (N/P > 0).
| |||||||||||||||
Таблица 2: Интерпретация соотношения N/P в зависимости от батареи
условия. Практический диапазон соотношения N/P в зависимости от срока службы батареи
предоставлен. Практический диапазон соотношения N/P в зависимости от срока службы батареи
предоставлен. |
Расчет соотношения N/P для литий-металлической батареи
Для простоты расчета соотношения N/P для металлического лития
аккумуляторы, часто площадь емкости в мАч см -2 для литиевого металла
используется материал анода и катода. Стоит отметить, что часто
теоретическая емкость Li и практическая емкость катода равны
используется для расчета отношения N/P. Это потому, что металл Li часто
промышленно обработанный в виде тонкой пленки (от 500 мкм до 20
мкм в толщину), а начальная емкость Li не
сильно зависит от условий езды на велосипеде. Однако основная причина
для использования практической мощности, эквивалентно измеренной мощности, для
катода заключается в том, что фактическая емкость катода чувствительна к рабочему
условия, такие как окно рабочего напряжения, скорость C, температура и
и т. д. Поэтому в полевых условиях принято рассматривать измеряемый катод
мощность из определенных рабочих условий для расчета соотношения N/P. Поскольку электроды батареи относительно тонкие, значения емкости
нормализуются по размеру электрода, чтобы получить площадь емкости
анод и катод. Сообщается также о гравиметрических возможностях, но это
стало обычным делом использовать площадные мощности для определения соотношения N/P.
Поскольку анод из литиевого металла представляет собой тонкую пленку, полезное уравнение для
рассчитать соотношение N/P с металлической фольгой лития, соотнеся толщину лития с площадью
емкость. Приведенное ниже уравнение относится к тому, как толщина металлического лития
фольга связана с ее теоретической емкостью.
Поскольку электроды батареи относительно тонкие, значения емкости
нормализуются по размеру электрода, чтобы получить площадь емкости
анод и катод. Сообщается также о гравиметрических возможностях, но это
стало обычным делом использовать площадные мощности для определения соотношения N/P.
Поскольку анод из литиевого металла представляет собой тонкую пленку, полезное уравнение для
рассчитать соотношение N/P с металлической фольгой лития, соотнеся толщину лития с площадью
емкость. Приведенное ниже уравнение относится к тому, как толщина металлического лития
фольга связана с ее теоретической емкостью.
| ||||||||
Таблица 3: Площадь емкости Li с
относительно его толщины. Обратите внимание, что это теоретические
ценности. Толщина рассчитывается исходя из идеального
плоская и гладкая пленка Li. Обратите внимание, что это теоретические
ценности. Толщина рассчитывается исходя из идеального
плоская и гладкая пленка Li. |
| Т Ли | = | 10000 Q А М с n F ρ | (1) |
где
| Т Ли | ≡ | Толщина лития [мкм] |
| Q А | ≡ | емкость Li [мАч см -2 ] |
| М ш | ≡ | молекулярная масса Li = 6,941 [г моль -1 ] |
| п | ≡ | количество переданных электронов = 1 |
| Ф | ≡ | Постоянная Фарадея = 26801,4814 [мА·ч моль -1 ] |
| р | ≡ | плотность Li = 0,534 [г см -3 ] |
Используя приведенное выше уравнение, толщина лития может быть
рассчитывается как функция площади емкости Li или наоборот. В таблице 3 показаны три соответствующие толщины лития на основе трех
репрезентативные площадные мощности, обычно используемые в полевых условиях. Рис. 1 показывает
более полный спектр соответствующей толщины Li на основе
площадная емкость. Кроме того, можно использовать эту диаграмму для быстрой оценки
площадь емкости лития в зависимости от толщины используемой литиевой фольги.
В таблице 3 показаны три соответствующие толщины лития на основе трех
репрезентативные площадные мощности, обычно используемые в полевых условиях. Рис. 1 показывает
более полный спектр соответствующей толщины Li на основе
площадная емкость. Кроме того, можно использовать эту диаграмму для быстрой оценки
площадь емкости лития в зависимости от толщины используемой литиевой фольги.
и соответствующая энергия Плотность
На рис. 2 показано сравнение структуры ячеек между
Литий-ионный элемент и литий-металлический элемент (N/P > 0) с соответствующими компонентами батареи
в ячейке, такие как токосъемники, сепараторы и электроды.
Основываясь на структуре ячеек, конфигурация литий-металлических ячеек увеличивается примерно на
В 1,67 раза выше гравиметрическая плотность энергии и в 3 раза выше
объемная плотность энергии, основанная на конфигурациях литий-ионных элементов.
Обратите внимание, что это прогнозируемые значения, а точные значения могут
изменение на основе различных спецификаций и размеров ячеек; однако,
относительное увеличение плотности энергии является надежным значением. Следовательно, очевидно, что такая конфигурация литий-металлического элемента имеет
большее преимущество улучшения объемной плотности энергии, чем
гравиметрическая плотность энергии литиевой батареи. Электромобилям требуется
высокая объемная плотность энергии из-за ограниченного пространства
форм-фактором автомобиля, а на трансмиссию не так сильно влияет
дополнительный вес автомобиля. Это стало основным драйвером развития
литий-металлические батареи, и все еще продолжаются исследования по дальнейшему
улучшить плотность энергии литиевых батарей.
Следовательно, очевидно, что такая конфигурация литий-металлического элемента имеет
большее преимущество улучшения объемной плотности энергии, чем
гравиметрическая плотность энергии литиевой батареи. Электромобилям требуется
высокая объемная плотность энергии из-за ограниченного пространства
форм-фактором автомобиля, а на трансмиссию не так сильно влияет
дополнительный вес автомобиля. Это стало основным драйвером развития
литий-металлические батареи, и все еще продолжаются исследования по дальнейшему
улучшить плотность энергии литиевых батарей.
Сообщалось, что гравиметрическая энергия
плотность литий-металлических аккумуляторов (N/P > 0) можно повысить за счет
систематическая оптимизация параметров батареи. [2-4] Существует множество
параметры, влияющие на плотность энергии батареи, такие как отношение N/P,
загрузка электролита, типы и емкости катодов, насыпная плотность
катод, толщина сепаратора, толщина токосъемника, рабочая
окно напряжения, неактивные компоненты батареи и т. д. Оптимизируя
вышеупомянутые параметры, литий-металлический аккумулятор способен превзойти 500
Втч кг -1 . [2] Благодаря улучшенной плотности энергии пробег
пробег электромобилей может быть увеличен примерно с 300 миль до 600 миль.
миль.
д. Оптимизируя
вышеупомянутые параметры, литий-металлический аккумулятор способен превзойти 500
Втч кг -1 . [2] Благодаря улучшенной плотности энергии пробег
пробег электромобилей может быть увеличен примерно с 300 миль до 600 миль.
миль.
Безанодный литий-металлический элемент (N/P=0) является идеальным
конфигурация ячейки, так как в ячейке нет избытка Li. Таким образом
безанодный литий-металлический аккумулятор считается «Святым Граалем» для Li
батарея. Благодаря безанодной конфигурации литий-металлического элемента практичность
объемная плотность энергии 1200 Втч л -1 достигается при
уровень стека. [3] Это многообещающий результат для развития более
надежные электромобили. Хотя улучшение батарей требует интенсивного
исследований и разработок, скоро появятся высокопроизводительные литиевые батареи.
реализована, и эта усовершенствованная аккумуляторная технология действительно будет способствовать дальнейшему
способствовать 4 й промышленной революции.
© Мун Сек Ким. Автор гарантирует, что произведение принадлежит автору, и что Стэнфордский университет не предоставил никакой другой информации. чем руководство по набору текста и ссылкам. Автор предоставляет разрешение копировать, распространять и отображать эту работу в неизменном виде, со ссылкой на автора, только в некоммерческих целях. Все другие права, включая коммерческие права, сохраняются за автор.
Ссылки
[1] Д. Лин, Ю. Лю и Ю. Цуй, «Возрождение литиевых Анод металлический для аккумуляторов высокой энергии», Нац. нанотехнолог. 12 , 194 (2017).
[2] J. Liu et al. , «Пути практического Высокоэнергетические литий-металлические батареи с длительным циклом», Nat. Energy 4 , 180 (2019).
[3] A.J.Louli et al. , «Диагностика и
Исправление отказа безанодной ячейки с помощью электролита и морфологических
Анализ», Нац. Энергия 5 , 693 (2020).
Энергия 5 , 693 (2020).
[4] П. Альбертус и др. , «Статус и проблемы в использовании литий-металлического электрода для высокоэнергетических и недорогих Аккумуляторы», Nat. Energy 3 , 16 (2018).
[5] J. Zheng et al. , «Регулирование Электроосаждение морфологии лития: на пути к коммерческой значимости Вторичные литий-металлические батареи, Chem. Soc. Rev. 49 , 2701 (2020).
[6] Х.-Б. Ченг и др. , «На пути к безопасному литию Металлический анод в перезаряжаемых батареях: обзор», Chem. Rev. 117 , 10403 (2017).
[7] Ж.-Г. Чжан, «Без анода», Nat. Энергия. 4 , 637 (2019).
Три аккумуляторные технологии, которые могут обеспечить энергией будущее | Saft
Миру нужно больше энергии, желательно в чистой и возобновляемой форме. Наши стратегии хранения энергии в настоящее время формируются за счет литий-ионных аккумуляторов, являющихся передовыми технологиями, но на что мы можем рассчитывать в ближайшие годы?
Начнем с основных сведений об аккумуляторах.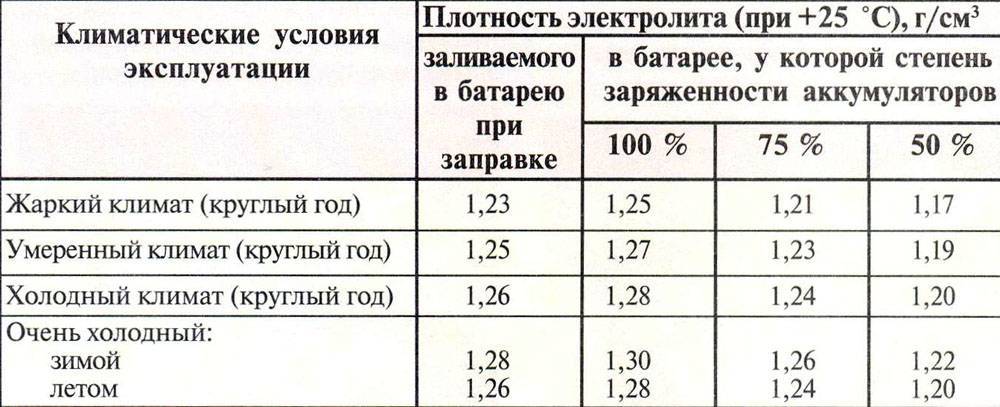 Батарея представляет собой набор из одного или нескольких элементов, каждый из которых имеет положительный электрод (катод), отрицательный электрод (анод), сепаратор и электролит. Использование для них различных химикатов и материалов влияет на свойства батареи — сколько энергии она может хранить и выдавать, сколько энергии она может обеспечить или сколько раз ее можно разряжать и перезаряжать (также называемая циклической емкостью).
Батарея представляет собой набор из одного или нескольких элементов, каждый из которых имеет положительный электрод (катод), отрицательный электрод (анод), сепаратор и электролит. Использование для них различных химикатов и материалов влияет на свойства батареи — сколько энергии она может хранить и выдавать, сколько энергии она может обеспечить или сколько раз ее можно разряжать и перезаряжать (также называемая циклической емкостью).
Аккумуляторные компании постоянно экспериментируют, чтобы найти более дешевые, плотные, легкие и более мощные химические вещества. Мы поговорили с Патриком Бернардом, директором по исследованиям Saft, который рассказал о трех новых аккумуляторных технологиях с трансформационным потенциалом.
ЛИТИЙ-ИОННЫЕ АККУМУЛЯТОРЫ НОВОГО ПОКОЛЕНИЯ
Что это?
В литий-ионных (литий-ионных) аккумуляторах накопление и высвобождение энергии обеспечивается перемещением ионов лития от положительного электрода к отрицательному туда и обратно через электролит. В этой технологии положительный электрод действует как первоначальный источник лития, а отрицательный электрод — как носитель лития. Несколько химических элементов собраны под названием литий-ионных аккумуляторов в результате десятилетий отбора и оптимизации, близких к совершенству положительных и отрицательных активных материалов. Литированные оксиды металлов или фосфаты являются наиболее распространенным материалом, используемым в качестве материалов для положительных положительных результатов. Графит, а также графит/кремний или литированные оксиды титана используются в качестве негативных материалов.
В этой технологии положительный электрод действует как первоначальный источник лития, а отрицательный электрод — как носитель лития. Несколько химических элементов собраны под названием литий-ионных аккумуляторов в результате десятилетий отбора и оптимизации, близких к совершенству положительных и отрицательных активных материалов. Литированные оксиды металлов или фосфаты являются наиболее распространенным материалом, используемым в качестве материалов для положительных положительных результатов. Графит, а также графит/кремний или литированные оксиды титана используются в качестве негативных материалов.
Ожидается, что в ближайшие годы литий-ионная технология достигнет предела энергопотребления при использовании реальных материалов и конструкций элементов. Тем не менее, недавние открытия новых семейств прорывных активных материалов должны разблокировать нынешние ограничения. Эти инновационные соединения могут хранить больше лития в положительных и отрицательных электродах и впервые позволят объединить энергию и мощность. Кроме того, с этими новыми соединениями также учитываются дефицит и критичность сырья.
Кроме того, с этими новыми соединениями также учитываются дефицит и критичность сырья.
Каковы его преимущества?
Сегодня среди всех современных технологий хранения данных технология литий-ионных аккумуляторов обеспечивает самый высокий уровень плотности энергии. Такие характеристики, как быстрая зарядка или рабочий температурный диапазон (от -50°C до 125°C), могут быть точно настроены благодаря большому выбору конструкций элементов и химических составов. Кроме того, литий-ионные аккумуляторы обладают дополнительными преимуществами, такими как очень низкий саморазряд и очень долгий срок службы, а также цикличность, обычно тысячи циклов зарядки/разрядки.
Когда его ожидать?
Ожидается, что новое поколение передовых литий-ионных аккумуляторов будет развернуто до первого поколения твердотельных аккумуляторов. Они идеально подходят для использования в таких приложениях, как системы хранения энергии для возобновляемых источников энергии и транспорта (морского, железнодорожного, авиационного и внедорожного), где требуется высокая энергия, высокая мощность и безопасность.
АККУМУЛЯТОРЫ СЕРНЫЕ ЛИТИЙ
Что это такое?
В литий-ионных батареях ионы лития накапливаются в активных материалах, действующих как стабильные структуры-хозяева во время заряда и разряда. В литий-серных (Li-S) батареях нет структур-хозяев. При разрядке литиевый анод расходуется, а сера превращается в различные химические соединения; при зарядке происходит обратный процесс.
Каковы его преимущества?
В Li-S аккумуляторе используются очень легкие активные материалы: сера в положительном электроде и металлический литий в качестве отрицательного электрода. Вот почему его теоретическая плотность энергии чрезвычайно высока: в четыре раза больше, чем у литий-иона. Это делает его подходящим для авиационной и космической промышленности.
Компания Saft выбрала и одобрила наиболее многообещающую технологию Li-S на основе твердотельного электролита. Этот технический путь обеспечивает очень высокую плотность энергии, длительный срок службы и устраняет основные недостатки жидкого Li-S (ограниченный срок службы, высокий саморазряд и т. д.).
д.).
Кроме того, эта технология дополняет твердотельные литий-ионные благодаря своей превосходной гравиметрической плотности энергии (+30% на кону в Втч/кг).
Когда ждать?
Основные технологические барьеры уже преодолены, и уровень зрелости очень быстро приближается к полномасштабным прототипам.
Ожидается, что эта технология появится на рынке сразу после полупроводниковых литий-ионных аккумуляторов для приложений, требующих длительного времени автономной работы.
ТВЕРДОТЕЛЬНЫЕ БАТАРЕИ
Что это такое?
Твердотельные батареи представляют собой смену парадигмы с точки зрения технологии. В современных литий-ионных батареях ионы перемещаются от одного электрода к другому через жидкий электролит (это также называется ионной проводимостью). В полностью твердотельных батареях жидкий электролит заменен твердым соединением, которое, тем не менее, позволяет ионам лития мигрировать внутри него. Эта концепция далеко не нова, но за последние 10 лет — благодаря интенсивным исследованиям во всем мире — были открыты новые семейства твердых электролитов с очень высокой ионной проводимостью, аналогичной жидкому электролиту, что позволило преодолеть этот особый технологический барьер.
Эта концепция далеко не нова, но за последние 10 лет — благодаря интенсивным исследованиям во всем мире — были открыты новые семейства твердых электролитов с очень высокой ионной проводимостью, аналогичной жидкому электролиту, что позволило преодолеть этот особый технологический барьер.
Сегодня усилия компании Saft Research & Development сосредоточены на двух основных типах материалов: полимерах и неорганических соединениях с целью синергии физико-химических свойств, таких как технологичность, стабильность, проводимость…
Каковы его преимущества?
Первым огромным преимуществом является заметное повышение безопасности на уровне элемента и батареи: твердые электролиты негорючи при нагревании, в отличие от их жидких аналогов. Во-вторых, он позволяет использовать инновационные высоковольтные материалы с высокой емкостью, что позволяет создавать более плотные и легкие батареи с более длительным сроком хранения в результате снижения саморазряда. Более того, на системном уровне это принесет дополнительные преимущества, такие как упрощенная механика, а также управление температурой и безопасностью.
